1 . 电子工业常用 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有___________ 。
(2) 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为___________ 。
(3)试剂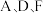 的化学式分别是
的化学式分别是___________ 、___________ 、___________ 。用 溶液制取
溶液制取 晶体的方法是
晶体的方法是___________ 。
A.蒸发结晶 B.降温结晶
 左右的
左右的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得 溶液,某同学设计如图方案:
溶液,某同学设计如图方案: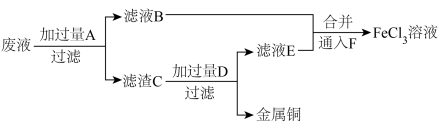
 的
的 溶液,需要的主要玻璃仪器除了量筒外还有
溶液,需要的主要玻璃仪器除了量筒外还有(2)
 溶液与铜箔发生反应的离子方程式为
溶液与铜箔发生反应的离子方程式为(3)试剂
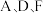 的化学式分别是
的化学式分别是 溶液制取
溶液制取 晶体的方法是
晶体的方法是A.蒸发结晶 B.降温结晶
您最近一年使用:0次
名校
解题方法
2 . 配制溶液:
称量→溶解→冷却→操作①→洗涤→注入→混匀→操作②→摇匀→装瓶贴标签
(1)操作①为___________ 、操作②为___________ 。
(2)用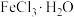 配制
配制 溶液时,应称量
溶液时,应称量___________ g固体(保留两位小数),需要的定量仪器为___________ 。
(3)配置溶液时,不慎掉入镀层缺损的镀铜小铁钉,写出可能发生的反应的离子方程式___________ 。
称量→溶解→冷却→操作①→洗涤→注入→混匀→操作②→摇匀→装瓶贴标签
(1)操作①为
(2)用
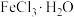 配制
配制 溶液时,应称量
溶液时,应称量(3)配置溶液时,不慎掉入镀层缺损的镀铜小铁钉,写出可能发生的反应的离子方程式
您最近一年使用:0次
名校
解题方法
3 . 四氧化三铁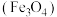 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
(1)中国科学院上海硅酸盐研究所研制出“纳米药物分子运输车”,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是___________。
(2)① 能和稀硫酸反应,写出反应的离子方程式
能和稀硫酸反应,写出反应的离子方程式___________ 。
②验证反应后溶液中含有 的最恰当的试剂是
的最恰当的试剂是___________ 。
A.氯水 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D. 溶液
溶液
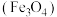 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。(1)中国科学院上海硅酸盐研究所研制出“纳米药物分子运输车”,该“运输车”可提高肿瘤的治疗效果,其结构如图所示。下列有关说法正确的是___________。

| A.该“运输车”中四氧化三铁和二氧化硅都属于氧化物 |
| B.四氧化三铁起到“磁性导航仪”的作用 |
| C.该“运输车”属于混合物 |
| D.该“运输车”分散于水中所得的分散系属于胶体 |
 能和稀硫酸反应,写出反应的离子方程式
能和稀硫酸反应,写出反应的离子方程式②验证反应后溶液中含有
 的最恰当的试剂是
的最恰当的试剂是A.氯水 B.酸性高锰酸钾溶液 C.硫氰化钾溶液 D.
 溶液
溶液
您最近一年使用:0次
名校
解题方法
4 . 以废铁屑(含少量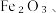 FeS等杂质)为原料,制备硫酸亚铁晶体
FeS等杂质)为原料,制备硫酸亚铁晶体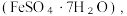 流程示意图如下:
流程示意图如下: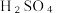 的作用是
的作用是
_________ (用离子方程式表示)。过程中产生的有毒气体,可用___________ 溶液吸收。
(2)酸浸时间对所得溶液的成分影响如下表所示。
用文字说明导致上述颜色变化的可能原因。___________
(3)已知: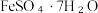 受热易失水,则操作X为:蒸发浓缩、
受热易失水,则操作X为:蒸发浓缩、________ 、过滤、洗涤。FeSO4强热后继续分解,推测产物为___________ 、Fe2O3和SO3。
测定所得硫酸亚铁晶体中的含量,步骤如下:
Ⅰ.称取ag硫酸亚铁晶体样品,配制成100mL溶液。
Ⅱ.取出10mL溶液,加入适量稀硫酸,滴入 的
的 溶液,至反应完全,共消耗
溶液,至反应完全,共消耗 溶液cmL。(反应原理:
溶液cmL。(反应原理:
(4)计算硫酸亚铁晶体样品中 质量分数
质量分数___________ 。
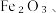 FeS等杂质)为原料,制备硫酸亚铁晶体
FeS等杂质)为原料,制备硫酸亚铁晶体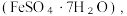 流程示意图如下:
流程示意图如下:
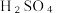 的作用是
的作用是
(2)酸浸时间对所得溶液的成分影响如下表所示。
| 酸浸时间 | 1min | 30min | 120min |
| 用KSCN溶液检验 | 变红 | 未变红 | 变红 |
(3)已知:
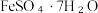 受热易失水,则操作X为:蒸发浓缩、
受热易失水,则操作X为:蒸发浓缩、测定所得硫酸亚铁晶体中的含量,步骤如下:
Ⅰ.称取ag硫酸亚铁晶体样品,配制成100mL溶液。
Ⅱ.取出10mL溶液,加入适量稀硫酸,滴入
 的
的 溶液,至反应完全,共消耗
溶液,至反应完全,共消耗 溶液cmL。(反应原理:
溶液cmL。(反应原理:
(4)计算硫酸亚铁晶体样品中
 质量分数
质量分数
您最近一年使用:0次
名校
5 . 根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、氨水、HI(强酸)溶液、 溶液、NaCl溶液、NaOH溶液
溶液、NaCl溶液、NaOH溶液
①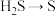 的离子方程式:
的离子方程式:____________ 。
② 的离子方程式:
的离子方程式:____________ 。
③ (两性氧化物)
(两性氧化物) 的
的化学方程式 :____________ 。
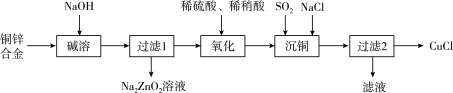
(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:化学方程式 :____________ 。
②写出氧化步骤时发生的主要反应的离子方程式:____________ 。
③写出沉铜步骤时发生的主要反应的离子方程式:____________ 。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、氨水、HI(强酸)溶液、
 溶液、NaCl溶液、NaOH溶液
溶液、NaCl溶液、NaOH溶液①
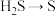 的离子方程式:
的离子方程式:②
 的离子方程式:
的离子方程式:③
 (两性氧化物)
(两性氧化物) 的
的(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:
②写出氧化步骤时发生的主要反应的离子方程式:
③写出沉铜步骤时发生的主要反应的离子方程式:
您最近一年使用:0次
6 . 回答下列问题
(1)电子工业常用的30%的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为______ ,检验溶液中还有 的试剂
的试剂______ .
(2)工业上制取漂白粉的化学反应方程式为______ ;
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为______ .
(1)电子工业常用的30%的
 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为 的试剂
的试剂(2)工业上制取漂白粉的化学反应方程式为
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为
您最近一年使用:0次
解题方法
7 . 各物质的转化关系如下图所示,请完成下列空白。
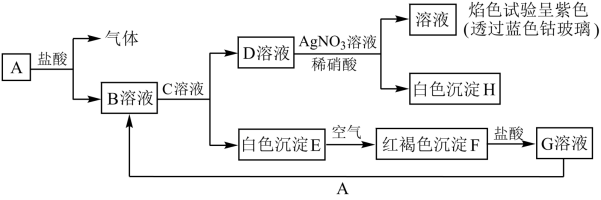
(1)写出B和D 的化学式:B___________ ;D___________ 。
(2)写出E F的化学方程式:
F的化学方程式:___________ 。
(3)向G溶液中加入A,写出反应的离子方程式___________ 。
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子___________ 。

(1)写出B和D 的化学式:B
(2)写出E
 F的化学方程式:
F的化学方程式:(3)向G溶液中加入A,写出反应的离子方程式
(4)设计实验检验A与盐酸反应后溶液中存在的阳离子
您最近一年使用:0次
8 . Ⅰ.中国“奋斗号”载人潜水器在马里亚纳海沟成功坐底深度10909米,挑战了全球海洋最深处。国产新型钛合金、能源供给锂电池等功不可没。磷酸亚铁锂(LiFePO4)可作为锂电池的正极材料,请回答下列问题:
(1)潜水器外壳使用的钛合金
| A.耐高压 | B.耐腐蚀 | C.硬度小 | D.密度小 |
(2)磷酸亚铁锂(LiFePO4)中Fe的化合价为
(3)铁元素的相关信息如图所示,其相对原子质量是

(4)有关铁的性质,说法正确的是________。
| A.在空气中,加热Fe(OH)2可得FeO |
| B.一定条件下,Fe 能与水蒸气反应生成H2 |
| C.常温下,Fe与浓硫酸能反应生成SO2 |
| D.实验室用FeCl3溶液与NaOH溶液反应制备Fe(OH)3胶体 |
(5)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是________。
| A.Fe | B.FeO | C.Fe2O3 | D.Fe3O4 |
(6)要检验Fe3+,可选用的试剂是________。
| A.KSCN 溶液 | B.KMnO4溶液 | C.稀硝酸 | D.BaCl2溶液 |
Ⅱ.钠是生活中常见的金属元素,其多种化合物因其特殊性质在生活中都有广泛应用,例如,NaHCO3可用作食品膨松剂、Na2O2可用作供氧剂等。
(7)NaHCO3可用作膨松剂,原因是
(8)下列电离方程式正确的是________。
| A.NaOH = Na+ + O2-+ H+ | B.H2O = H+ + OH- |
C.HClO ClO-+ H+ ClO-+ H+ | D.CH3COONH4 CH3COO-+ NH4+ CH3COO-+ NH4+ |
(9)钠与滴加酚酞的水反应时
| A.钠浮在水面上 | B.钠熔成小球 | C.钠静止在水面上 | D.溶液变为红色 |
(10)Na2O2可作载人潜水器供氧剂,下列关于Na2O2说法正确的是________。
| A.只有离子键 | B.可在常温下由Na与O2反应制得 |
| C.Na2O2与H2O发生化合反应 | D.Na2O2与CO2反应有O2生成 |
您最近一年使用:0次
解题方法
9 . 铁及其化合物与生产、生活关系密切
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为__________
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是__________ (用化学方程式表示)
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
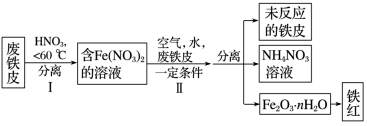
①步骤Ⅰ若要检验是否有Fe3+生成,方法是__________
②步骤Ⅱ中发生反应: ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是__________ (任写一项)。
(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
①K2FeO4中铁元素的化合价__________ ;配平上述反应__________ 。此过程中氧化剂是__________ (填化学式)。
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是__________ 、__________ 。
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ若要检验是否有Fe3+生成,方法是
②步骤Ⅱ中发生反应:
 ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH
 ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O①K2FeO4中铁元素的化合价
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是
您最近一年使用:0次
名校
解题方法
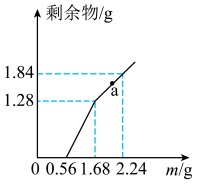
10 . 向 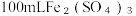 和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
(1)加入少量铁粉时,发生的离子反应______________ 。
(2)原溶液中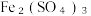 和CuSO4的物质的量之比为
和CuSO4的物质的量之比为_______ 。
(3)a点时溶液中溶质的物质的量浓度为____________ 。
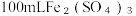 和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
(1)加入少量铁粉时,发生的离子反应
(2)原溶液中
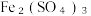 和CuSO4的物质的量之比为
和CuSO4的物质的量之比为(3)a点时溶液中溶质的物质的量浓度为
您最近一年使用:0次



