名校
1 . 实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料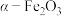 。其主要实验流程如下:
。其主要实验流程如下:
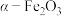 。其主要实验流程如下:
。其主要实验流程如下:
| A.酸浸:用一定浓度的硫酸浸取铁泥,能提高铁元素浸出率的措施有适当升高温度,加快搅拌速度 |
B.还原:向“酸浸”后的滤液中加入过量铁粉,可用KSCN溶液检验 是否完全还原 是否完全还原 |
C.沉铁:将提纯后的 溶液与氨水 溶液与氨水 混合溶液反应,生成 混合溶液反应,生成 沉淀的离子方程式为 沉淀的离子方程式为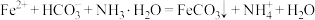 |
D.沉铁步骤中为防止生成 ,应在搅拌下向氨水 ,应在搅拌下向氨水 混合溶液中缓慢加入 混合溶液中缓慢加入 溶液 溶液 |
您最近一年使用:0次
2024-02-29更新
|
563次组卷
|
5卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
名校
解题方法
2 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液 | 溶液颜色变红 | 溶液X含有Fe3+ |
| B | 向饱和的Na2CO3溶液通入CO2 | 产生白色沉淀 | 溶解度:NaHCO3<Na2CO3 |
| C | 向Fe2O3、CuO、Fe的混合粉末中加入过量稀盐酸 | 析出红色固体 | 反应后溶液中阳离子只有H+和Fe2+ |
| D | 取少量溶液Y,先滴加稀硝酸酸化,再滴加适量AgNO3溶液 | 生成白色沉淀 | Y溶液中有Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-22更新
|
125次组卷
|
2卷引用:湖南省株洲市第二中学2021届高三下学期第三次模拟考试化学试卷
3 . 某化学学习小组在实验室制备无水三氯化铁,其实验装置如图。三氯化铁是棕黄色、易潮解、100℃能升华的物质。
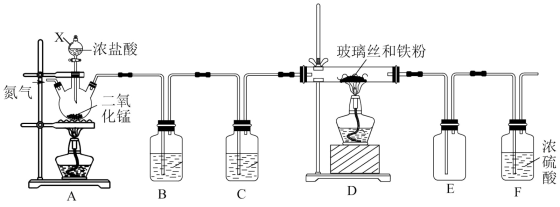
回答下列问题:
(1)装置A中三颈烧瓶里反应的离子方程式是_______ 。
(2)为得到纯净、干燥的Cl2,B、C中的试剂分别为_______ 、_______ 。
(3)实验开始前先通氮气的目的是_______ 。
(4)为使氯气与铁充分反应,应注意的操作是_______ 。
(5)请你评价该装置的主要缺点是_______ 。
(6)设计实验证明D中反应产物中一定含有Fe3+:(要求有试剂、现象和操作)_______ 。

回答下列问题:
(1)装置A中三颈烧瓶里反应的离子方程式是
(2)为得到纯净、干燥的Cl2,B、C中的试剂分别为
(3)实验开始前先通氮气的目的是
(4)为使氯气与铁充分反应,应注意的操作是
(5)请你评价该装置的主要缺点是
(6)设计实验证明D中反应产物中一定含有Fe3+:(要求有试剂、现象和操作)
您最近一年使用:0次
2024-04-03更新
|
48次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
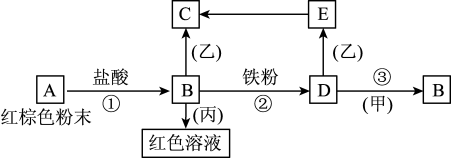
4 . 下列物质之间有如下反应关系:
(1)写出下列物质的化学式:
A___________ B___________ D___________ 甲___________ 乙___________ 丙___________ ;
(2)写出E→C反应的化学方程式:___________ ;
(3)写出B+丙反应的离子方程式:___________ 。
(1)写出下列物质的化学式:
A
(2)写出E→C反应的化学方程式:
(3)写出B+丙反应的离子方程式:
您最近一年使用:0次
解题方法
5 . 有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
| A.盐酸 | B.烧碱溶液 | C.氨水 | D.KSCN溶液 |
您最近一年使用:0次
6 . 某同学利用如图所示装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
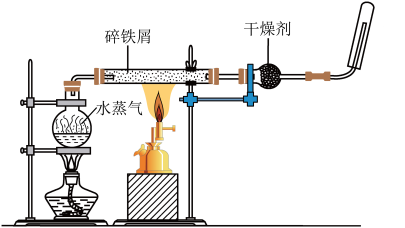
(1)试管中发生反应的化学方程式为___________ 。
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是___________ (只有一个选项符合题意),若溶液未变红,则试管中固体是___________ (只有一个选项符合题意)。
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关反应的化学方程式___________ 。
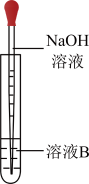
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色。由此可知,实验室FeCl2溶液需现用现配的原因是___________ ,并且配制时应加入少量___________ 。

(1)试管中发生反应的化学方程式为
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关反应的化学方程式

(4)一段时间后,该同学发现(2)中未变红的溶液变成红色。由此可知,实验室FeCl2溶液需现用现配的原因是
您最近一年使用:0次
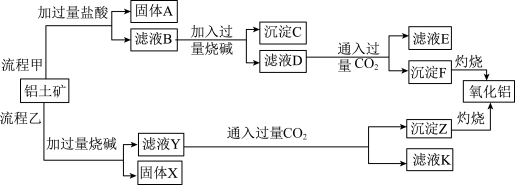
7 . 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取Al2O3粗产品的两种工艺流程如图:(已知:SiO2不溶于盐酸)
(1)流程甲加入盐酸后生成Fe3+的离子方程式为___________ ;验证滤液B中是否含Fe3+,可取少量滤液并加入___________ (填试剂名称)检验。
(2)固体A的主要成分是___________ ,沉淀C的主要成分是___________ (填化学式)。
(3)流程乙中,过量烧碱与Al2O3反应的离子方程式为___________ 。
(4)滤液E中溶质的主要成分是________ (填化学式),写出该物质的一种用途_________ 。
(1)流程甲加入盐酸后生成Fe3+的离子方程式为
(2)固体A的主要成分是
(3)流程乙中,过量烧碱与Al2O3反应的离子方程式为
(4)滤液E中溶质的主要成分是
您最近一年使用:0次
名校
解题方法
8 . 下列各组离子在选项条件下一定能大量共存的是
A.无色溶液:Na+、Cu2+、Cl−、 |
B.酸性溶液: 、Fe3+、S2−、 、Fe3+、S2−、 |
C.遇酚酞变红的溶液:Na+、K+、 、 、 |
D.碱性溶液:K+、Al3+、 、 、 |
您最近一年使用:0次
9 . 下列变化只有加入氧化剂才能实现的是
| A.FeCl3→FeCl2 | B.KMnO4→Mn2+ |
| C.HCl→Cl2 | D.H2O2→O2 |
您最近一年使用:0次
名校
10 . 下列化学用语表达正确的是
| A.乙烯的实验式:C2H4 |
| B.用FeCl3溶液“腐蚀”覆铜板:Fe3++Cu=Fe2++Cu2+ |
C.NH4Cl在水中的电离方程式:NH4Cl  +Cl- +Cl- |
D.用电子式表示NaCl的形成过程: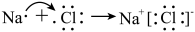 |
您最近一年使用:0次



