解题方法
1 . 某工厂的废金属屑中主要成分为 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体
,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体 和胆矾晶体
和胆矾晶体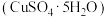 。
。

(1)步骤Ⅰ中,发生的非氧化还原反应的离子方程式为_______ ,涉及到的分离操作是_______ ,该分离操作中常用的玻璃仪器有_______ 。
(2)步骤Ⅱ中,发生反应的离子方程式为_______ 。若用大理石与浓盐酸制取 并通入溶液
并通入溶液 中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体
中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体 减少,可采取的改进措施是
减少,可采取的改进措施是_______ 。
(3)试剂 是
是_______ ,溶液 在空气中易被氧化,设计一个简单的实验方案检验溶液
在空气中易被氧化,设计一个简单的实验方案检验溶液 是否被氧化
是否被氧化_______ 。选择合理试剂确定溶液 未被全部氧化,可选择
未被全部氧化,可选择_______ 试剂。
①氯水② 溶液③
溶液③ 溶液④
溶液④ 酸性溶液
酸性溶液
(4) 溶液制取胆矾晶体需经过
溶液制取胆矾晶体需经过_______ 、冷却结晶、过滤、干燥得到胆矾晶体。
(5)若实验室称取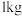 废金属
废金属 含铁元素
含铁元素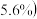 进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到
进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到_______  绿矾
绿矾 。
。
 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体
,为变废为宝,该工厂利用废金属制取氯化铝、绿矾晶体 和胆矾晶体
和胆矾晶体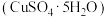 。
。
(1)步骤Ⅰ中,发生的非氧化还原反应的离子方程式为
(2)步骤Ⅱ中,发生反应的离子方程式为
 并通入溶液
并通入溶液 中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体
中,一段时间后,观察到溶液中产生的白色沉淀逐渐减少,为避免固体 减少,可采取的改进措施是
减少,可采取的改进措施是(3)试剂
 是
是 在空气中易被氧化,设计一个简单的实验方案检验溶液
在空气中易被氧化,设计一个简单的实验方案检验溶液 是否被氧化
是否被氧化 未被全部氧化,可选择
未被全部氧化,可选择①氯水②
 溶液③
溶液③ 溶液④
溶液④ 酸性溶液
酸性溶液(4)
 溶液制取胆矾晶体需经过
溶液制取胆矾晶体需经过(5)若实验室称取
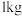 废金属
废金属 含铁元素
含铁元素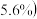 进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到
进行实验,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到 绿矾
绿矾 。
。
您最近一年使用:0次
解题方法
2 . 已知A为常见的金属单质,根据如图所示的关系,请回答下列问题。
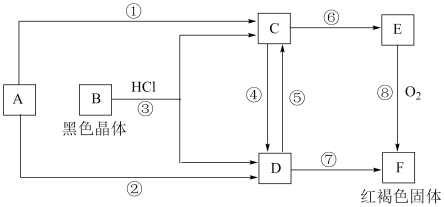
(1)写出下列物质的化学式A:___________ 、B:___________ 、D:___________ 、F:___________ 。
(2)写出反应③的离子方程式:___________ 。
(3)写出反应⑧的化学方程式:___________ 。
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:___________ 。
(5)检验D中金属阳离子操作方法是___________ 。

(1)写出下列物质的化学式A:
(2)写出反应③的离子方程式:
(3)写出反应⑧的化学方程式:
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:
(5)检验D中金属阳离子操作方法是
您最近一年使用:0次
名校
3 . 金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1) 溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为
溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为___________ 。
(2)经检测某酸性废水中所含离子及其浓度如表所示:
则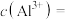
___________ mol/L。
(3)已知 的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:
的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:___________ 。
(4)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是___________ 、___________ 。
② 在空气中加热反应生成
在空气中加热反应生成 时,氧化剂和还原剂的物质的量之比为
时,氧化剂和还原剂的物质的量之比为___________ 。
(5)用托盘天平(1g以下用游码)称量绿矾( )晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是
)晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是___________ 。
a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻线,未补加水
d.定容时,俯视刻度线
(1)
 溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为
溶液用于腐蚀铜箔印刷线路板,该反应的离子方程式为(2)经检测某酸性废水中所含离子及其浓度如表所示:
| 离子 |  |  |  |  |  |
浓度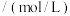 | 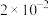 | 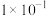 | 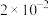 | 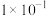 |
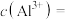
(3)已知
 的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:
的高纯度结晶体是一种紫色潮解性固体,适用于制磁性氧化铁纳米粉末。写出磁性氧化铁与足量稀硝酸反应的化学方程式:(4)氧化铁是重要的工业颜料,用废铁屑制备它的流程如图:

①完成“操作Ⅰ”所需要的玻璃仪器除烧杯外,还需要的是
②
 在空气中加热反应生成
在空气中加热反应生成 时,氧化剂和还原剂的物质的量之比为
时,氧化剂和还原剂的物质的量之比为(5)用托盘天平(1g以下用游码)称量绿矾(
 )晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是
)晶体配制450mL0.1mol/L溶液,以下实验操作会导致所配溶液浓度偏低的是a.用托盘天平称量绿矾晶体时,将砝码放在左盘,药品放在右盘
b.洗涤烧杯和玻璃棒后,将洗涤液倒入废液缸中
c.摇匀后发现液面低于刻线,未补加水
d.定容时,俯视刻度线
您最近一年使用:0次
2023-07-15更新
|
330次组卷
|
3卷引用:安徽省黄山市2022-2023学年高一上学期期末质量检测化学试题
安徽省黄山市2022-2023学年高一上学期期末质量检测化学试题安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题(已下线)专题06 铁、铝及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
解题方法
4 . 下列检验溶液中的某种离子或除去杂质的操作方法正确的是
| A.向某溶液中加AgNO3溶液产生白色沉淀,证明有Cl- |
| B.向某溶液中滴加KSCN溶液,无明显现象,再滴加H2O2,溶液呈红色,说明原溶液中含有Fe2+ |
| C.除去NaCl溶液中少量的Na2CO3,可加入适量的H2SO4溶液 |
D.向某溶液中加稀盐酸酸化的BaCl2溶液产生白色沉淀,证明有 |
您最近一年使用:0次
解题方法
5 . 下列指定反应的离子方程式正确的是
A.侯氏制碱法中发生的反应: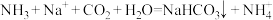 |
B.将钠加入硫酸铜溶液中: |
C.氢氧化铁与氢碘酸反应: |
D.偏铝酸钠溶液中通入过量 : :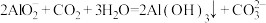 |
您最近一年使用:0次
名校
解题方法
6 . 下列离子的检验方法合理的是
| A.向某溶液中滴入KSCN溶液呈红色,说明原溶液中不含Fe2+ |
| B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+ |
| C.向某溶液中加入KSCN溶液呈红色,说明原溶液中含有Fe3+ |
| D.向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变为红褐色,说明原溶液中含有Fe2+,不含有Mg2+ |
您最近一年使用:0次
2023-06-10更新
|
143次组卷
|
3卷引用:安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题
解题方法
7 . 为迎接冬奥会王刚同学用毛笔蘸取少量30% 溶液在铜片上写上“冬奥”两个字,放置片刻,用少量水将铜片上的溶液冲到小烧杯中,下列说法中正确的是
溶液在铜片上写上“冬奥”两个字,放置片刻,用少量水将铜片上的溶液冲到小烧杯中,下列说法中正确的是
 溶液在铜片上写上“冬奥”两个字,放置片刻,用少量水将铜片上的溶液冲到小烧杯中,下列说法中正确的是
溶液在铜片上写上“冬奥”两个字,放置片刻,用少量水将铜片上的溶液冲到小烧杯中,下列说法中正确的是| A.烧杯中的溶液呈黄色 |
| B.铜片无任何变化 |
| C.铜片上有凹陷的“冬奥”字样 |
D.发生了反应: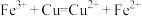 |
您最近一年使用:0次
名校
解题方法
8 . 将1.28g铜片加入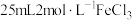 溶液中,完全反应后,下列说法正确的是
溶液中,完全反应后,下列说法正确的是
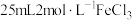 溶液中,完全反应后,下列说法正确的是
溶液中,完全反应后,下列说法正确的是A.溶液中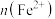 与 与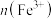 之比为2∶1 之比为2∶1 |
| B.向反应后溶液中滴加KSCN溶液无明显现象 |
C.铜片有剩余,溶液呈浅绿色, 基本不变 基本不变 |
| D.氧化产物与还原产物的物质的量之比为1∶2 |
您最近一年使用:0次
2023-01-07更新
|
123次组卷
|
3卷引用:安徽省皖南十校2022-2023学年高一上学期期末测试化学试题
名校
9 . 下列有关物质的性质与用途具有对应关系的是
A. 受热易分解,可用于治疗胃酸过多症 受热易分解,可用于治疗胃酸过多症 |
B. 溶液显酸性,可用于蚀刻铜制的电路板 溶液显酸性,可用于蚀刻铜制的电路板 |
C. 具有强氧化性,可用作自来水消毒剂 具有强氧化性,可用作自来水消毒剂 |
D. 密度比空气大,可用作镁着火时的灭火剂 密度比空气大,可用作镁着火时的灭火剂 |
您最近一年使用:0次
2023-01-07更新
|
347次组卷
|
4卷引用:安徽省皖南十校2022-2023学年高一上学期期末测试化学试题
10 . 铁是人们生活中常见的金属。掌握铁及其化合物的性质才能让其更好的为人类服务。
(1)取氯化亚铁固体,配制成0.1 mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是_______ 。
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入几滴_______ ,溶液变红,该同学认为是Cl2将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)乙同学取2 mL FeCl2溶液,向其中滴入NaOH溶液,观察到的实验现象是_______ 。
(4)高铁酸钠(Na2FeO4)是一种新型的净水剂,它的氧化性比高锰酸钾、次氯酸等还强。可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O;高铁酸钠中,铁元素的化合价是_______ ;上述制取铁酸钠的反应中,铁元素被_______ (填“还原”或“氧化”)。
(5)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: 。28g铁粉中含有的Fe原子数是
。28g铁粉中含有的Fe原子数是_______ NA,若铁粉完全反应,析出Cu单质的质量为_______ g。
(1)取氯化亚铁固体,配制成0.1 mol·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入几滴
(3)乙同学取2 mL FeCl2溶液,向其中滴入NaOH溶液,观察到的实验现象是
(4)高铁酸钠(Na2FeO4)是一种新型的净水剂,它的氧化性比高锰酸钾、次氯酸等还强。可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O;高铁酸钠中,铁元素的化合价是
(5)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:
 。28g铁粉中含有的Fe原子数是
。28g铁粉中含有的Fe原子数是
您最近一年使用:0次



