A.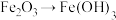 | B.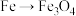 | C.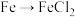 | D. |
| A.若加盐酸时有气体产生,不能证明脱氧剂未变质 |
| B.若滴加KSCN溶液,无明显变化,再滴加氯水显血红色,则证明脱氧剂未变质 |
| C.若滴加KSCN溶液,溶液显血红色,则证明脱氧剂已变质 |
| D.若加入铜粉充分反应后,溶液呈蓝色,则证明脱氧剂已变质 |
A.铝粉投入到NaOH溶液中2Al+2OH-=2 +H2O +H2O |
B.Al(OH)3溶于NaOH溶液中Al(OH)3+OH-= +2H2O +2H2O |
| C.FeCl2溶液中通入Cl2中2Fe2++Cl2=2Fe3++2Cl- |
D.Al2O3粉末溶于NaOH溶液中Al2O3+2OH—=2 +H2O +H2O |
| 物质(括号内为杂质) | 除杂试剂 | |
| A | NO (NO2) | H2O、无水CaCl2 |
| B | Cl2 (HCl) | H2O、浓H2SO4 |
| C | NaCl溶液(MgCl2) | 适量NaOH溶液、稀HCl, |
| D | FeCl2溶液(FeCl3) | Fe粉 |
| A.A | B.B | C.C | D.D |
| A.一定有Fe2+,可能有Cu2+ | B.一定有Fe2+、Cu2+,可能有Fe3+ |
| C.只有Fe2+和Cu2+ | D.只有Fe2+ |
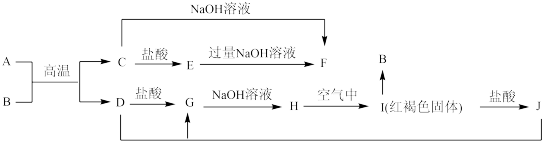
(1)C是
(2)写出J与D反应转化为G的离子方程式:
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式:
(4)写出H在空气中生成I对应方程式
(5)写出一种B的用途
| A.氯化铁溶液 | B.硫酸铜溶液 | C.氯气 | D.稀盐酸 |
8 . 某同学利用下图所示实验装置进行铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。

请回答下列问题:
Ⅰ.(1)该反应的化学方程式是
(2)该同学对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有
假设3:既有Fe也有Fe3O4。
(3)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g。从数据分析,反应后硬质试管中固体物质的组成成分为
Ⅱ.长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
A.设计实验检验FeSO4溶液的变质程度
实验方案 | 实验现象 | 实验结论 | |
步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | FeSO4溶液部分变质 | |
步骤2 | 取待检测液于试管中,向其中滴加K3[Fe(SCN)6]溶液 | ||
①将上述方案补充完整
②步骤2涉及的离子反应方程式是
③若要使变质的FeSO4复原,方法是
| A.原混合物中n(Fe2O3):n(Fe)=3:1 |
| B.无法计算原混合物的质量 |
| C.向溶液中通入0.025molCl2,可以将Fe2+完全转化为Fe3+ |
| D.收集产生的气体刚好能与0.448L的Cl2完全反应 |
| A.1.5mol | B.1.25mol |
| C.0.75mol | D.1.00mol |



