解题方法
1 . “孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近一年使用:0次
解题方法
2 . 下列除杂试剂或方法正确的是
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A |  溶液 溶液 |  | 加入过量 溶液并过滤、洗涤 溶液并过滤、洗涤再将沉淀溶于适量盐酸 |
| B | 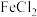 溶液 溶液 |  | 加入过量铜粉并过滤、洗涤 |
| C |  |  | 在空气中灼烧至质量不再变化 |
| D |  |  | 在空气中灼烧至质量不再变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列说法正确的是
| A.预热的铜丝能在氯气中燃烧,生成棕黄色的烟雾 |
| B.工业上用Na2O和H2O制备NaOH |
| C.可将FeCl3晶体溶于浓盐酸后稀释得到FeCl3稀溶液 |
| D.FeO在空气中受热能迅速被氧化成Fe2O3 |
您最近一年使用:0次
23-24高二上·浙江杭州·期末
4 . 类比法是一种学习化学的重要方法。 下列“类比”合理的是
| A.MgCl2溶液在空气中蒸干得到MgO固体,则SrCl2溶液在空气中蒸干得到SrO固体 |
| B.Fe3O4与盐酸反应生成Fe2+和Fe3+, 则Fe3S4也可与盐酸反应生成Fe2+和Fe3+ |
| C.CuS与O2在高温下反应生成CuO,则HgS与O2在高温下反应生成HgO |
| D.CO2是直线型分子, 则COS也是直线型分子 |
您最近一年使用:0次
23-24高一上·浙江·期末
解题方法
5 . 为探究某难溶性盐X(仅含三种常见元素)的组成,设计并完成以下实验(流程中部分物质已略去):
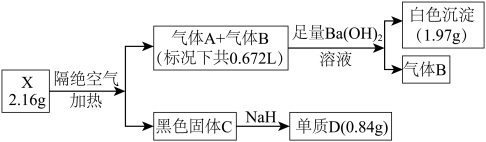
已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为_______ ,B的化学式为_______ 。
(2)X隔绝空气高温分解的化学方程式为_______ 。
(3)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式:_______ 。
(4)将产生的气体A全部被50mL0.25mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为_______ 。

已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为
(2)X隔绝空气高温分解的化学方程式为
(3)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式:
(4)将产生的气体A全部被50mL0.25mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为
您最近一年使用:0次
解题方法
6 . 工业上常用过量废铁屑与硫酸反应产生硫酸亚铁,铁屑中常含有下列杂质,其中对反应产品纯度影响不大的是
| A.油污 | B.铁锈 | C.锌 | D.硫化物 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法不正确 的是
| A.FeO在空气中加热可能得到Fe3O4固体 |
| B.结合H+和Zn2+的放电顺序,电解ZnSO4溶液不能得到Zn |
| C.早在1000多年前,古人就采用加热胆矾或绿矾的方法制取硫酸 |
D.合成氨厂利用反应CO+H2O CO2+H2制取氢气,故该条件下CO的还原性比H2强 CO2+H2制取氢气,故该条件下CO的还原性比H2强 |
您最近一年使用:0次
19-20高二·浙江·期末
8 . 硫酸亚铁( )加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物气体。下列说法正确的是
)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物气体。下列说法正确的是
 )加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物气体。下列说法正确的是
)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物气体。下列说法正确的是| A.生活中常将M与油料混合,制成油漆 |
| B.取少量M加入一定量稀盐酸中溶解,加入适量KSCN溶液,判断是否有亚铁离子存在 |
| C.若将两种非金属氧化物和氨气混合后通入到氯化钡溶液中,与直接通入氯化钡溶液中相比,沉淀量一定不变 |
D.将两种非金属氧化物气体通入到氯化钡溶液中,若产生白色沉淀,则该沉淀是 和 和 的混合 的混合 |
您最近一年使用:0次
19-20高二·浙江·期末
9 . 物质X是新型净水剂的中间体,它可以看成氯化铝(在180℃升华)和一种盐A按物质的量之比 组成。在密闭容器中加热8.75 X使之完全分解,冷却至0℃后可得到3.2 g固体氧化物B、0.448 L无色气体D(体积已折算为标准状况)、4.27 g混合物晶体E。B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色。D气体能使品红褪色。晶体E溶于水,加入盐酸酸化的
组成。在密闭容器中加热8.75 X使之完全分解,冷却至0℃后可得到3.2 g固体氧化物B、0.448 L无色气体D(体积已折算为标准状况)、4.27 g混合物晶体E。B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色。D气体能使品红褪色。晶体E溶于水,加入盐酸酸化的 溶液,有白色沉淀产生。请回答下列问题:
溶液,有白色沉淀产生。请回答下列问题:
(1)X的化学式为________ 。
(2)将A固体隔绝空气充分灼烧,使其分解,生成等物质的量的B、D和另一种化合物,则A分解的化学方程式为________ 。
(3)将E混合晶体溶于水配成溶液,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为________ 。E混合晶体中某种物质在一定条件下能和KI固体反应,写出该方程式________ 。
 组成。在密闭容器中加热8.75 X使之完全分解,冷却至0℃后可得到3.2 g固体氧化物B、0.448 L无色气体D(体积已折算为标准状况)、4.27 g混合物晶体E。B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色。D气体能使品红褪色。晶体E溶于水,加入盐酸酸化的
组成。在密闭容器中加热8.75 X使之完全分解,冷却至0℃后可得到3.2 g固体氧化物B、0.448 L无色气体D(体积已折算为标准状况)、4.27 g混合物晶体E。B溶于稀盐酸后,滴加KSCN溶液,混合液变血红色。D气体能使品红褪色。晶体E溶于水,加入盐酸酸化的 溶液,有白色沉淀产生。请回答下列问题:
溶液,有白色沉淀产生。请回答下列问题:(1)X的化学式为
(2)将A固体隔绝空气充分灼烧,使其分解,生成等物质的量的B、D和另一种化合物,则A分解的化学方程式为
(3)将E混合晶体溶于水配成溶液,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
10 . 向一定量的Fe、FeO、Fe3O4的混合物中加入200mL1mol·L-1的盐酸,恰好使混合物完全溶解,放出448mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
| A.11.2g | B.5.6g | C.2.8g | D.无法计算 |
您最近一年使用:0次



