解题方法
1 . 劳动创造美好生活。下列劳动项目所涉及的知识,其化学(离子)方程式表达错误的是
| 劳动项目 | 化学(离子)方程式 | |
| A | 用 溶液制作印刷电路板 溶液制作印刷电路板 | 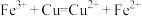 |
| B | 用稀盐酸除去铁架台上的铁锈 |  |
| C | 用葡萄酿酒 |  |
| D | 用含铝粉和 的疏通剂疏通管道 的疏通剂疏通管道 | 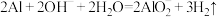 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 化学研究源于实验与理论的结合,得益于科学的推断与探究。
(1)一个体重 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是___________ 。
A. B.
B. C.
C.
②工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有___________ 性。
③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有___________ 性。
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为: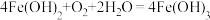 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是___________ 。
(3)某化学兴趣小组用食品脱氧剂( 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。
实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是___________ (写离子符号)。
②检验溶液丙中 的方案是
的方案是___________ 。
③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)
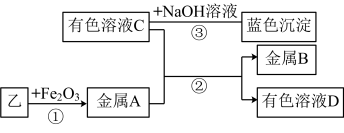
写出反应②的离子方程式___________ ,若反应消耗 金属A,转移电子的数目为
金属A,转移电子的数目为___________ 。
(1)一个体重
 的健康人含铁
的健康人含铁 ,这
,这 铁在人体中以
铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。①服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收,以下为常见铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
②工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是将人体内的
而中毒的事件,其原因是将人体内的 转化为
转化为 而失去了与
而失去了与 结合的能力,这说明
结合的能力,这说明 具有
具有③工业盐中毒后,可服用维生素C来缓解中毒症状,这说明维生素C具有
(2)常见的食品脱氧剂多为无机铁系脱氧剂,其主要成分为活性铁粉。脱氧中的一步主要反应为:
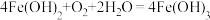 ,该脱氧反应中还原剂是
,该脱氧反应中还原剂是(3)某化学兴趣小组用食品脱氧剂(
 铁粉、
铁粉、 活性炭、
活性炭、 氯化钠)进行如图两个实验。
氯化钠)进行如图两个实验。实验Ⅰ:

请回答:
①溶液丙中一定含有的金属阳离子是
②检验溶液丙中
 的方案是
的方案是③实验Ⅱ:将乙烘干后进行如图实验,物质之间的转化关系如图(部分产物路法)

写出反应②的离子方程式
 金属A,转移电子的数目为
金属A,转移电子的数目为
您最近一年使用:0次
名校
3 . I.A、B、D、E、F是原子序数依次增大的五种短周期元素。A是元素周期表中相对原子质量最小的元素,B原子L层电子数是K层电子数的3倍。D是短周期中原子半径最大的主族元素,E的周期序数和族序数相等,D、F的原子最外层电子数之和为8。
(1)则A为___________ ,B为___________ ,E为___________ ,F为___________ (填元素符号)
Ⅱ工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(2)写出反应①的化学方程式___________ 。
(3)反应①后过滤的沉淀为___________ ,简述确定此物质中金属元素及其价态的操作过程___________ 。
(1)则A为
Ⅱ工业上用铝土矿(主要成分为Al2O3,只含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

回答下列问题:
(2)写出反应①的化学方程式
(3)反应①后过滤的沉淀为
您最近一年使用:0次
名校
4 . 某化学小组围绕 开展主题学习。
开展主题学习。
Ⅰ.分类和性质
(1)墨粉中含有 (可表示为
(可表示为 ),
),
___________ (填“是”或“不是”)碱性氧化物,原因为___________ (用化学反应方程式说明)。
Ⅱ.制备
方法一:

方法二:

(2)方法二中A的化学式是___________ ,操作Ⅰ和操作Ⅱ相同,为___________ 。
(3)与方法二比较,方法一的不足之处有___________ (答1点即可)。
(4)氢氧化氧铁(FeOOH)中铁元素的化合价是___________ ,当A溶液①和A溶液②的质量之比为___________ 时,铁元素全部转化到 中。
中。
Ⅲ.应用
(5)纳米高性能 (平均直径为
(平均直径为 )可以实现高效催化分解水,其反应历程如下图所示。
)可以实现高效催化分解水,其反应历程如下图所示。

①该过程中的能量转化形式为___________ 转化为化学能,在加热的条件下反应b的化学方程式为___________ 。
②纳米高性能 均匀分散在水中,具有丁达尔现象,请设计实验方案证明
均匀分散在水中,具有丁达尔现象,请设计实验方案证明___________ 。
 开展主题学习。
开展主题学习。Ⅰ.分类和性质
(1)墨粉中含有
 (可表示为
(可表示为 ),
),
Ⅱ.制备
方法一:

方法二:

(2)方法二中A的化学式是
(3)与方法二比较,方法一的不足之处有
(4)氢氧化氧铁(FeOOH)中铁元素的化合价是
 中。
中。Ⅲ.应用
(5)纳米高性能
 (平均直径为
(平均直径为 )可以实现高效催化分解水,其反应历程如下图所示。
)可以实现高效催化分解水,其反应历程如下图所示。
①该过程中的能量转化形式为
②纳米高性能
 均匀分散在水中,具有丁达尔现象,请设计实验方案证明
均匀分散在水中,具有丁达尔现象,请设计实验方案证明
您最近一年使用:0次
名校
解题方法
5 . 中科院网报道,纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和作为药物载体用于疾病的治疗。其制备过程如下,下列叙述合理的是
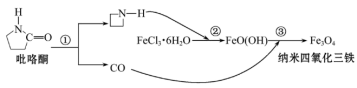

| A.Fe3O4可以表示为FeO·Fe2O3,属于混合物 |
B.在反应②中FeCl3·6H2O被环丙胺(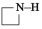 )还原为FeO(OH) )还原为FeO(OH) |
| C.纳米四氧化三铁材料为胶体 |
| D.反应③的化学方程式是6FeO(OH)+CO=2Fe3O4+3H2O+CO2 |
您最近一年使用:0次
名校
解题方法
6 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价一类”二维图。下图是铁元素的“价一类”二维图,下列说法正确的是


A.常温下Fe与水反应生成 |
B.工业上用CO还原 炼铁,该反应不属于置换反应 炼铁,该反应不属于置换反应 |
C.维生素C能将 转化为 转化为 ,过程中维生素C作还原剂 ,过程中维生素C作还原剂 |
D. 浊液露置于空气中,白色迅速转变为红褐色 浊液露置于空气中,白色迅速转变为红褐色 |
您最近一年使用:0次
2022-12-12更新
|
216次组卷
|
7卷引用:福建省莆田第二十四中学2021-2022学年高一下学期开学摸底考试化学(2卷)试题
福建省莆田第二十四中学2021-2022学年高一下学期开学摸底考试化学(2卷)试题江苏省海安市2020-2021学年高一上学期期末考试化学试题(已下线)《新教材变化解读及考法剖析 》(人教版2019必修第一册)第三章(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)江苏省海安市实验中学2021-2022高一上学期第二次学情检测化学试题江苏省南京市第五高级中学2022-2023学年高一上学期学情自测卷化学试题(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
7 . 某铁矿石的有效成分是Fe2O3,用如图所示装置测该铁矿石有效成分的含量(杂质不参与反应),称取2.00g铁矿石于硬质玻璃管A中,充分反应后测得干燥管B增重1.32g,C增重0.10g,下列相关说法中错误的是


| A.应先通一段时间CO,称量干燥管B后,再加热硬质玻璃管A |
| B.干燥管C的作用是防止空气中的水蒸气和CO2进入干燥管B |
| C.在硬质玻璃管A中发生的反应中,Fe2O3为氧化剂 |
| D.铁矿石有效成分的质量分数为86.0% |
您最近一年使用:0次
2022-10-01更新
|
378次组卷
|
2卷引用:福建省厦门双十中学2022-2023学年高一上学期第二次月考化学试题
名校
解题方法
8 . 铁黄(FeOOH)是重要的化工产品。某科研小组在实验室进行铁黄制备研究。
已知:①铁黄制备原理4FeSO4+O2+6H2O 4FeOOH↓+4H2SO4。
4FeOOH↓+4H2SO4。
②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)FeOOH可表示为xFe2O3•yH2O,其中 =
=____ 。
(2)铁皮处理:取一定量铁皮,用稀硫酸除去表面铁锈。该除锈反应的化学方程式为_____ 。
(3)制备铁黄:在如图所示装置的三颈烧瓶内进行制备。

步骤一:加入一定量除锈后的碎铁皮
步骤二:加入含有少量铁黄晶种的悬浊液;
步骤三:滴加少量FeSO4溶液;
步骤四:控制合适条件,边搅拌边鼓入空气,充分反应48小时,得到大量FeOOH沉淀。
①将三颈烧瓶中所得FeOOH沉淀分离出来的实验操作是____ (填操作名称)。
②为提高产品纯度,需洗涤分离出的沉淀。洗涤前沉淀表面吸附的阴离子为____ (填离子符号)。
③实验中仅滴加少量 FeSO4溶液,就能得到大量 FeOOH沉淀,其原因是____ 。
已知:①铁黄制备原理4FeSO4+O2+6H2O
 4FeOOH↓+4H2SO4。
4FeOOH↓+4H2SO4。②为促进生成的铁黄沉淀有序生长,实验时需加入少量已制铁黄作为晶种。
(1)FeOOH可表示为xFe2O3•yH2O,其中
 =
=(2)铁皮处理:取一定量铁皮,用稀硫酸除去表面铁锈。该除锈反应的化学方程式为
(3)制备铁黄:在如图所示装置的三颈烧瓶内进行制备。

步骤一:加入一定量除锈后的碎铁皮
步骤二:加入含有少量铁黄晶种的悬浊液;
步骤三:滴加少量FeSO4溶液;
步骤四:控制合适条件,边搅拌边鼓入空气,充分反应48小时,得到大量FeOOH沉淀。
①将三颈烧瓶中所得FeOOH沉淀分离出来的实验操作是
②为提高产品纯度,需洗涤分离出的沉淀。洗涤前沉淀表面吸附的阴离子为
③实验中仅滴加
您最近一年使用:0次
名校
解题方法
9 . 钢铁是应用广泛的金属材料。
(1)英国学者R•坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用铁矿石与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为____ 。
②古法炼铁的原理包含一氧化碳与氧化铁在高温下反应,反应的化学方程式是____ 。
③生铁和钢是两种含碳量____ 的铁合金(填“相同”或“不同”)。
(2)铁锈成分中含有氧化铁(Fe2O3),写出氧化铁与稀硫酸反应的化学方程式____ 。
(1)英国学者R•坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用铁矿石与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为
②古法炼铁的原理包含一氧化碳与氧化铁在高温下反应,反应的化学方程式是
③生铁和钢是两种含碳量
(2)铁锈成分中含有氧化铁(Fe2O3),写出氧化铁与稀硫酸反应的化学方程式
您最近一年使用:0次
名校
10 . 图为铁及其化合物的“价—类”二维图。利用如图可以从不同角度研究含铁物质的性质及其转化关系。下列分析结果不正确的是


A.二维图缺失的类别①应填“单质”,化学式②应填“ ” ” |
B.从物质类别分析, 属于碱性氧化物,可以与稀HCl反应 属于碱性氧化物,可以与稀HCl反应 |
C.从化合价角度分析, 具有还原性,可以使酸性高锰酸钾溶液褪色 具有还原性,可以使酸性高锰酸钾溶液褪色 |
D.从物质转化角度分析, 和 和 都可以通过一步反应直接转化成② 都可以通过一步反应直接转化成② |
您最近一年使用:0次
2022-03-30更新
|
397次组卷
|
6卷引用:福建省泉州第一中学2021-2022学年高一下学期期中考试化学试题



