名校
1 . 某化学兴趣小组同学为探究化合物 的稳定性进行如下操作:
的稳定性进行如下操作:

下列分析正确的是
 的稳定性进行如下操作:
的稳定性进行如下操作:
下列分析正确的是
| A.气体a是二氧化碳 | B.固体c是四氧化三铁 |
| C.白色沉淀的质量为2.00g | D.d中滴加 褪色,d中存在 褪色,d中存在 |
您最近一年使用:0次
2023-11-16更新
|
614次组卷
|
3卷引用:湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题
名校
解题方法
2 . 汽车安全气囊是行车安全的重要保障。当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放大量的氮气形成气囊,从而保护司机及乘客免受伤害。为研究安全气囊工作的化学原理,取安全装置中的固体粉末进行实验。经组成分析,确定该粉末仅含Na、Fe、N、O四种元素。水溶性实验表明,固体粉末部分溶解。经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸。取13.0g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72L。单质乙在高温、隔绝空气的条件下与红棕色不溶物粉末反应,生成氧化物丙和另一种单质。化合物丙与空气接触可转化为可溶性盐。请回答下列问题:
(1)甲的化学式为_______ ;丙的电子式为_______ 。
(2)单质乙与红棕色粉末发生反应的化学方程式为_______ ;安全气囊中红棕色粉末的作用是_______ 。
(3)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是_______ (填字母代号)。
(4)可溶性盐的成分可能是_______ ;请设计一个可行的简单实验方案,探究化合物丙与空气接触后生成可溶性盐的成分(不考虑结晶水合物),请简单叙述你的实验方案、原理:_______ 。
(1)甲的化学式为
(2)单质乙与红棕色粉末发生反应的化学方程式为
(3)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是_______ (填字母代号)。
| A.KCl | B.KNO3 | C.Na2S | D.CuO |
您最近一年使用:0次
3 . 下列离子方程式正确的是
A.钠与水反应: |
| B.Fe2O3溶于过量的氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O |
C.向 溶液中滴加 溶液中滴加 溶液至中性: 溶液至中性: |
D.Fe与稀硝酸反应,当 时, 时, |
您最近一年使用:0次
2023-01-10更新
|
325次组卷
|
2卷引用:湖南省怀化市2022-2023学年高三下学期期末考试化学试题
4 . 某磁铁矿石A的主要成分是磁性氧化铁( ),还含少量的
),还含少量的 、
、 。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知
。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知 不溶于水和碱,但溶于酸:
不溶于水和碱,但溶于酸: )。根据流程回答下列问题:
)。根据流程回答下列问题:

(1)溶液C的主要成分是___________ 。
(2)溶液D中的金属阳离子与过量试剂X反应的离子方程式是___________ 。
(3)在溶液F中滴加 溶液的现象是
溶液的现象是___________ ;发生的化学反应方程式为___________ 。
(4)聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分 ,含少量碳及二氧化硅)为原料制备的流程如图:
,含少量碳及二氧化硅)为原料制备的流程如图:

①加热条件下酸浸时, 与硫酸反应。酸浸时,通入
与硫酸反应。酸浸时,通入 的目的是
的目的是___________ 。
②“ 浓度检测”是先将100mL含
浓度检测”是先将100mL含 溶液用适量的
溶液用适量的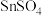 还原为
还原为 ;再用酸性
;再用酸性 标准溶液测定
标准溶液测定 的量(
的量( 被还原为
被还原为 ),此时发生反应的离子方程式为:
),此时发生反应的离子方程式为:___________ 。若用掉
 溶液50mL,则
溶液50mL,则 的物质的量浓度为
的物质的量浓度为___________ 。
 ),还含少量的
),还含少量的 、
、 。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知
。某工厂利用此矿石进行有关物质的回收利用,工艺流程如下:(已知 不溶于水和碱,但溶于酸:
不溶于水和碱,但溶于酸: )。根据流程回答下列问题:
)。根据流程回答下列问题:
(1)溶液C的主要成分是
(2)溶液D中的金属阳离子与过量试剂X反应的离子方程式是
(3)在溶液F中滴加
 溶液的现象是
溶液的现象是(4)聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分
 ,含少量碳及二氧化硅)为原料制备的流程如图:
,含少量碳及二氧化硅)为原料制备的流程如图:
①加热条件下酸浸时,
 与硫酸反应。酸浸时,通入
与硫酸反应。酸浸时,通入 的目的是
的目的是②“
 浓度检测”是先将100mL含
浓度检测”是先将100mL含 溶液用适量的
溶液用适量的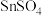 还原为
还原为 ;再用酸性
;再用酸性 标准溶液测定
标准溶液测定 的量(
的量( 被还原为
被还原为 ),此时发生反应的离子方程式为:
),此时发生反应的离子方程式为:
 溶液50mL,则
溶液50mL,则 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
2022-01-26更新
|
1128次组卷
|
4卷引用:湖南长沙麓山国际实验中学2022-2023学年高一上学期期末线上化学试题



