1 . 称取6.00g氧化铜和氧化铁固体混合物,加入75.0mL2.00mol/L的硫酸充分溶解,往所得溶液中加入8.40g铁粉,充分反应后,得固体的质量为4.56g。请计算:
(1)加入的铁粉的物质的量为___________ mol。
(2)加入铁粉充分反应后,溶液中溶质为___________ ,其物质的量浓度为___________ mol/L(不考虑体积变化)。
(3)固体混合物中氧化铜的质量百分比为___________ 。
(1)加入的铁粉的物质的量为
(2)加入铁粉充分反应后,溶液中溶质为
(3)固体混合物中氧化铜的质量百分比为
您最近一年使用:0次
解题方法
2 . 为了探究固体化合物X(仅含两种元素)的组成和性质,设计并完成如下实验(已知化合物A的摩尔质量:200g/mol<M<300g/mol):

请回答:
(1)白色沉淀E的化学式是_____ 。
(2)固体X中的元素是_____ 。(填元素符号)
(3)固体X在空气中煅烧生成化合物A和气体D的化学方程式_____ 。
(4)往溶液B通入适量氯气的离子方程式是_____ 。

请回答:
(1)白色沉淀E的化学式是
(2)固体X中的元素是
(3)固体X在空气中煅烧生成化合物A和气体D的化学方程式
(4)往溶液B通入适量氯气的离子方程式是
您最近一年使用:0次
23-24高一上·浙江·期末
解题方法
3 . 为探究某难溶性盐X(仅含三种常见元素)的组成,设计并完成以下实验(流程中部分物质已略去):
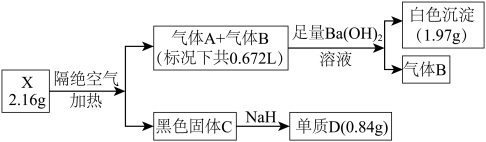
已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为_______ ,B的化学式为_______ 。
(2)X隔绝空气高温分解的化学方程式为_______ 。
(3)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式:_______ 。
(4)将产生的气体A全部被50mL0.25mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为_______ 。

已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为
(2)X隔绝空气高温分解的化学方程式为
(3)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式:
(4)将产生的气体A全部被50mL0.25mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为
您最近一年使用:0次
4 . 确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别加入30.0 mL某浓度的稀硫酸中,充分反应后, 每组样品剩余固体的质量与原样品质量的关系如图所示。

(1)该混合物中,n(Fe2O3):n(Cu)=___________ 。
(2)稀硫酸的物质的量浓度为___________ 。

(1)该混合物中,n(Fe2O3):n(Cu)=
(2)稀硫酸的物质的量浓度为
您最近一年使用:0次
2021-05-29更新
|
962次组卷
|
5卷引用:【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)
【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)(已下线)【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00147】浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题浙江省舟山市舟山中学2022-2023学年高一上学期12月质量检测化学试题(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题
解题方法
5 . 已知X为 和CuO的混合物,且知氧化性顺序:
和CuO的混合物,且知氧化性顺序: 。取等质量的两份X样品进行如图所示的实验:
。取等质量的两份X样品进行如图所示的实验:
(1)若溶液D中只有一种金属离子,则一定是___________ ;若C固体是纯净物,该固体是___________ 。
(2)印刷电路板是由高分子材料和铜箔复合而成,可用A溶液作“腐蚀剂"刻制印刷电路的离子反应方程式为___________ 。
(3)若溶液D中只有一种金属离子,步骤③所得固体C是纯净物,质量为12.8g,无色气体E在标准状况下的体积为2.24L。则每份X样品中 的质量为
的质量为___________ 。
 和CuO的混合物,且知氧化性顺序:
和CuO的混合物,且知氧化性顺序: 。取等质量的两份X样品进行如图所示的实验:
。取等质量的两份X样品进行如图所示的实验:
(1)若溶液D中只有一种金属离子,则一定是
(2)印刷电路板是由高分子材料和铜箔复合而成,可用A溶液作“腐蚀剂"刻制印刷电路的离子反应方程式为
(3)若溶液D中只有一种金属离子,步骤③所得固体C是纯净物,质量为12.8g,无色气体E在标准状况下的体积为2.24L。则每份X样品中
 的质量为
的质量为
您最近一年使用:0次
名校
解题方法
6 . 为探究某难溶性盐X(仅含三种常见元素)的组成,设计并完成以下实验(流程中部分物质已略去):

已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为________________ 。
(2)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式___________________ 。
(3)将产生的气体A全部被100 mL 0.35 mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为____________________ 。

已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为
(2)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式
(3)将产生的气体A全部被100 mL 0.35 mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为
您最近一年使用:0次
2020-01-16更新
|
436次组卷
|
4卷引用:浙江省宁波市九校2019-2020学年高一上学期期末联考化学试题
浙江省宁波市九校2019-2020学年高一上学期期末联考化学试题(已下线)【新东方】2020-88(已下线)【新东方】2020-96浙江省宁波市镇海中学2023-2024学年高一上学期化学期末复习提分卷
解题方法
7 . 粉末状试样A是由等物质的量的CaO和Fe2O3组成的混合物,进行如下实验:
①取适量A与铝进行铝热反应,产物中有单质B生成。
②另取21.6gA全部溶于0.20L、6.0mol/L盐酸中,得溶液C。
③将①中得到的单质B和②中的溶液C反应放出4.48L(标准状况)气体,同时生成溶液D,还残留有固体物质B。
④用KSCN溶液检验时,溶液D不变色。
(1)①中生成的单质B是_________ 。
(2)③中所发生的各反应的离子方程式是______________ ,_____________ 。
(3)若溶液D的体积仍视为0.20L,则该溶液中c(Ca2+)为_______ ,c(Fe2+)为_______ 。
①取适量A与铝进行铝热反应,产物中有单质B生成。
②另取21.6gA全部溶于0.20L、6.0mol/L盐酸中,得溶液C。
③将①中得到的单质B和②中的溶液C反应放出4.48L(标准状况)气体,同时生成溶液D,还残留有固体物质B。
④用KSCN溶液检验时,溶液D不变色。
(1)①中生成的单质B是
(2)③中所发生的各反应的离子方程式是
(3)若溶液D的体积仍视为0.20L,则该溶液中c(Ca2+)为
您最近一年使用:0次
解题方法
8 . (Ⅰ)浓硝酸与浓盐酸混合过程中会产生少量的黄绿色气体单质X、化合物M和无色液体,化合物M中所有原子均达到8电子的稳定结构。2mol M加热分解生成1mol氧化产物X和2mol无色气体Y,Y遇到空气呈现红棕色。
(1)镁与气体X反应产物的电子式_______ 。
(2)浓硝酸与浓盐酸反应的化学方程式为_______ 。
(3)化合物M水解生成两种酸,为非氧化还原反应,该反应的化学方程式为_______ 。
(Ⅱ)石油铁储罐久置未清洗易引发火灾,经分析研究,事故是由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1︰3反应生成的物质丙自燃引起的。某研究小组将一定量的丙粉末投入足量的浓盐酸中发生反应,得到4.8g淡黄色固体和气体乙,乙在标准状况下的密度为1.52g·L-1.过滤后向滤液(假设乙全部逸出)中加入足量的NaOH溶液,先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24g。已知气体乙可溶于水。请回答下列问题:
(4)甲的化学式为_______ 。
(5)丙在盐酸中反应的化学方程式为_______ 。
(6)丙与盐酸反应后的滤液暴露在空气中一段时间颜色加深,其原因是(用离子方程式表示)_______ 。
(7)为消除石油铁储罐的火灾隐患,下列措施可行的是(填编号)_______ 。
A.石油入罐前脱硫
B.定期用酸清洗罐体
C.罐体内壁涂刷油漆
D.罐体中充入氮气
(1)镁与气体X反应产物的电子式
(2)浓硝酸与浓盐酸反应的化学方程式为
(3)化合物M水解生成两种酸,为非氧化还原反应,该反应的化学方程式为
(Ⅱ)石油铁储罐久置未清洗易引发火灾,经分析研究,事故是由罐体内壁附着的氧化物甲与溶于石油中的气态氢化物乙按1︰3反应生成的物质丙自燃引起的。某研究小组将一定量的丙粉末投入足量的浓盐酸中发生反应,得到4.8g淡黄色固体和气体乙,乙在标准状况下的密度为1.52g·L-1.过滤后向滤液(假设乙全部逸出)中加入足量的NaOH溶液,先出现白色沉淀,最终转变为红褐色沉淀,过滤、洗涤、灼烧后的固体质量为24g。已知气体乙可溶于水。请回答下列问题:
(4)甲的化学式为
(5)丙在盐酸中反应的化学方程式为
(6)丙与盐酸反应后的滤液暴露在空气中一段时间颜色加深,其原因是(用离子方程式表示)
(7)为消除石油铁储罐的火灾隐患,下列措施可行的是(填编号)
A.石油入罐前脱硫
B.定期用酸清洗罐体
C.罐体内壁涂刷油漆
D.罐体中充入氮气
您最近一年使用:0次



