解题方法
1 . 有关铁的氧化物的说法中,不正确 的是
| A.赤铁矿主要成分是Fe2O3,Fe2O3是红棕色的,常用作红色油漆和涂料 |
B.Fe3O4是黑色晶体,其中 的铁显+2价, 的铁显+2价, 的铁显+3价 的铁显+3价 |
| C.FeO、Fe2O3都不溶于水,但都能和盐酸反应生成相应的盐 |
| D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3 |
您最近一年使用:0次
解题方法
2 . 下列物质性质与用途对应关系正确的是
| A.“84”消毒液具有强氧化性,能用于饮用水杀菌消毒 |
| B.硬铝密度小、强度高,具有较强的抗腐蚀能力,常用于制造飞机外壳 |
| C.碳酸钠的溶液显碱性,医疗上可用作中和胃酸 |
D.用盐酸除铁锈,是因为 溶于水后,其溶液显碱性 溶于水后,其溶液显碱性 |
您最近一年使用:0次
3 . 类比是研究物质性质的常用方法之一。下列说法正确的是
A.Cu与 能化合生成 能化合生成 ,推测Fe与 ,推测Fe与 也能化合生成 也能化合生成 |
| B.碳酸氢钠可以治疗胃酸过多,推测碳酸钠也可以治疗胃酸过多 |
C.Fe可以置换出 溶液中的铜,推测Na也可以置换出 溶液中的铜,推测Na也可以置换出 溶液中的铜 溶液中的铜 |
D.CuO是碱性氧化物可以和酸反应生成盐和水,推测 也可以和酸反应生成盐和水 也可以和酸反应生成盐和水 |
您最近一年使用:0次
解题方法
4 . I.铝灰的回收利用方法很多,现用含有 、
、 和少量
和少量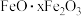 的铝灰制备
的铝灰制备 ,工艺流程如图:
,工艺流程如图:

已知步骤③中所得溶液生成氢氧化物沉淀的pH如表所示:
(1)步骤③中加入高锰酸钾溶液的作用是_______ 。
(2)在该浓度下除去铁的化合物,调节pH的范围为_______ 。
(3)调控步骤③中调pH时最佳试剂为_______ 。
II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg•L-1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10-12,Ksp(CdS)=8.0×10-27;回答下列问题:
(4)向某含镉废水中加入Na2S,当S2-浓度达到8.0×10-8mol∙L-1时废水中Cd2+的浓度为_______ 。
(5)室温下,反应CdCO3(s)+S2-(aq) CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=_______ (结果保留两位有效数字)
 、
、 和少量
和少量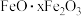 的铝灰制备
的铝灰制备 ,工艺流程如图:
,工艺流程如图:
已知步骤③中所得溶液生成氢氧化物沉淀的pH如表所示:
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时的pH | 3.4 | 6.3 | 1.5 |
| 完全沉淀时的pH | 4.7 | 8.3 | 2.8 |
(2)在该浓度下除去铁的化合物,调节pH的范围为
(3)调控步骤③中调pH时最佳试剂为
II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg•L-1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10-12,Ksp(CdS)=8.0×10-27;回答下列问题:
(4)向某含镉废水中加入Na2S,当S2-浓度达到8.0×10-8mol∙L-1时废水中Cd2+的浓度为
(5)室温下,反应CdCO3(s)+S2-(aq)
 CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=
您最近一年使用:0次
5 . 利用“价类二维图”可以从不同角度研究含铁物质的性质及其转化关系,图中甲~戊均含铁元素。回答下列问题:
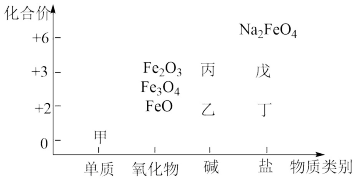
(1)Na2FeO4是一种新型饮用水消毒剂。工业上常用NaClO、Fe(NO3)3、NaOH制备:3ClO-+2Fe3++10OH-=2
 +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为(2)打印机使用的墨粉中含有Fe3O4,下列关于Fe3O4的说法正确的是 (填标号)。
| A.有磁性,是FeO与Fe2O3的混合物 |
| B.属于两性氧化物,与酸、碱都能反应 |
| C.Fe3O4与稀盐酸反应生成Fe2+与Fe3+物质的量之比为1:2 |
| D.Fe与水蒸气在高温下反应能生成Fe3O4 |
您最近一年使用:0次
解题方法
6 . “孤蓬自振”学习小组向一定质量的Fe、FeO、Fe2O3的混合物中,加入100mL1.0mol/L的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中滴加几滴KSCN溶液,溶液未显红色。请回答:
(1)加盐酸后所得溶液的溶质是______ (填化学式),物质的量浓度是______ mol/L。
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是______ g。
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=______ 。
(1)加盐酸后所得溶液的溶质是
(2)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量是
(3)该混合物中铁、氧两种元素的粒子个数比N(Fe):N(O)=
您最近一年使用:0次
解题方法
7 . 下列除杂试剂或方法正确的是
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A |  溶液 溶液 |  | 加入过量 溶液并过滤、洗涤 溶液并过滤、洗涤再将沉淀溶于适量盐酸 |
| B | 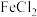 溶液 溶液 |  | 加入过量铜粉并过滤、洗涤 |
| C |  |  | 在空气中灼烧至质量不再变化 |
| D |  |  | 在空气中灼烧至质量不再变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下列离子方程式中正确的是
| A.铁与稀硫酸制氢气: 2Fe+6H+=2Fe3+ +3H2↑ |
B.用大理石和稀盐酸制备二氧化碳: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| C.金属Na投入MgCl2溶液中:2Na+Mg2+=2Na++Mg |
| D.Fe2O3和稀盐酸反应:Fe2O3+6H+=2Fe3++3H2O |
您最近一年使用:0次
名校
9 . 完成下列问题。
(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的化学方程式:_______ ;常用澄清石灰水检验CO2气体的离子方程式是_______ 。
(2)将表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的化学方程式是_______ ;反应片刻后,可观察到有气体产生,其离子方程式是_______ 。
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为_______ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为_______ 。
(4)钠与水反应的化学方程式:_______ 。
(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的化学方程式:
(2)将表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的化学方程式是
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
(4)钠与水反应的化学方程式:
您最近一年使用:0次
名校
解题方法
10 . 以化合价为纵坐标,物质类别为横坐标的图像称为价类二维图,在地壳中的含量仅次于铝,居第四位的元素价类二维图如图所示,下列说法错误的是
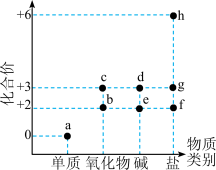

A.制备、观察 需要隔绝空气 需要隔绝空气 | B.b和 可分别与水发生反应生成 可分别与水发生反应生成 和 和 |
C.e在潮湿的空气中容易转变为 | D. 的某种盐是具备净水和消毒双重功能的水处理剂 的某种盐是具备净水和消毒双重功能的水处理剂 |
您最近一年使用:0次



