题号 | 题型 | 分值 | 能力层次 | 知识点 | |
1 | 单选 | 2 | 了解 | 常见 | |
2 | 单选 | 2 | 了解 | 化学符号及名称的综合 | |
3 | 单选 | 2 | 了解 | 物质的性质与用途 | |
4 | 单选 | 2 | 了解 | 离子共存 | |
5 | 单选 | 2 | 了解 | 化学实验方案的评价 | |
6 | 单选 | 2 | 了解 | 离子方程式的书写判断 | |
7 | 单选 | 2 | 理解 | 常见元素单质及其化合物的综合应用 | |
8 | 单选 | 2 | 理解 | 元素周期律 | |
9 | 单选 | 2 | 理解 | 物质间的转化 | |
10 | 单选 | 2 | 理解 | 化学反应中的能量变化、化学反应速率、反应限度、弱电解质的电离 | |
11 | 不定项 | 4 | 理解 | 燃料电池 | |
12 | 不定项 | 4 | 理解 | 有机化学 | |
13 | 不定项 | 4 | 理解 | 实验原理和操作 | |
14 | 不定项 | 4 | 综合运用 | 弱电解质的电离平衡、水解平衡 | |
15 | 不定项 | 4 | 综合运用 | 化学平衡 | |
16 | 16-1 | 填空 | 2 | 了解 | 工业流程条件控制 |
16-2 | 填空 | 2 | 理解 | 实验操作分析 | |
16-3 | 填空 | 2 | 综合运用 | 离子方程式书写 | |
16-4 | 填空 | 2 | 理解 | 图像分析 | |
16-5 | 填空 | 2 | 理解 | 产物分析 | |
16-6 | 填空 | 2 | 理解 | 化学方程式书写 | |
17 | 17-1 | 填空 | 2 | 了解 | 常见有机化合物的官能团 |
17-2 | 填空 | 2 | 了解 | 判断有机反应类型 | |
17-3 | 填空 | 3 | 理解 | 同分异构体的书写 | |
17-4 | 填空 | 3 | 综合运用 | 有机物的结构推断 | |
17-5 | 填空 | 5 | 综合运用 | 设计合理路线合成简单有机物 | |
18 | 18-1-1 | 填空 | 2 | 综合运用 | Ksp计算 |
18-1-2 | 填空 | 2 | 理解 | 平衡常数计算 | |
18-2-1 | 填空 | 2 | 理解 | 滴定过程的误差分析 | |
18-2-2 | 填空 | 6 | 综合运用 | 化学计算 | |
19 | 19-1 | 填空 | 2 | 理解 | 加热方式的选择 |
19-2 | 填空 | 2 | 理解 | 实验分析 | |
19-3-1 | 填空 | 2 | 理解 | 化学方程式书写 | |
19-3-2 | 填空 | 2 | 了解 | 容器名称 | |
19-4 | 填空 | 2 | 综合运用 | 实验条件控制 | |
19-5 | 填空 | 5 | 综合运用 | 运用实验原理设计实验方案 | |
20 | 20-I-1 | 填空 | 2 | 理解 | 图像分析,论据推理 |
20-I-2 | 填空 | 2 | 理解 | 根据方程式计算 | |
20-Ⅱ-1-1-1 | 填空 | 2 | 理解 | 物质稳定性分析 | |
20-Ⅱ-1-1-2 | 填空 | 2 | 综合运用 | 离子的判断 | |
20-Ⅱ-1-2 | 填空 | 2 | 综合运用 | pH计算 | |
20-Ⅱ-2-1 | 填空 | 2 | 综合运用 | 离子方程式书写 | |
20-Ⅱ-2-2 | 填空 | 2 | 综合运用 | 根据图像论据推理 | |
21A | 21-1 | 填空 | 2 | 理解 | 电子排布式的书写 |
21-2 | 填空 | 2 | 理解 | 空间构型判断 | |
21-3 | 填空 | 2 | 理解 | 杂化方式判断 | |
21-4 | 填空 | 2 | 理解 | 键型数目比较 | |
21-5 | 填空 | 2 | 理解 | 电负性大小比较 | |
21-6 | 填空 | 2 | 理解 | 方程式书写 | |
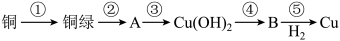
(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)请写出铜绿与盐酸反应的离子方程式:
(3)上述转化过程中属于氧化还原反应的是
(4)铜绿在受热时可直接分解生成物质B、CO2和水,其分解的化学方程式为
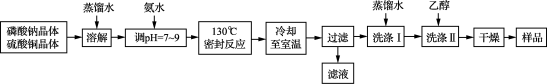
主要反应原理:2Na3PO4+4CuSO4+2NH3·H2O===Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1) 实验室进行“过滤”操作使用的玻璃仪器主要有
(2) 流程中“洗涤Ⅰ”后,检验沉淀已洗涤干净的方法是
(3) 准确称取上述流程所得的样品38.56 g [假定样品中只含Cu4O(PO4)2和CuO两种物质],使其完全溶于一定量的硝酸中,再加入氢氧化钠溶液,使铜完全沉淀,将沉淀灼烧使其转变为黑色氧化铜,最终称得残留固体质量为27.20 g。计算所得样品中磷酸氧铜的质量分数
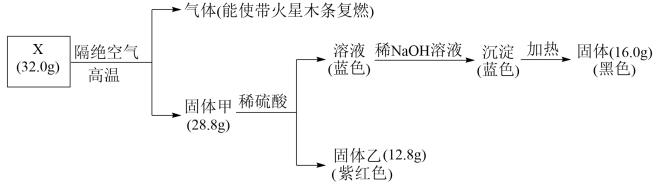
请回答:
(1)X的化学式是
(2)固体甲与稀硫酸反应的离子方程式是
(3)加热条件下氨气被固体X氧化成一种气体单质,写出该反应的化学方程式

根据题意完成下列填空:
(1)向含有铜粉的稀硫酸中滴加硝酸,在铜粉溶解时最终可以观察到的实验现象:
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是
(3)将CuSO4·5H2O与NaHCO3按一定的比例共同投入到150mL沸水中,剧烈搅拌,冷却后,有绿色晶体析出。该晶体的化学组成为Cux (OH) y (CO3) z·nH2O。实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是
(4)为了确定晶体的化学式,某实验小组进行如下实验:a.称取3.640g晶体,加入足量的稀盐酸使固体完全溶解,收集到标准状况下的气体448.0 mL;b.称取等质量的晶体,灼烧至完全分解,得到2.400g残余固体。通过计算确定晶体的化学式(写出计算过程)。
试回答下列问题:
(1)细菌把硫化铜氧化为硫酸铜的过程中起了什么作用:
(2)从硫酸铜溶液中提取铜,简便而经济的方法是
(3)普通生产铜的方法是在空气中燃烧硫化铜(产物中有一种气态氧化物)。试比较两种方法的优缺点。



