解题方法
1 . 下列反应的离子方程式书写正确的是
A.碳酸钙与稀盐酸反应: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| B.金属钠加入硫酸铜溶液的反应中:2Na+CuSO4=Na2SO4+Cu |
| C.铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
| D.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
您最近一年使用:0次
2 . 胆矾(CuSO4·5H2O)是一种重要化工原料。某研究小组以生锈的铜屑为原料(主要成分是Cu,含有少量的油污、CuO、CuCO3、Cu(OH)2)制备胆矾流程如图,下列说法不正确的是
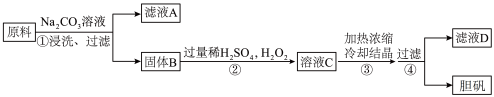

| A.步骤②中包含了氧化还原反应,氧化剂与还原剂的物质的量比为1∶1 |
| B.步骤③④得到的胆矾晶体,可以用水进行洗涤干燥 |
| C.往滤液D中加入淀粉-KI溶液,无明显现象 |
| D.将25g胆矾晶体与75g水混合,配制得到质量分数为16%的硫酸铜溶液 |
您最近一年使用:0次
3 . 某废旧金属材料中主要为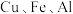 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾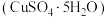 的一种流程如下:
的一种流程如下: 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。
回答下列问题:
(1)“破碎”的目的是___________ 。
(2)“碱浸”时发生反应的离子方程式为___________ 。
(3)“酸浸、氧化”的温度不宜过高,原因是___________ ;“滤渣2”的主要成分是___________ (填化学式)。
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有 的是___________。
的是___________。
(5)测定产品的纯度:准确称取胆矾样品 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为___________ (保留3位有效数字)。
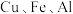 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾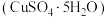 的一种流程如下:
的一种流程如下: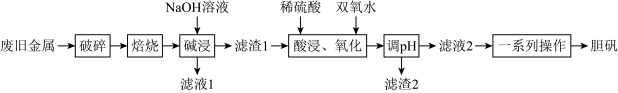
 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。回答下列问题:
(1)“破碎”的目的是
(2)“碱浸”时发生反应的离子方程式为
(3)“酸浸、氧化”的温度不宜过高,原因是
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有
 的是___________。
的是___________。A. 溶液,新制氯水 溶液,新制氯水 | B.酸性高锰酸钾溶液 |
C. 溶液 溶液 | D.淀粉 试纸 试纸 |
(5)测定产品的纯度:准确称取胆矾样品
 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为
您最近一年使用:0次
名校
解题方法
4 . 2023年10月央视的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
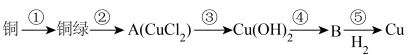
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:______
(2)A、B在无色火焰上灼烧时,其焰色______ (填“相同”或“不相同”),该原理是______ (填“物理”或“化学”)变化。
(3)完成步骤②和③可选用的试剂分别为______ 、______ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少______ ?(写出计算过程)
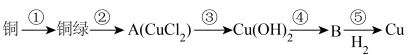
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)A、B在无色火焰上灼烧时,其焰色
(3)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
(4)若在该转化过程中有2mol氧化铜生成,则该氧化铜的质量为多少
您最近一年使用:0次
名校
解题方法
5 . 在下列反应中,HCl作氧化剂的是
| A.NaOH+HCl=NaCl+H2O | B.Zn+2HCl=ZnCl2+H2↑ |
C.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ | D.CuO+2HCl=CuCl2+H2O |
您最近一年使用:0次
2024-01-08更新
|
39次组卷
|
2卷引用:广东省肇庆市四会市四会中学、封开县广信中学2023-2024学年高一上学期第二次月考化学试题
名校
6 . 下列除杂方法正确的是
| 选项 | 物质(杂质) | 除杂方法 |
| A | 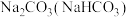 | 加热至恒重 |
| B |  | 加入足量稀盐酸,过滤 |
| C | 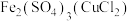 | 加入足量铁粉,过滤 |
| D | 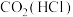 | 用饱和 溶液洗气 溶液洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-01更新
|
478次组卷
|
3卷引用:广东省部分名校2023-2024学年高一上学期联合质量监测化学试卷
名校
解题方法
7 . 某无色透明溶液中可能大量存在Ag+、Mg2+、Fe3+、Cu2+中的一种或几种。请回答下列问题:
(1)不用做任何实验就可以肯定溶液中不存在的离子是___________
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是___________ ,有关反应的离子方程式为___________
(3)取(2)的滤液加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是___________ ,生成沉淀的离子方程式为___________
(4)原溶液中可能大量存在的阴离子是___________ (填序号)。
A.Cl- B. C.OH-
C.OH-
(1)不用做任何实验就可以肯定溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
(3)取(2)的滤液加入过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)原溶液中可能大量存在的阴离子是
A.Cl- B.
 C.OH-
C.OH-
您最近一年使用:0次
名校
解题方法
8 . 下列离子能大量共存的是
A.在含大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.无色澄清透明的溶液中: 、 、 、 、 、 、 、 、 |
C.使无色酚酞试液呈红色的溶液中: 、 、 、 、 、 、 |
D.使石蕊试液变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2023-10-13更新
|
334次组卷
|
6卷引用:广东省广州市广雅集团2023-2024学年高一上学期11月期中考试化学试题
9 . 工业上由含铜废料(含有 、
、 、
、 等)制备硝酸铜晶体的流程如图:
等)制备硝酸铜晶体的流程如图:
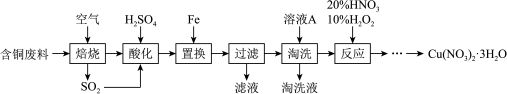
(1)写出CuS“焙烧”生成SO2和CuO的化学反应方程式:_______
(2)“过滤”后需洗涤沉淀,请设计实验证明已洗涤干净_______
(3)“淘洗”所用的溶液A应选用_______ (填序号)a.稀硫酸b.浓硫酸c.稀硝酸d.浓硝酸
(4)“反应”步骤加10%H2O2可以避免污染性气体的产生,写出该反应的离子方程式:_______ ,也可以用气体_______ (填化学式)代替双氧水
(5)大量排放SO2容易造成酸雨等环境问题,工业上可用双碱脱硫法处理废气,过程如图所示,写出双碱脱硫法的总反应方程式:_______
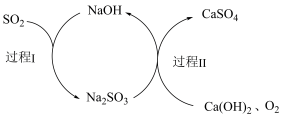
(6)已知:混合气体为SO2与N2的混合气体,为测定SO2在混合气体中的体积分数,实验小组设计了如图实验方案:
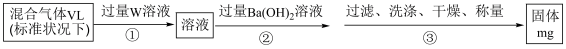
①W溶液可以是_______ (填标号)。
a.H2O2溶液 b.酸性KMnO4溶液 c.氯水
②该混合气体中气体SO2的体积分数为_______ (用含V、m的式子表示)
 、
、 、
、 等)制备硝酸铜晶体的流程如图:
等)制备硝酸铜晶体的流程如图:
(1)写出CuS“焙烧”生成SO2和CuO的化学反应方程式:
(2)“过滤”后需洗涤沉淀,请设计实验证明已洗涤干净
(3)“淘洗”所用的溶液A应选用
(4)“反应”步骤加10%H2O2可以避免污染性气体的产生,写出该反应的离子方程式:
(5)大量排放SO2容易造成酸雨等环境问题,工业上可用双碱脱硫法处理废气,过程如图所示,写出双碱脱硫法的总反应方程式:

(6)已知:混合气体为SO2与N2的混合气体,为测定SO2在混合气体中的体积分数,实验小组设计了如图实验方案:
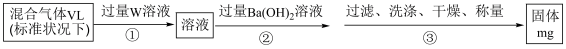
①W溶液可以是
a.H2O2溶液 b.酸性KMnO4溶液 c.氯水
②该混合气体中气体SO2的体积分数为
您最近一年使用:0次
解题方法
10 . 下列化学用语对事实的表征正确的是
A.氮气的电子式: |
B. 分子结构模型: 分子结构模型: |
C. (g)通过灼热铁粉: (g)通过灼热铁粉: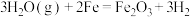 |
D.铜在潮湿空气中易产生铜绿[主要成分为 ]: ]: |
您最近一年使用:0次



