10-11高一下·黑龙江大庆·期中
名校
1 . 将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述中正确的是( )
| A.反应速率:两者相同 |
| B.消耗硝酸的物质的量:前者多,后者少 |
| C.反应生成气体的颜色:前者浅,后者深 |
| D.反应中转移的电子总数:前者多,后者少 |
您最近一年使用:0次
2020-07-02更新
|
719次组卷
|
41卷引用:【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第一次月考化学试题
【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第一次月考化学试题(已下线)【南昌新东方】2019 南昌二中 高一下 第一次月考(已下线)2010—2011学年黑龙江大庆铁人中学高一下学期期中考试化学试卷(已下线)2010—2011浙江省嘉兴一中高一下学期期中考试化学试卷(已下线)2011-2012学年吉林省长春二中高一上学期期末考试化学试卷(已下线)2011-2012学年浙江临海市白云高级中学高一下学期期中考试化学卷(已下线)2012-2013学年浙江省杭州十四中高一上学期期末考试化学试卷(已下线)2012-2013学年广东省深圳科学高中高一第一学期期末考试化学试卷A(已下线)2013-2014黑龙江省大庆铁人中学高一4月月考化学试卷2014-2015甘肃省白银市会宁县五中高一上学期期末化学试卷2014届浙江省东阳中学高三下学期期中考试化学试卷2016届湖南省衡阳县第一中学高三上学期第三次月考化学试卷2016届新疆兵团农二师华山中学高三上学期第二次月考化学试卷2015-2016学年江苏省清江中学高一上期末考试化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2016-2017学年天津市第一中学高一上期末化学卷山西省怀仁县第一中学2016-2017学年高一下学期期中考试化学试题2017-2018学年高一人教版必修一:27 硫酸和硝酸的强氧化性课时训练化学试题高中化学人教版 必修1 第四章 非金属及其化合物 4.氨 硫酸 硝酸 硫酸云南省腾冲市第八中学2017-2018学年高一下学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【押题专练】山东省日照青山学校2018-2019学年高一上学期12月月考化学试题(已下线)【走进新高考】(人教版必修一)4.4.2氨、硝酸、硫酸——硝酸 同步练习02甘肃省金昌市第二中学2018-2019学年高一(文)下学期期中考试化学试题甘肃省武威市古浪县第二中学2020届高三上学期第四次诊断考试化学试题2020届高三化学二轮冲刺新题专练——氮及其氧化物的性质安徽省淮北市第一中学2019-2020学年高一下学期《氮及其化合物性质》 跟进作业 (第三课时)福建省泉州第十六中学2019-2020学年高一下学期5月月考化学试题河北省沧州市河间市第四中学2019-2020学年高一下学期期中考试化学试题(已下线)4.4.2 硫酸和硝酸的氧化性(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)(已下线)练习14 硝酸 酸雨及防治-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物黑龙江省实验中学 2021-2022 学年高一下学期第一次月考4月化学试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题湖北省黄冈市麻城市第二中学2021-2022学年高一下学期6月月考化学试题河南省漯河市2021级普通高中学业水平模拟考试化学试题辽宁省鞍山市普通高中2022-2023学年高一下学期期中考试化学(A卷)试题云南省泸西县第一中学2022-2023学年高一下学期期末考试化学试题云南省保山市腾冲市第八中学2020-2021学年高一下学期期中考试化学试题上海市行知中学2023-2024学年高一下学期期中考试 化学试卷 新疆乌鲁木齐市高级中学2023-2024学年高一下学期期中考试 化学试卷
名校
解题方法
2 . 向Cu和CuO的混合物中加入0.6 L 2.0 mol/L的稀硝酸,混合物完全溶解,同时生成标准状况下NO 4.48 L。向所得溶液中加入一定体积1.0 mol/L NaOH溶液,恰好使Cu2+完全沉淀,将沉淀洗涤,充分灼烧后得32.0 g固体。求:
(1)混合物中Cu的质量是____________ 。
(2)混合物消耗HNO3的物质的量是____________ 。
(3)NaOH溶液的体积是____________ 。
(1)混合物中Cu的质量是
(2)混合物消耗HNO3的物质的量是
(3)NaOH溶液的体积是
您最近一年使用:0次
2020-06-16更新
|
452次组卷
|
2卷引用:江西省南昌市八一中学2019-2020学年高一下学期期中考试化学试题
18-19高一下·江西南昌·阶段练习
名校
解题方法
3 . 将3.2g Cu与30.0mL10.0 mol/L HNO3充分反应,还原产物只有NO和NO2,若反应后溶液中有amol H+,则此溶液中含HNO3的物质的量是
| A.0.5a mol | B.2a mol | C.0.1a mol | D.(0.1+a) mol |
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
名校
解题方法
4 . 铜粉放入稀硫酸中,加热后无明显现象产生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐可能是
| A.Na2CO3 | B.NaNO3 | C.Fe2(SO4)3 | D.FeSO₄ |
您最近一年使用:0次
名校
解题方法
5 . 利用固体表面催化工艺进行NO分解的过程如下图所示。下列说法不正确的是
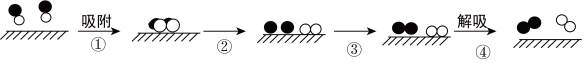

A.该分解过程是:2NO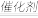 N2+O2 N2+O2 |
| B.实验室制取NO可以用铜与稀硝酸反应 |
| C.过程②释放能量,过程③吸收能量 |
| D.标准状况下,NO分解生成5.6 LN2转移电子数约为6.02×1023 |
您最近一年使用:0次
2020-05-17更新
|
723次组卷
|
9卷引用:【南昌新东方】5 2020年10月江西南昌-南大附中-高三-上学期-月考化学卷
(已下线)【南昌新东方】5 2020年10月江西南昌-南大附中-高三-上学期-月考化学卷河北唐山市2020 届高三第一次模拟考试理科综合化学试题天津市和平区2020届高三第三次质量调查化学试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编广东省东莞市光明中学2020-2021学年高二上学期期中考试化学试题天津市实验中学滨海学校2021届高三上学期第一次月考化学试题江苏省连云港市东海县2021-2022学年高一下学期期中考试化学试题江苏省南京师范大学附属中学2022-2023学年高一下学期期中考试化学试题江苏省常州市第一中学2022-2023学年高一下学期期末测试化学试题
6 . 2.8g铜、银合金与足量的一定浓度的硝酸完全反应,放出的气体与224mL的O2(标准状况)混合,通入水中,恰好完全吸收,则合金中Cu与Ag的质量之比为( )
| A.8∶27 | B.1∶2 | C.27∶8 | D.2∶1 |
您最近一年使用:0次
2020-05-11更新
|
133次组卷
|
2卷引用:江西省吉安市第三中学2023届高三一模考试化学试题
名校
解题方法
7 . 铜与浓硫酸反应的装置如图所示。下列描述合理的是


A.反应过程中,试管Ⅰ中出现灰黑色固体是 |
| B.反应结束后,为观察溶液颜色需向试管Ⅰ中加入水 |
| C.若试管Ⅱ盛放紫色石蕊溶液,可观察到紫色褪至无色 |
| D.为验证气体产物具有还原性,试管Ⅱ可盛放溴水 |
您最近一年使用:0次
2020-05-09更新
|
535次组卷
|
7卷引用:【南昌新东方】5 2020年10月江西南昌-南大附中-高三-上学期-月考化学卷
(已下线)【南昌新东方】5 2020年10月江西南昌-南大附中-高三-上学期-月考化学卷广东省深圳市2020届高三第一次调研考试理科综合能力测试化学试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编安徽省舒城中学2020-2021学年高二上学期开学考试化学试题(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)山东省潍坊市诸城一中2021届高三11月份模拟化学试题(已下线)考向08 金属材料 金属的冶炼-备战2022年高考化学一轮复习考点微专题
8 . 将15.2 g 铜和镁组成的混合物加入250 mL4.0mol•L-1的稀硝酸中,固体完全溶解,生成的气体只有NO。向所得溶液中加入1.0L NaOH溶液,此时金属离子恰好沉淀完全,沉淀质量为25.4 g,下列说法正确的是
| A.原固体混合物中,Cu和Mg的物质的量之比为1:2 |
| B.氢氧化钠溶液的浓度为0.8 mol·L-1 |
| C.固体溶解后的溶液中硝酸的物质的量为0.1mol |
| D.生成的NO气体在标况下的体积为2.24 L |
您最近一年使用:0次
2020-04-22更新
|
1025次组卷
|
6卷引用:江西省临川第一中学暨临川一博中学2021-2022学年高一下学期期中检测化学试题
18-19高一下·江西南昌·阶段练习
解题方法
9 . 亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:

①为制备纯净干燥的气体,装置II中盛放的药品是:__________________ 。写出该装置制备氯气的离子方程式:______________________________________ 。
②为了制备纯净干燥的NO,装置I中蒸馏烧瓶中的试剂为Cu,分液漏斗中装有稀硝酸,则装置II中盛放的是__________ 。
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→_________________________ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO和Cl2外,另一个作用是________________________________ 。
③装置Ⅶ的作用是______________________________________ 。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________________________ 。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:

①为制备纯净干燥的气体,装置II中盛放的药品是:
②为了制备纯净干燥的NO,装置I中蒸馏烧瓶中的试剂为Cu,分液漏斗中装有稀硝酸,则装置II中盛放的是
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO和Cl2外,另一个作用是
③装置Ⅶ的作用是
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为
您最近一年使用:0次
18-19高一下·江西南昌·阶段练习
解题方法
10 . (1)氨气是一种重要的工业原料,工业上常利用氨气检查氯气管道是否漏气。
①写出实验室用熟石灰和氯化铵制取氨气的反应方程式__________________________________
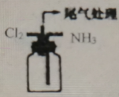
②某学习小组利用下图装置模拟工业上利用氨气检查氯气管道是否漏气。反应开始后,装置内出现白烟并在容器壁内凝结,另一生成物是空气中的主要成分之一。该反应的化学方程式为_____________________________ 。
(2)根据下图操作及现象推断酸X为_________ 。
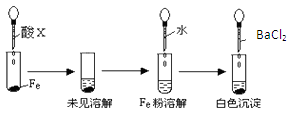
a.浓盐酸 b.浓硫酸 c.浓硝酸
(3)①在100mL 18mol/L的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是__________ (填写代号):
A. 7.32L B. 6.72L C. 20.16L D. 30.24L
②若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_________________ 。
(4)硝酸铀酰[UO2(NO3)2]加热可发生如下分解反应:UO2(NO3)2→UxOY+NO2↑+O2↑(未配平),在600K时,将气体产物收集于试管中并倒扣于水中气体全部被吸收,水充满试管。则UxOY中U的化合价是_________ 。
①写出实验室用熟石灰和氯化铵制取氨气的反应方程式
②某学习小组利用下图装置模拟工业上利用氨气检查氯气管道是否漏气。反应开始后,装置内出现白烟并在容器壁内凝结,另一生成物是空气中的主要成分之一。该反应的化学方程式为

(2)根据下图操作及现象推断酸X为

a.浓盐酸 b.浓硫酸 c.浓硝酸
(3)①在100mL 18mol/L的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A. 7.32L B. 6.72L C. 20.16L D. 30.24L
②若使上述反应中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(4)硝酸铀酰[UO2(NO3)2]加热可发生如下分解反应:UO2(NO3)2→UxOY+NO2↑+O2↑(未配平),在600K时,将气体产物收集于试管中并倒扣于水中气体全部被吸收,水充满试管。则UxOY中U的化合价是
您最近一年使用:0次



