名校
1 . 某小组探究 的催化氧化,实验装置如图,③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟。
的催化氧化,实验装置如图,③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟。
 的催化氧化,实验装置如图,③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟。
的催化氧化,实验装置如图,③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟。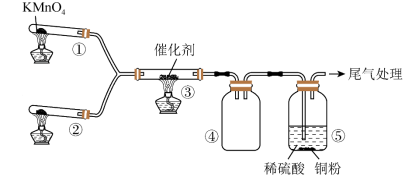
A.①中固体药品可用 代替,②中固体药品可为 代替,②中固体药品可为 与 与 |
B.③、④中现象说明③中的反应是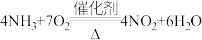 |
C.④中白烟的主要成分是 |
| D.一段时间后,⑤中溶液可能变蓝 |
您最近一年使用:0次
解题方法
2 . 研究硫及其化合物的应用价值对于社会发展意义重大。请回答以下问题。
(1)下图为硫酸铜的制备和转化关系(反应条件略去):____ (选填写“强”或“弱”);
②为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是_______ 。
③由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径______ (选填“甲”或“乙”),理由是_______ 。
(2)用下图所示装置制备纯净的SO2(同时生成一种正盐),请写出发生装置中反应的化学方程式为______ ,装置的连接顺序为: a → _____ → e ( 按气流方向,用小写字母表示 ),碱石灰的主要作用为______ 。
(1)下图为硫酸铜的制备和转化关系(反应条件略去):
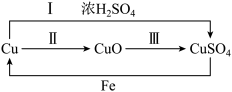
②为验证铜和浓硫酸反应生成的气体,将气体通入品红溶液,观察到的现象是
③由上图可知,制备硫酸铜可以用途径甲(反应Ⅰ)或途径乙(反应Ⅱ+Ⅲ),从环保角度考虑,应选择途径
(2)用下图所示装置制备纯净的SO2(同时生成一种正盐),请写出发生装置中反应的化学方程式为
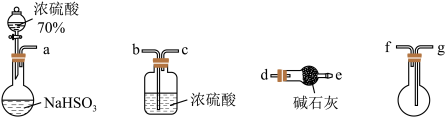
您最近一年使用:0次
3 . 向10.95g铜铝混合物(除铜、铝外无其他物质)中加入2 稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
 稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是
稀硝酸,充分反应后固体完全溶解,收集到V L(已换算成标准状况下的体积)NO气体(无其他气体生成),继续向反应后的混合溶液中滴加NaOH溶液至过量,经过滤﹑洗涤、干燥,得到14.7g固体。下列说法正确的是| A.V约为3.36 |
| B.混合物中铜与铝的物质的量之比为2∶1 |
| C.至少需要400mL稀硝酸 |
| D.滴加NaOH溶液的过程中,固体质量最大为18.2g |
您最近一年使用:0次
2024-05-03更新
|
108次组卷
|
2卷引用:江西省宜春市丰城市第九中学2023-2024学年高一下学期期中考试化学试题
名校
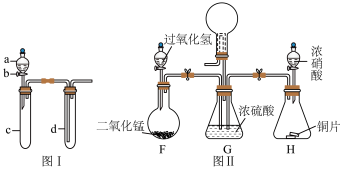
4 . I.铜与稀硝酸反应产生NO,NO又被氧化成NO2,对实验观察无色NO有干扰,过多的NO、NO2又会污染环境。为使实验的设计符合绿色化学的思想,某兴趣小组设计出如图所示装置来改进“铜与硝酸反应”的实验。___________ 。
(2)以下是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案___________ (填甲或乙或丙)。
甲:Cu和浓硝酸反应乙:Cu和稀硝酸反应丙:Cu、O2和稀硝酸反应
Ⅱ.探究NO2、O2混合气体的喷泉实验。
(3)图IIG装置中浓硫酸有三种作用:①___________ ;②混合NO2、O2气体;③观察气泡的速率,控制混合气体的比例。
(4)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则F与H装置中产生气体在同温同压下的体积比是___________ 。
Ⅲ.利用氨气与次氯酸钠反应制备 ,其制备装置如图所示。
,其制备装置如图所示。
(5)仪器 的优点为
的优点为___________ ,仪器 的作用是
的作用是___________ 。
(6)上述装置B、C间缺少一个装置___________ ,可能导致的结果及原因是___________ 。
(2)以下是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案
甲:Cu和浓硝酸反应乙:Cu和稀硝酸反应丙:Cu、O2和稀硝酸反应
Ⅱ.探究NO2、O2混合气体的喷泉实验。
(3)图IIG装置中浓硫酸有三种作用:①
(4)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则F与H装置中产生气体在同温同压下的体积比是
Ⅲ.利用氨气与次氯酸钠反应制备
 ,其制备装置如图所示。
,其制备装置如图所示。 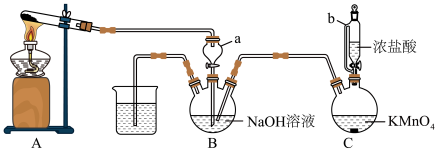
(5)仪器
 的优点为
的优点为 的作用是
的作用是(6)上述装置B、C间缺少一个装置
您最近一年使用:0次
名校
解题方法
5 . 38.4gCu与一定量浓硝酸恰好完全反应生成0.9mol氮的氧化物,这些氧化物恰好溶解在0.5L2mol/LNaOH溶液中得到 和
和 的混合溶液,下列有关判断不正确的是
的混合溶液,下列有关判断不正确的是
 和
和 的混合溶液,下列有关判断不正确的是
的混合溶液,下列有关判断不正确的是| A.硝酸在反应中既体现氧化性又体现酸性 |
| B.氮的氧化物中可能为NO、NO2、N2O4 |
C.混合溶液中 的物质的量是0.6mol 的物质的量是0.6mol |
| D.若浓硝酸体积为200mL,则其物质的量浓度为11mol/L |
您最近一年使用:0次
名校
解题方法
6 . 将铜丝插入浓硝酸中进行如图所示的实验,下列说法正确的是
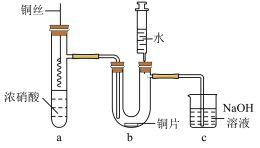

| A.装置a中出现红棕色气体,只体现HNO3的酸性 |
| B.装置c用NaOH吸收尾气,说明NO和NO2均是酸性氧化物 |
| C.注入水后装置b中铜片表面产生气泡,说明Cu与硝酸生成H2 |
| D.一段时间后抽出铜丝,向装置b中U形管内注入水,液体在U形管内在逐渐变成蓝色 |
您最近一年使用:0次
名校
7 . 下列说法正确的是
| A.将HI与浓硫酸混合,有紫色蒸气产生,体现浓硫酸的酸性 |
| B.检验铜和浓硫酸反应后是否生成硫酸铜,可向反应后试管中注入水看溶液是否变蓝 |
| C.浓硫酸与铁加热后发生反应,生成的气体可能是混合物 |
D. 可用作“钡餐”,故 可用作“钡餐”,故 没有毒性 没有毒性 |
您最近一年使用:0次
名校
解题方法
8 . 五水硫酸铜在化工、农业、医药、食品等方面均有广泛的用途,实验室制备方法如下:
(1)制备硫酸铜溶液
称取3.0g铜粉放入双颈烧瓶中,加入11.0mL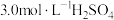 ,再分批缓慢加入5.0mL
,再分批缓慢加入5.0mL 浓
浓 ,待反应缓和后水浴加热。在加热过程中补加6.0mL
,待反应缓和后水浴加热。在加热过程中补加6.0mL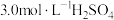 和1.0mL浓硝酸。
和1.0mL浓硝酸。
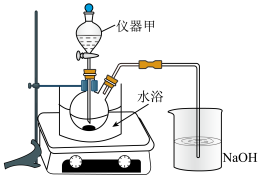
①仪器甲的名称是______ ,硝酸的主要作用是______ 。
②分批加入硝酸的主要原因是______ 。
③实验过程中,观察到有气体生成,NaOH溶液的作用是吸收______ 和______ 。
(2)制得五水硫酸铜粗品
待Cu接近于全部溶解后,趁热用倾析法将溶液转至小烧杯中,然后通过“相关操作”得到粗五水硫酸铜晶体。
①趁热用倾析法转液的目的是______ 、______ 。
②通过“相关操作”得到粗五水硫酸铜晶体,其“相关操作”是指将溶液转至蒸发皿中,水浴加热,______ 。
③如果蒸发水时温度过高,得到的晶体会偏白色,则原因是______ 。(用化学反应方程式表示)
(1)制备硫酸铜溶液
称取3.0g铜粉放入双颈烧瓶中,加入11.0mL
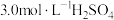 ,再分批缓慢加入5.0mL
,再分批缓慢加入5.0mL 浓
浓 ,待反应缓和后水浴加热。在加热过程中补加6.0mL
,待反应缓和后水浴加热。在加热过程中补加6.0mL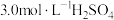 和1.0mL浓硝酸。
和1.0mL浓硝酸。
①仪器甲的名称是
②分批加入硝酸的主要原因是
③实验过程中,观察到有气体生成,NaOH溶液的作用是吸收
(2)制得五水硫酸铜粗品
待Cu接近于全部溶解后,趁热用倾析法将溶液转至小烧杯中,然后通过“相关操作”得到粗五水硫酸铜晶体。
①趁热用倾析法转液的目的是
②通过“相关操作”得到粗五水硫酸铜晶体,其“相关操作”是指将溶液转至蒸发皿中,水浴加热,
③如果蒸发水时温度过高,得到的晶体会偏白色,则原因是
您最近一年使用:0次
2024-04-04更新
|
242次组卷
|
3卷引用:江西省南昌市2024届高三第一次模拟测试化学试卷
9 . 下列实验目的对应的实验操作和现象正确的是
选项 | 实验目的 | 实验操作和现象 |
A | 验证菠菜中含有铁元素 | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入少量稀硝酸后,再加几滴KSCN溶液,溶液变红 |
B | 验证铜与浓硫酸共热反应生成 | 向反应后的溶液中加入水,观察溶液为蓝色 |
C | 证明甲烷与氯气发生反应生成四氯甲烷 | 将装有甲烷与氯气混合物的密封试管进行光照,试管内壁产生油状液滴 |
D | 检验碘仿 中含有碘元素 中含有碘元素 | 取少量碘仿于试管中,用稀 酸化,加入 酸化,加入 溶液,有黄色沉淀生成 溶液,有黄色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 将22.7 g由Cu、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7 g。另取等质量的合金溶于过量稀HNO3中,生成了6.72 L NO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则沉淀的质量为
| A.22.1 g | B.25.4 g | C.33.2g | D.30.2 g |
您最近一年使用:0次
2024-04-01更新
|
509次组卷
|
4卷引用:江西省宜春市高安二中,丰城九中,樟树中学,万载中学五2023-2024学年高一上学期11月月考化学试题
江西省宜春市高安二中,丰城九中,樟树中学,万载中学五2023-2024学年高一上学期11月月考化学试题江西省南昌市第十九中学2023-2024学年高一下学期3月月考化学试题(已下线)5.2.3硝酸和酸雨的防治课后作业提高篇(已下线)专题02 氮及其化合物(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)



