名校
1 . 1.52 g铜镁合金溶于 50 mL密度为 1.40 g/mL、质量分数为 63%的浓硝酸中恰好完全溶解,得到 NO2和 N2O4的混合 气体 1120mL(标准状况)。向反应后的溶液中加入 1.0 mol/L NaOH 溶液,当金属离子全部沉淀时,得到 2.54 g 沉淀。 下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是 2:1 | B.该浓硝酸中 HNO3的物质的量浓度是 14.0 mol/L |
| C.得到 2.54g沉淀时,加入 NaOH 溶液的体积至少 600mL | D.反应过程中转移的电子数是0.03 NA |
您最近一年使用:0次
2 . 将铜粉放入稀硫酸中,加热后无明显现象,但加入某盐一段时间后,发现铜粉质量减少,则该盐不可能是
A. | B.NaCl | C. | D. |
您最近一年使用:0次
2020-09-23更新
|
238次组卷
|
4卷引用:江西省丰城市东煌学校2021-2022学年高一下学期5月月考化学试题
江西省丰城市东煌学校2021-2022学年高一下学期5月月考化学试题高一必修第一册(鲁科2019)第3章 第3节 氮的循环北京第一〇一中学怀柔分校2020-2021学年高一上学期期末考试化学试题(已下线)第12讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)
10-11高一下·内蒙古乌兰察布·期中
名校
解题方法
3 . 铜粉放入稀硫酸中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐可能是( )
A. | B. | C. | D. |
您最近一年使用:0次
2020-09-16更新
|
998次组卷
|
38卷引用:江西省赣州市于都县第三中学、全南县第二中学2017-2018学年高一上学期期末联考化学试题
江西省赣州市于都县第三中学、全南县第二中学2017-2018学年高一上学期期末联考化学试题(已下线)2010—2011学年内蒙古集宁一中高一下学期期中考试化学试卷(已下线)2012届福建省惠安高级中学高三第三次月考化学试卷(已下线)2011-2012年福建漳州芗城中学高一下学期期中考试化学试卷(已下线)2011-2012学年广东省深圳高级中学高一下学期期中化学试卷(已下线)2011-2012学年安徽省马鞍山二中高一下学期期中素质测试化学试卷(已下线)2012-2013学年陕西省长安一中高二下学期期中考试化学试卷(已下线)2013-2014安徽安庆一中下学期期中考试高一化学文科试卷(已下线)2013-2014黑龙江省鹤岗一中高一下学期期中考试化学试卷2014-2015福建省漳浦县三校高一下学期期中联考化学试卷2015-2016学年山东省莱阳一中高一上12月月考化学试卷2015-2016学年黑龙江省佳木斯二中高一上学期期末考试化学试卷2015-2016学年福建师大附中高一下期中化学试卷2016-2017学年山东省菏泽市高一上学期期末考试(B卷)化学试卷2016-2017学年江苏省启东中学高一下学期第一次月考化学试卷2016-2017学年吉林省梅河口第五中学高二下学期第一次月考化学试卷内蒙古杭锦后旗奋斗中学2016-2017学年高一下学期期中考试化学试题山东省昌邑市第一中学2017-2018学年高一上学期期末模拟化学试题山东省枣庄市第三中学2017-2018学年高一1月学情调查化学试题山东师范大学附属中学2017-2018学年高一上学期第二次学分认定(期末)考试化学试题【全国百强校】山东省泰安市新泰市第一中学2018-2019学年高一上学期第二次质量检测化学试题(已下线)【走进新高考】(人教版必修一)4.4.2氨、硝酸、硫酸——硝酸 同步练习02河南省安阳市第二中学2018-2019学年高一上学期期末考试化学试题甘肃省临夏回族自治州积石山县移民中学2019-2020学年高三上学期期中考试化学试题黑龙江省哈尔滨市第六中学2019-2020学年高一上学期期末考试化学试题河北省张家口市崇礼县第一中学2019-2020学年高一下学期期中考试化学试题辽宁省锦州市黑山县黑山中学2019-2020学年高一6月质量检测化学试题鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时2 硫酸鲁科版(2019)高一必修第一册高效手册——第3章 物质的性质与转化广东省佛山市第一中学2019-2020学年高一下学期第一次段考化学试题必修第二册RJ高效学习手册-第五章吉林省长春市实验中学2020-2021学年高一下学期阶段考试化学试题山西省大同市天镇县实验中学2020-2021学年高一下学期阶段性检测化学试题四川省遂宁市射洪中学2021-2022学年高一下学期第一次月考化学试题安徽省青阳县第一中学2021-2022学年高一下学期3月月考化学试题广东省清远市博爱学校2021-2022学年高一下学期第一次教学质量检测化学试题第3课时 硝酸 酸雨及其防治山东省大联考2023-2024学年高一下学期3月月考化学试题
名校
解题方法
4 . 将3.84gCu和一定量浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,Cu反应完毕时,共收集到气体2.24L(标准状况),则反应消耗HNO3的物质的量为( )
| A.0.28mol | B.0.26mol | C.0.24mol | D.0.22mol |
您最近一年使用:0次
2020-09-14更新
|
68次组卷
|
2卷引用:江西省奉新县第一中学2020-2021学年高二上学期第一次月考化学试题
名校
解题方法
5 . 一定条件下,将3.52g铜和铁的混合物溶于30mL一定浓度的热硝酸中,恰好完全反应,得到NO和NO2的混合气体0.08mol,且所得溶液不能使酸性高锰酸钾溶液褪色。向反应后的溶液中加入1mol∙L-1的NaOH溶液,当金属离子恰好全部沉淀时得到6.24g沉淀。该硝酸的浓度为
| A.2.4mol∙L-1 | B.5.3mol∙L-1 | C.7.2mol∙L-1 | D.8mol∙L-1 |
您最近一年使用:0次
2020-08-19更新
|
396次组卷
|
3卷引用:江西省井冈山市宁冈中学2021-2022学年高三下学期开学考试化学试题
解题方法
6 . 铜与一定量浓硝酸反应,得到硝酸铜溶液和22.4L(标准状况)NO2、N2O4、NO的混合气体,这些气体与16.8L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。则消耗铜的质量为
| A.96 g | B.64g | C.48g | D.32g |
您最近一年使用:0次
名校
7 . CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
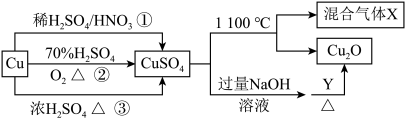
| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为2:3 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.已知1molCuSO4在1100℃所得混合气体X为SO2和O2,则O2为0.75mol |
| D.Y可以是葡萄糖 |
您最近一年使用:0次
2020-07-17更新
|
909次组卷
|
9卷引用:江西省南昌市第二中学2019-2020学年高二下学期期末考试化学试题
江西省南昌市第二中学2019-2020学年高二下学期期末考试化学试题江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题江西省吉安市2020-2021学年高二上学期期中统考化学试题湖北武汉市部分重点中学(六校)2022-2023学年高一下学期期末考试化学试题吉林省长春市东北师范大学附属中学2022-2023学年高一下学期期末考试化学试题河北师范大学附属中学2023-2024学年高二上学期开学考试化学试题河南省洛阳市新安县第一高级中学2023-2024学年高一上学期致远班10月月考化学试题黑龙江省大兴安岭实验中学2023-2024学年高二上学期开学考试化学试卷(已下线)重难点01 浓硫酸、浓硝酸的性质与反应计算-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
13-14高一下·安徽·期中
8 . 将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,共产生NO气体4.48L(标准状况),向所得溶液中加入物质的量浓度为3mol/L的NaOH溶液至沉淀完全。则下列有关叙述中不正确的是
| A.开始加入合金的物质的量之和为0.3mol |
| B.生成沉淀的质量比原合金的质量增加10.2g |
| C.沉淀完全时消耗NaOH溶液的体积为200mL |
| D.反应中被还原和未被还原的硝酸物质的量之比为3:1 |
您最近一年使用:0次
2020-07-11更新
|
323次组卷
|
10卷引用:江西省宜春市宜丰县宜丰中学2019-2020学年高一下学期第一次月考化学试题
江西省宜春市宜丰县宜丰中学2019-2020学年高一下学期第一次月考化学试题(已下线)2013-2014学年安徽师大附中高一下学期期中考查化学试卷2016-2017学年安徽省师大附中高二上入学测试化学试卷江苏省苏州市震泽中学2019-2020学年高一上学期第二次月考化学试题安徽师大附中2019-2020学年高一下学期线上质量评估(期中)化学试题重庆市巴蜀中学2019-2020学年高一下学期期中考试化学试题吉林省白城市洮南市第一中学2020-2021学年高一下学期第一次月考化学试题四川省南充高级中学2020-2021学年高一下学期期中考试化学试题四川省宜宾市叙州区第一中学校2021-2022学年高一下学期期中考试化学试题天津市第二十中学2023-2024学年高一下学期 化学学情调研(一)试卷
名校
解题方法
9 . 有硫酸与硝酸的混合液,取出其中10 mL,加入足量的BaCl2溶液,将生成的沉淀过滤洗涤,干燥称得质量为9.32 g。另取这种溶液10 mL与4 mol·L-1的NaOH溶液25 mL恰好中和。计算:
(1)混合液中H2SO4的物质的量浓度是______
(2)混合液中HNO3的物质的量浓度是______
(3)另取10 mL的混合液与0.96 g铜粉共热时,产生气体在标准状况体积是______ L?
(1)混合液中H2SO4的物质的量浓度是
(2)混合液中HNO3的物质的量浓度是
(3)另取10 mL的混合液与0.96 g铜粉共热时,产生气体在标准状况体积是
您最近一年使用:0次
2020-07-10更新
|
177次组卷
|
2卷引用:江西省上饶中学2019-2020学年高二下学期期末考试化学试题
10-11高一下·黑龙江大庆·期中
名校
10 . 将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述中正确的是( )
| A.反应速率:两者相同 |
| B.消耗硝酸的物质的量:前者多,后者少 |
| C.反应生成气体的颜色:前者浅,后者深 |
| D.反应中转移的电子总数:前者多,后者少 |
您最近一年使用:0次
2020-07-02更新
|
715次组卷
|
40卷引用:【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第一次月考化学试题
【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第一次月考化学试题(已下线)【南昌新东方】2019 南昌二中 高一下 第一次月考(已下线)2010—2011学年黑龙江大庆铁人中学高一下学期期中考试化学试卷(已下线)2010—2011浙江省嘉兴一中高一下学期期中考试化学试卷(已下线)2011-2012学年吉林省长春二中高一上学期期末考试化学试卷(已下线)2011-2012学年浙江临海市白云高级中学高一下学期期中考试化学卷(已下线)2012-2013学年浙江省杭州十四中高一上学期期末考试化学试卷(已下线)2012-2013学年广东省深圳科学高中高一第一学期期末考试化学试卷A(已下线)2013-2014黑龙江省大庆铁人中学高一4月月考化学试卷2014-2015甘肃省白银市会宁县五中高一上学期期末化学试卷2014届浙江省东阳中学高三下学期期中考试化学试卷2016届湖南省衡阳县第一中学高三上学期第三次月考化学试卷2016届新疆兵团农二师华山中学高三上学期第二次月考化学试卷2015-2016学年江苏省清江中学高一上期末考试化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2016-2017学年天津市第一中学高一上期末化学卷山西省怀仁县第一中学2016-2017学年高一下学期期中考试化学试题2017-2018学年高一人教版必修一:27 硫酸和硝酸的强氧化性课时训练化学试题高中化学人教版 必修1 第四章 非金属及其化合物 4.氨 硫酸 硝酸 硫酸云南省腾冲市第八中学2017-2018学年高一下学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【押题专练】山东省日照青山学校2018-2019学年高一上学期12月月考化学试题(已下线)【走进新高考】(人教版必修一)4.4.2氨、硝酸、硫酸——硝酸 同步练习02甘肃省金昌市第二中学2018-2019学年高一(文)下学期期中考试化学试题甘肃省武威市古浪县第二中学2020届高三上学期第四次诊断考试化学试题2020届高三化学二轮冲刺新题专练——氮及其氧化物的性质安徽省淮北市第一中学2019-2020学年高一下学期《氮及其化合物性质》 跟进作业 (第三课时)福建省泉州第十六中学2019-2020学年高一下学期5月月考化学试题河北省沧州市河间市第四中学2019-2020学年高一下学期期中考试化学试题(已下线)4.4.2 硫酸和硝酸的氧化性(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)(已下线)练习14 硝酸 酸雨及防治-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物黑龙江省实验中学 2021-2022 学年高一下学期第一次月考4月化学试题河南省洛阳市洛阳格致学校2021-2022学年高一下学期三月月考化学试题湖北省黄冈市麻城市第二中学2021-2022学年高一下学期6月月考化学试题河南省漯河市2021级普通高中学业水平模拟考试化学试题辽宁省鞍山市普通高中2022-2023学年高一下学期期中考试化学(A卷)试题云南省泸西县第一中学2022-2023学年高一下学期期末考试化学试题云南省保山市腾冲市第八中学2020-2021学年高一下学期期中考试化学试题上海市行知中学2023-2024学年高一下学期期中考试 化学试卷



