名校
解题方法
1 . 甲烷在地壳中储量丰富,该物质是一种重要的燃料和工业原料。请回答下列问题:
(1)甲烷的燃烧热 kJ⋅mol
kJ⋅mol ,则一定量
,则一定量 完全燃烧生成1 mol
完全燃烧生成1 mol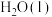 时放出的热量为
时放出的热量为_______ kJ。
(2)甲烷、水蒸气重整可获取合成气(CO、 ),涉及的主反应和副反应如下:
),涉及的主反应和副反应如下:
主反应:


副反应:
 kJ⋅mol
kJ⋅mol

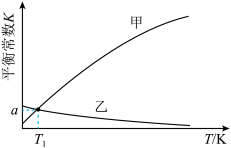
两个反应的平衡常数随温度的变化曲线如图所示,则表示主反应的曲线是_______ (填“甲”或“乙”);温度为 K时,反应
K时,反应 的平衡常数
的平衡常数
_______ (用含a的代数式表示)。 )有利于实现“碳中和”,该甲烷重整的反应为
)有利于实现“碳中和”,该甲烷重整的反应为

①下列措施能使甲烷平衡转化率提高的是_______ (填字母,下同),能使平衡常数增大的是_______ 。
A增大 的浓度 B.升高温度 C.增大压强 D.减小
的浓度 B.升高温度 C.增大压强 D.减小 的浓度
的浓度
②一定条件下,在2 L恒容密闭容器中充入2 mol 和一定量的
和一定量的 发生上述反应,测得初始压强为
发生上述反应,测得初始压强为 ,10 min时容器内压强不再变化,且压强为
,10 min时容器内压强不再变化,且压强为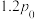 ,0~10min内平均反应速率
,0~10min内平均反应速率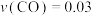 mol⋅L
mol⋅L ⋅min
⋅min ,达到平衡时
,达到平衡时 的转化率为
的转化率为_______ %,初始时加入的 为
为_______ mol。
(1)甲烷的燃烧热
 kJ⋅mol
kJ⋅mol ,则一定量
,则一定量 完全燃烧生成1 mol
完全燃烧生成1 mol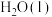 时放出的热量为
时放出的热量为(2)甲烷、水蒸气重整可获取合成气(CO、
 ),涉及的主反应和副反应如下:
),涉及的主反应和副反应如下:主反应:



副反应:

 kJ⋅mol
kJ⋅mol

两个反应的平衡常数随温度的变化曲线如图所示,则表示主反应的曲线是
 K时,反应
K时,反应 的平衡常数
的平衡常数
 )有利于实现“碳中和”,该甲烷重整的反应为
)有利于实现“碳中和”,该甲烷重整的反应为

①下列措施能使甲烷平衡转化率提高的是
A增大
 的浓度 B.升高温度 C.增大压强 D.减小
的浓度 B.升高温度 C.增大压强 D.减小 的浓度
的浓度②一定条件下,在2 L恒容密闭容器中充入2 mol
 和一定量的
和一定量的 发生上述反应,测得初始压强为
发生上述反应,测得初始压强为 ,10 min时容器内压强不再变化,且压强为
,10 min时容器内压强不再变化,且压强为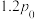 ,0~10min内平均反应速率
,0~10min内平均反应速率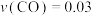 mol⋅L
mol⋅L ⋅min
⋅min ,达到平衡时
,达到平衡时 的转化率为
的转化率为 为
为
您最近一年使用:0次
2024-05-07更新
|
107次组卷
|
2卷引用:2024届海南省琼海市嘉积中学高三下学期模拟预测化学试题
名校
解题方法
2 . 在25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的摩尔燃烧焓依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2 800 kJ/mol,则下列热化学方程式正确的是
A.C(s)+ O2(g)=CO(g) ΔH=-393.5 kJ/mol O2(g)=CO(g) ΔH=-393.5 kJ/mol |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ/mol |
| C.2H2(g)+O2(g)=2H2O(l) ΔH=+571.6 kJ/mol |
D. C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) ΔH=-1 400 kJ/mol C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) ΔH=-1 400 kJ/mol |
您最近一年使用:0次
2023-08-26更新
|
1342次组卷
|
53卷引用:2016届海南省华侨中学高三考前模拟理综化学试卷
2016届海南省华侨中学高三考前模拟理综化学试卷(已下线)2011-2012学年海南省洋浦中学高二下学期期末考试化学试卷(已下线)2013届陕西省宝鸡市高三第三次模拟理综化学试卷(已下线)2013-2014学年海南省三亚市一中高二上学期期中考试理科化学试卷(已下线)2013-2014学年海南三亚一中高二上学期期中考试理科化学试卷(B)2016届贵州省遵义航天高级中学高三第五次模拟理科综合试卷华中师范大学海南附属中学2019-2020学年高二上学期第三次月考化学试题(已下线)单项选择题(已下线)09-10年温州市高二下学期期末四校联考化学卷(已下线)2010年河北省邯郸市高二上学期期末考试化学试卷(已下线)2010—2011学年湖北省长阳一中高二上学期期末考试化学试卷(已下线)2011-2012学年陕西省西安市第一中学高二上学期期中考试化学试卷(已下线)2011-2012学年江西上饶中学高一零点、实验班下期末化学试卷(已下线)2014届高考化学二轮复习提分训练 专题5化学反应与能量练习卷(已下线)2014-2015学年山西省太原第五中学高二10月月考化学试卷2014-2015四川省邛崃市高埂中学高二下学期第一次月考化学试卷2015-2016学年贵州省思南中学高二上第一半月考化学试卷2016-2017学年河北省涿鹿中学高二上学期第一次月考化学试卷2016-2017学年吉林省汪清六中高二上第一次月考化学试卷2016-2017学年广西柳州铁路一中高二上段考理化学卷辽宁省鞍山市第一中学2016-2017学年高一下学期期中考试化学试题宁夏银川市六盘山高级中学2017-2018学年高二上学期第一次月考化学试题山东省临沂市蒙阴县实验中学2017-2018学年高二上学期期中考试化学试题1山东省临沂市蒙阴县实验中学2017-2018学年高二上学期期中考试化学试题2山西省忻州二中2018-2019学年高二上学期期中考试化学试题(已下线)2019年9月1日《每日一题》人教选修4—— 每周一测河南省周口中英文学校2019-2020学年高二上学期第一次月考化学试题四川省广安市岳池县顾县中学2019—2020学年第一学期高二上学期期中测试化学(选修四)试题山西省运城市景胜中学2019-2020学年高二上学期期中考试化学试题江西省上饶市“山江湖”协作体2019-2020学年高二上学期期中联考(自主班)化学试题云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题(已下线)1.2 燃烧热 能源(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)内蒙古自治区通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二上学期期中考试化学试题河南省豫北名校2020-2021学年高二上学期11月质量检测化学试题江苏省南菁高级中学2020-2021学年度高二上学期第一次阶段性考试化学(强化班)试题江苏省江阴长泾中学2020~2021学年下学期期中考试化学试题青海省海东市第二中学2020-2021学年高二4月月考化学试题吉林省长春外国语学校2020-2021学年高一下学期期末考试化学试题(已下线)第二节 燃烧热 能源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)(已下线)1.1.2 热化学方程式 燃烧热-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题18 化学反应与能量(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练甘肃省舟曲县第一中学2021-2022学年高二上学期第一次月考化学试题江西省吉安市(吉安县三中、泰和二中、安福二中、井大附中 )2021-2022学年高二上学期期中考试化学试题山西省运城市康杰中学2021-2022学年高二上学期期中化学试题(已下线)1.1.2 热化学方程式 燃烧热(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)1.1.2 热化学方程式 燃烧热(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第02讲 热化学方程式与燃烧热(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第一章 化学反应的热效应(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)云南省昆明市寻甸县第二中学2022-2023学年高二上学期10月月考 化学试卷第3课时 反应焓变的计算(已下线)专题01 反应热、焓变与热化学方程式【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
解题方法
3 . 已知:①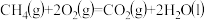
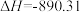 kJ·mol-1
kJ·mol-1
②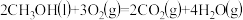
 kJ·mol-1
kJ·mol-1
③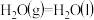
 kJ·mol-1
kJ·mol-1
下列说法正确的是
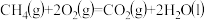
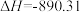 kJ·mol-1
kJ·mol-1②
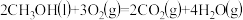
 kJ·mol-1
kJ·mol-1③
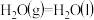
 kJ·mol-1
kJ·mol-1下列说法正确的是
A.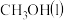 的燃烧热 的燃烧热 kJ·mol-1 kJ·mol-1 |
B. 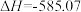 kJ·mol-1 kJ·mol-1 |
C.等物质的量的 和 和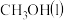 完全燃烧, 完全燃烧, 放出的热量更多 放出的热量更多 |
D.在中性溶液中, 和 和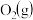 不能形成燃料电池 不能形成燃料电池 |
您最近一年使用:0次
名校
4 . 化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,错误的是( )
| A.钢铁腐蚀时可能发生的正极反应:2H2O + O2+ 4e-= 4OH- |
| B.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol |
C.纯碱水解的离子方程式:CO32-+H2O HCO3-+ OH- HCO3-+ OH- |
| D.Ca(HCO3)2溶液中加入过量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O |
您最近一年使用:0次
2019-01-30更新
|
248次组卷
|
6卷引用:2016届海南中学高三高考模拟八化学试卷
2016届海南中学高三高考模拟八化学试卷(已下线)2012届陕西省铁一中高三第二次模拟考试化学试卷(已下线)2012届陕西省铁一中高三第二次模拟考试化学试卷 (已下线)2011届陕西省西安铁一中高三上学期摸底考试化学试卷夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解的基础考查山西省实验中学2020届高三化学复习针对性试题集(六)
5 . 下列描述中,正确的是
| A.由 CH3CH2OH(l)+3O2(g) =2CO2 (g)+3H2O(g) ΔH=-1366.8 kJ·mol-1,可知乙醇的标准燃烧热为1366.8 kJ·mol-1 |
| B.已知:C(金刚石,s)=C(石墨,s) ΔH<0,则金刚石比石墨稳定 |
| C.已知:N2(g)+O2(g)=2NO(g) ΔH=+180 kJ·mol-12CO(g)+O2(g)=2CO2 (g) ΔH=-566 kJ·mol-1则2CO(g)+2NO(g)===N2 (g)+2CO2(g) ΔH=-746 kJ·mol-1 |
| D.OH-(aq)+H+(aq)===H2O(l)ΔH=-57.3 kJ·mol-1故1 molHNO3与1mol NH3•H2O 完全反应,放出的热量一定为57.3 kJ·mol-1 |
您最近一年使用:0次
2016-12-09更新
|
229次组卷
|
3卷引用:2016届海南师大附中高三临考模拟化学试卷
6 . 下列说法正确的是
| A.CO(g)的燃烧热:△H="-283.0KJ/" mol,则 2CO2(g ) =2CO(g)+O2(g)反应的△H=" -55.0KJ/" mol |
| B.已知NaOH(aq) +HCl(aq )=" NaCl(aq)" +H2O(l)△H =" -57.30KJ/" mol-1,则含40.0gNaOH的稀溶液与稀醋酸完全中和,放出57.3KJ的热量 |
| C.已知2C(s)+2O2(g)=2CO2 (g)△H=a;2C(s)+O2 (g )=2CO(g)△H=b;则a>b |
| D.已知c(石墨,s)= C(金刚石,s)△H>0,则石墨比金刚石稳定 |
您最近一年使用:0次
2011·海南海口·一模
7 . 某兴趣小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后生成的白色物质进行了如下探究:
[实验]将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧至完全,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,你认为物质燃烧的条件是______________ 。
(2)实验室不小心发生钠着火,下列灭火方法正确的是__________
A.用水扑灭 B.用泡沫灭火器扑灭
C.用干粉灭火器扑灭 D.用砂子扑灭
[提出假设]
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:白色物质是Na2O和Na2CO3的混合物。
[设计实验方案.验证假设]该小组对燃烧后生成的白色物质进行如下探究:
[思考与交流]
(3)甲同学认为方案1得到的结论不正确,其理由是_________________ 。
(4)乙同学认为方案2得到的结论正确,白色物质为_______________ 。理由是____________________ 。
(5)写出钠在二氧化碳中燃烧的化学方程式为________________ 。
(6)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:____________________________ 。
[实验]将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧至完全,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)通过钠在CO2气体中燃烧的实验,你认为物质燃烧的条件是
(2)实验室不小心发生钠着火,下列灭火方法正确的是
A.用水扑灭 B.用泡沫灭火器扑灭
C.用干粉灭火器扑灭 D.用砂子扑灭
[提出假设]
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:白色物质是Na2O和Na2CO3的混合物。
[设计实验方案.验证假设]该小组对燃烧后生成的白色物质进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ① 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的BaCl2溶液 | 出现白色沉淀 | |
| ② 静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
[思考与交流]
(3)甲同学认为方案1得到的结论不正确,其理由是
(4)乙同学认为方案2得到的结论正确,白色物质为
(5)写出钠在二氧化碳中燃烧的化学方程式为
(6)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:
您最近一年使用:0次
2011·全国·高考真题
真题
8 . 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________ kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________ ;
(3)在溶积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
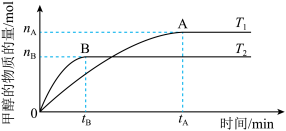
下列说法正确的是________ (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)= mol·L-1·min-1
mol·L-1·min-1
②该反应在T时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为______ ;
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为________ 、正极的反应式为________ 。理想状态下,该燃料电池消耗1mol甲醇所能产生的最大电能为702.1kJ,则该燃料电池的理论效率为________ (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
(1)用太阳能分解10mol水消耗的能量是
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)在溶积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);

下列说法正确的是
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=
 mol·L-1·min-1
mol·L-1·min-1②该反应在T时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时
 增大
增大(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为
(5)在直接以甲醇为燃料电池中,电解质溶液为酸性,负极的反应式为
您最近一年使用:0次



