名校
1 . 请回答下列问题:
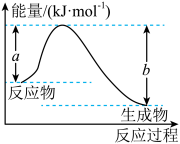
(1)如图表示某反应的能量变化关系,则此反应为___________ (填“吸热”或“放热”)反应,其中ΔH=___________ (用含有a、b的关系式表示)。___________ 114.6kJ(填“大于”、“等于”或“小于”)。
(3)在25℃,101kPa下,16g的N2H4(g)完全燃烧生成氮气和液态水时放热316kJ,则表示N2H4(g)燃烧热的热化学方程式为___________ 。
(4)甲醇(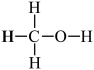 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=___________ 。
(1)如图表示某反应的能量变化关系,则此反应为
(3)在25℃,101kPa下,16g的N2H4(g)完全燃烧生成氮气和液态水时放热316kJ,则表示N2H4(g)燃烧热的热化学方程式为
(4)甲醇(
 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
CH3OH(g) ΔH。已知反应中相关的化学键键能数据如下:H-H键键能为436kJ/mol;C-O键键能为343kJ/mol;H-O键键能为463kJ/mol;H-C键键能为413kJ/mol;CO中的化学键键能为1071kJ/mol。计算该反应的ΔH=
您最近半年使用:0次
名校
解题方法
2 . 甲烷在地壳中储量丰富,该物质是一种重要的燃料和工业原料。请回答下列问题:
(1)甲烷的燃烧热 kJ⋅mol
kJ⋅mol ,则一定量
,则一定量 完全燃烧生成1 mol
完全燃烧生成1 mol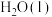 时放出的热量为
时放出的热量为_______ kJ。
(2)甲烷、水蒸气重整可获取合成气(CO、 ),涉及的主反应和副反应如下:
),涉及的主反应和副反应如下:
主反应:


副反应:
 kJ⋅mol
kJ⋅mol

两个反应的平衡常数随温度的变化曲线如图所示,则表示主反应的曲线是_______ (填“甲”或“乙”);温度为 K时,反应
K时,反应 的平衡常数
的平衡常数
_______ (用含a的代数式表示)。 )有利于实现“碳中和”,该甲烷重整的反应为
)有利于实现“碳中和”,该甲烷重整的反应为

①下列措施能使甲烷平衡转化率提高的是_______ (填字母,下同),能使平衡常数增大的是_______ 。
A增大 的浓度 B.升高温度 C.增大压强 D.减小
的浓度 B.升高温度 C.增大压强 D.减小 的浓度
的浓度
②一定条件下,在2 L恒容密闭容器中充入2 mol 和一定量的
和一定量的 发生上述反应,测得初始压强为
发生上述反应,测得初始压强为 ,10 min时容器内压强不再变化,且压强为
,10 min时容器内压强不再变化,且压强为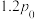 ,0~10min内平均反应速率
,0~10min内平均反应速率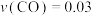 mol⋅L
mol⋅L ⋅min
⋅min ,达到平衡时
,达到平衡时 的转化率为
的转化率为_______ %,初始时加入的 为
为_______ mol。
(1)甲烷的燃烧热
 kJ⋅mol
kJ⋅mol ,则一定量
,则一定量 完全燃烧生成1 mol
完全燃烧生成1 mol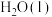 时放出的热量为
时放出的热量为(2)甲烷、水蒸气重整可获取合成气(CO、
 ),涉及的主反应和副反应如下:
),涉及的主反应和副反应如下:主反应:



副反应:

 kJ⋅mol
kJ⋅mol

两个反应的平衡常数随温度的变化曲线如图所示,则表示主反应的曲线是
 K时,反应
K时,反应 的平衡常数
的平衡常数
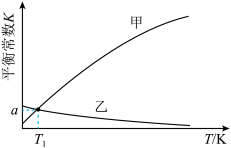
 )有利于实现“碳中和”,该甲烷重整的反应为
)有利于实现“碳中和”,该甲烷重整的反应为

①下列措施能使甲烷平衡转化率提高的是
A增大
 的浓度 B.升高温度 C.增大压强 D.减小
的浓度 B.升高温度 C.增大压强 D.减小 的浓度
的浓度②一定条件下,在2 L恒容密闭容器中充入2 mol
 和一定量的
和一定量的 发生上述反应,测得初始压强为
发生上述反应,测得初始压强为 ,10 min时容器内压强不再变化,且压强为
,10 min时容器内压强不再变化,且压强为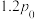 ,0~10min内平均反应速率
,0~10min内平均反应速率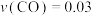 mol⋅L
mol⋅L ⋅min
⋅min ,达到平衡时
,达到平衡时 的转化率为
的转化率为 为
为
您最近半年使用:0次
3 . 请根据学过的知识回答下列问题:
(1)
 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程___________ 。
(2)已知: 键的键能是
键的键能是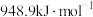 ,
, 键的键能是
键的键能是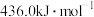 ,
, 键的键能是
键的键能是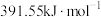 ,则
,则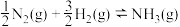

___________ 。
(3)已知:①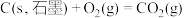

②

③

则298K时反应 的焓变:
的焓变:
___________ 。
(4)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  。
。
①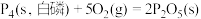

②

(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为___________ 。
(6)如图所示,某反应在不同条件下的反应历程分别为a、b。
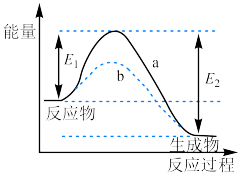
据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,反应历程a、b的反应热___________ (填“相同”或“不相同”)。
(1)

 完全燃烧生成液态水时放出341.7kJ热量,则表示
完全燃烧生成液态水时放出341.7kJ热量,则表示 燃烧热的热化学方程
燃烧热的热化学方程(2)已知:
 键的键能是
键的键能是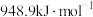 ,
, 键的键能是
键的键能是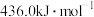 ,
, 键的键能是
键的键能是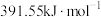 ,则
,则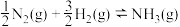

(3)已知:①
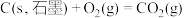

②


③


则298K时反应
 的焓变:
的焓变:
(4)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 。
。①
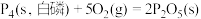

②


(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和

 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(6)如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近半年使用:0次
4 . 已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l)  =-890kJ/mol
=-890kJ/mol
CO(g)+1/2O2(g)=CO2(g) =-282.5kJ/mol。
=-282.5kJ/mol。
假如标准状况下由CH4、CO、CO2组成的89.6升混和气体完全燃烧时能放出1010千焦的热量,并生成18克液态水,那么燃烧前混和气体中CO占的体积百分含量约为
 =-890kJ/mol
=-890kJ/molCO(g)+1/2O2(g)=CO2(g)
 =-282.5kJ/mol。
=-282.5kJ/mol。假如标准状况下由CH4、CO、CO2组成的89.6升混和气体完全燃烧时能放出1010千焦的热量,并生成18克液态水,那么燃烧前混和气体中CO占的体积百分含量约为
| A.40% | B.50% | C.60% | D.70% |
您最近半年使用:0次
名校
解题方法
5 . 质量为2.0g的H2完全燃烧,恢复至室温,测得反应放出的热量为285.8kJ,则下列热化学方程式正确的是
A.  |
B.  |
C.  |
D. 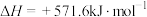 |
您最近半年使用:0次
名校
解题方法
6 . 甲醇(CH3OH)广泛用作燃料电池的燃料,可由天然气来合成,已知:
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=−71 kJ∙mol−1
②CO(g)+2H2(g)=CH3OH(l) ΔH=-90.5 kJ∙mol−1
③CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=−890 kJ∙mol−1
(1)甲醇的燃烧热为__________ 。
(2)若CO的燃烧热为282.5 kJ∙mol−1,则H2的燃烧热为___________ 。
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=−71 kJ∙mol−1
②CO(g)+2H2(g)=CH3OH(l) ΔH=-90.5 kJ∙mol−1
③CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=−890 kJ∙mol−1
(1)甲醇的燃烧热为
(2)若CO的燃烧热为282.5 kJ∙mol−1,则H2的燃烧热为
您最近半年使用:0次
名校
解题方法
7 . 下列说法或表示方法中,正确的是
A.由热化学方程式: C2H5OH(l)+ C2H5OH(l)+  O2(g)=CO2(g)+ O2(g)=CO2(g)+  H2O(l) ΔH=-683.4 kJ∙mol−1知乙醇的燃烧热为683.4 kJ∙mol−1 H2O(l) ΔH=-683.4 kJ∙mol−1知乙醇的燃烧热为683.4 kJ∙mol−1 |
| B.由C(金刚石)→ C(石墨) ΔH= −119 kJ∙mol−1可知,金刚石比石墨稳定 |
| C.H+(aq) + OH一(aq) = H2O(1) ΔH=−57.3 kJ∙mol−1。若将含0.5mol H2SO4的浓硫酸与含1molNaOH的稀溶液混合,放出的热量大于57.3 kJ |
| D.在101kPa 25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g) + O2(g) = 2H2O(1) ΔH = −285.8 kJ∙mol−1 |
您最近半年使用:0次
名校
8 . 填空
(1)已知: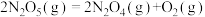
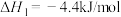

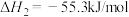
则反应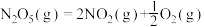

_______ kJ/mol。
(2)已知相关的化学键键能数据如下:
则

_______ kJ/mol。
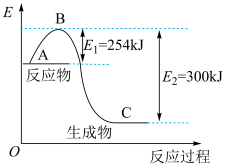
(3)下图是 和
和 反应生成
反应生成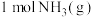 过程中能量变化示意图,合成氨反应的热化学方程式为
过程中能量变化示意图,合成氨反应的热化学方程式为_______ 。
(4)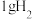 燃烧生成
燃烧生成 放热121 kJ,
放热121 kJ, 蒸发吸热44 kJ,
蒸发吸热44 kJ, 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(5)①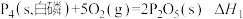
②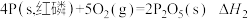
常温时红磷比白磷稳定,则
_______  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(1)已知:
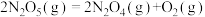
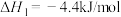

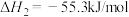
则反应
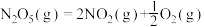

(2)已知相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | 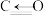 |
键能/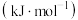 | 413 | 745 | 436 | 1075 |


(3)下图是
 和
和 反应生成
反应生成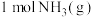 过程中能量变化示意图,合成氨反应的热化学方程式为
过程中能量变化示意图,合成氨反应的热化学方程式为
(4)
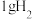 燃烧生成
燃烧生成 放热121 kJ,
放热121 kJ, 蒸发吸热44 kJ,
蒸发吸热44 kJ, 燃烧热的热化学方程式为
燃烧热的热化学方程式为(5)①
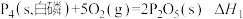
②
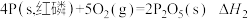
常温时红磷比白磷稳定,则

 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
您最近半年使用:0次
2024-01-12更新
|
322次组卷
|
2卷引用:海南省海口市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
9 . 请回答下列问题:
(1)据了解,我国的三峡工程将提供相当于3000万千瓦火力发电站的水力发电功率。因此,三峡工程建设将有助于控制___________
(2)已知1g炭粉在氧气中完全燃烧放出热量32.8kJ(与1g原煤相当),若以火力发电,要达3000万千瓦的功率,每年至少需耗原煤多少万吨?(每年按365天计, )
)___________
(1)据了解,我国的三峡工程将提供相当于3000万千瓦火力发电站的水力发电功率。因此,三峡工程建设将有助于控制___________
| A.温室效应 | B.白色污染 |
| C.城市污水的任意排放 | D.长江中、下游的洪涝灾害 |
 )
)
您最近半年使用:0次
10 . 我国锅炉燃煤采用沸腾炉(你了解沸腾炉吗?)逐渐增多,其好处在于
| A.增大煤炭燃烧时的燃烧热并形成清洁能源 |
| B.减少炉中杂质气体(如SO2)的形成 |
| C.提高煤炭的热效率并减少CO的排放 |
| D.使燃料充分燃烧,从而提高燃料的利用率 |
您最近半年使用:0次



