名校
解题方法
1 . 下列化学反应的表示正确的是
A.尿素和 溶液在碱性条件下反应: 溶液在碱性条件下反应: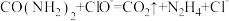 |
B.1-溴丙烷与氢氧化钠水溶液共热: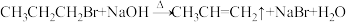 |
C.过量氨水和硫酸铜溶液反应: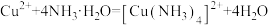 |
D.常温下 为液体,具有很高的燃烧热 为液体,具有很高的燃烧热 ,肼燃烧的热化学方程式: ,肼燃烧的热化学方程式: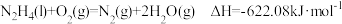 |
您最近半年使用:0次
名校
解题方法
2 . 25 ℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.69 kJ,下列热化学方程式正确的是
| A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=726kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1 |
| C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-726 kJ·mol-1 |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=1 452 kJ·mol-1 |
您最近半年使用:0次
3 . 下列关于热化学反应的描述正确的是
| A.HCl和NaOH反应的反应热ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3) kJ·mol-1 |
| B.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH<-890.3 kJ·mol-1 |
| C.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+566.0 kJ·mol-1 |
D.已知:500 ℃、30 MPa下,N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1;将3 mol H2和过量的N2在此条件下充分反应,会放出92.4 kJ热量 2NH3(g) ΔH=-92.4 kJ·mol-1;将3 mol H2和过量的N2在此条件下充分反应,会放出92.4 kJ热量 |
您最近半年使用:0次
4 . 下列有关热化学方程式的叙述中正确的是
| A.中和热的离子方程式为:OH-(aq)+H+(aq)=H2O(g) ∆H=-57.3 kJ·mol-1 |
| B.已知C(s)+O2(g)=CO2(g) ∆H1,C(s)+O2(g)=CO2(s) ∆H2,则∆H1>∆H2 |
| C.已知2H2(g)+O2(g)=2H2O(l) ∆H=-571.6 kJ·mol-1,则H2的燃烧热为-571.6 kJ·mol-1 |
| D.已知C(石墨,s)=C(金刚石,s) ∆H=+1.9 kJ·mol-1,则金刚石比石墨稳定 |
您最近半年使用:0次
5 . 填空
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:_____ 。反应III为_____ (选填“吸热”或“放热”)反应。
(2)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为_____ 。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____ 。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
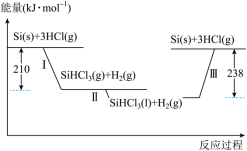
(2)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近半年使用:0次
名校
6 . 中国航天科技发展举世瞩目。2020年“嫦娥五号”成功携带月球样品返回地球,2021年“天问一号”着陆火星,它们都是由以液氢为燃料的“长征五号”火箭搭载升空的。下列有关说法错误的是
| A.氢气燃烧的产物不污染环境 |
| B.低温液态储氢可以大大提高氢气的密度,降低储运成本 |
C.已知 , ,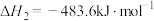 ,则 ,则 燃烧热 燃烧热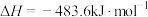 |
| D.获取氢气的方法较多,包括水的电解、煤的气化、乙烷裂解和氯碱工业等 |
您最近半年使用:0次
7 . 下列化学反应的表示正确的是
A.尿素和NaClO溶液在碱性条件下反应: |
B.过量氨水和硫酸铜溶液反应: |
C.1-溴丙烷与氢氧化钠水溶液共热: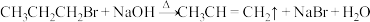 |
D.常温下N2H4为液体,具有很高的燃烧热(622.08 kJ⋅mol-1),肼燃烧的热化学方程式: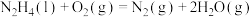 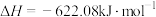 |
您最近半年使用:0次
解题方法
8 . 下列说法正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l) ΔH=−57.3kJ∙mol−1,在中和热的测定时实际加入的酸碱的量的多少会影响该反应的ΔH |
| B.1mol H2与0.5mol O2反应放出的热量就是H2的燃烧热 |
| C.加入催化剂可以改变反应的活化能,不能改变焓变 |
D.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ∆H=−38.6kJ∙mol−1 2NH3(g) ∆H=−38.6kJ∙mol−1 |
您最近半年使用:0次
解题方法
9 . 电池有铅蓄电池、燃料电池(如NO2NH3电池)、锂离子电池、Mg—次氯酸盐电池等,它们可以将化学能转化为电能。NH3、CH4、NaBH4都可用作燃料电池的燃料。CH4的燃烧热为890.3kJ•mol-1。电解则可以将电能转化为化学能,电解饱和NaCl溶液可以得到Cl2,用电解法可制备消毒剂高铁酸钠(Na2FeO4)。下列化学反应表示正确的是
A.铅蓄电池的正极反应:Pb-2e-+SO =PbSO4 =PbSO4 |
B.电解饱和NaCl溶液:2Na++2Cl- 2Na+Cl2↑ 2Na+Cl2↑ |
| C.CH4燃烧:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3kJ•mol-1 |
D.一定条件下NO2与NH3的反应:6NO2+8NH3 7N2+12H2O 7N2+12H2O |
您最近半年使用:0次
10 . 已知CH4的燃烧热为890.3 kJ·mol-1,下列化学反应表示正确的是
A.铅蓄电池的正极反应:Pb-2e-+ =PbSO4 =PbSO4 |
B.电解饱和NaCl溶液:2Na++2Cl- 2Na+Cl2↑ 2Na+Cl2↑ |
| C.CH4燃烧:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H=-890.3 kJ·mol-1 |
D.一定条件下NO2与NH3的反应:6NO2+8NH3 7N2+12H2O 7N2+12H2O |
您最近半年使用:0次



