1 . 肼 常用作火箭燃料,燃烧
常用作火箭燃料,燃烧 肼生成液态水时放出
肼生成液态水时放出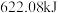 热量,可由
热量,可由 与
与 反应制备;下列变化的方程式表示正确的是
反应制备;下列变化的方程式表示正确的是
 常用作火箭燃料,燃烧
常用作火箭燃料,燃烧 肼生成液态水时放出
肼生成液态水时放出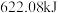 热量,可由
热量,可由 与
与 反应制备;下列变化的方程式表示正确的是
反应制备;下列变化的方程式表示正确的是A.次氯酸在水中的电离: |
B. 与 与 反应制备肼: 反应制备肼: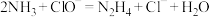 |
C.肼的燃烧: |
D. 与 与 的水溶液反应制备硒: 的水溶液反应制备硒: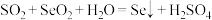 |
您最近一年使用:0次
名校
2 . ⅤA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。氨是重要的化工原料,广泛用于生产铵盐、硝酸、纯碱、医药等;肼( )的燃烧热为624kJ/mol,是常用的火箭燃料。白磷(
)的燃烧热为624kJ/mol,是常用的火箭燃料。白磷( )晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(
)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸( )为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
)为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
 )的燃烧热为624kJ/mol,是常用的火箭燃料。白磷(
)的燃烧热为624kJ/mol,是常用的火箭燃料。白磷( )晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(
)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸( )为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
)为一元弱酸,H3PO4为三元中强酸。雌黄(As2S3)和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4(沸点114 ℃)并放出H2S气体。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。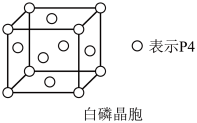
| A.NO2制HNO3的离子方程式:3NO2+H2O=2HNO3 +NO |
B.次磷酸与足量NaOH溶液反应: |
C.肼燃烧的热化学方程式: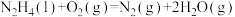 ; ;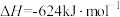 |
| D.雌黄制备雄黄的化学方程式:2As2S3+2SnCl2+4HCl=As4S4+2SnCl4+2H2S↑ |
您最近一年使用:0次
2024-03-04更新
|
269次组卷
|
3卷引用:江苏省连云港高级中学2023-2024学年高三下学期4月期中考试化学试题
名校
3 . 周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似, 的熔点为
的熔点为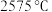 ,熔融时
,熔融时 能导电,而
能导电,而 不能导电;
不能导电; 的燃烧热为
的燃烧热为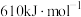 ,实验室中常用酸性
,实验室中常用酸性 测定物品中不溶性
测定物品中不溶性 的含量。铍镍合金可用于制造弹簧秤的弹簧,
的含量。铍镍合金可用于制造弹簧秤的弹簧, 可用作隔音材料,
可用作隔音材料, 可用作工业废气脱硫剂。下列化学反应表示正确的是
可用作工业废气脱硫剂。下列化学反应表示正确的是
 的熔点为
的熔点为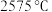 ,熔融时
,熔融时 能导电,而
能导电,而 不能导电;
不能导电; 的燃烧热为
的燃烧热为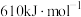 ,实验室中常用酸性
,实验室中常用酸性 测定物品中不溶性
测定物品中不溶性 的含量。铍镍合金可用于制造弹簧秤的弹簧,
的含量。铍镍合金可用于制造弹簧秤的弹簧, 可用作隔音材料,
可用作隔音材料, 可用作工业废气脱硫剂。下列化学反应表示正确的是
可用作工业废气脱硫剂。下列化学反应表示正确的是A. 与 与 溶液反应: 溶液反应: |
B.镁的燃烧:  |
C.向 溶液中滴加足量 溶液中滴加足量 溶液: 溶液: |
D.用酸性 测定 测定 的含量: 的含量: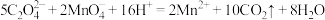 |
您最近一年使用:0次
2024-01-28更新
|
605次组卷
|
3卷引用:2024届江苏省连云港市高三第一次调研考试(一模)化学试题
2024届江苏省连云港市高三第一次调研考试(一模)化学试题河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
4 . 下列化学反应表示正确的是
A.电解饱和NaCl溶液: |
B.钢铁发生吸氧腐蚀的正极反应式: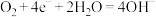 |
C.纯碱溶液呈碱性的原因: |
D.表示氢气燃烧热的热化学方程式: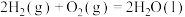  |
您最近一年使用:0次
解题方法
5 . 肼(N2H4)的燃烧热为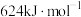 。下列说法正确的是
。下列说法正确的是
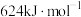 。下列说法正确的是
。下列说法正确的是A. 和 和 中的 中的 键角前者大于后者 键角前者大于后者 |
B. 分子中N原子轨道的杂化方式为 分子中N原子轨道的杂化方式为 |
C. 的沸点低于 的沸点低于 |
D.肼燃烧的热化学方程式为: |
您最近一年使用:0次
解题方法
6 . 下列化学反应的表示不正确的是
A.向硫酸铜中通入过量氨气: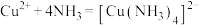 |
B.氨气的燃烧热: 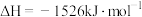 |
C.向稀硝酸中加入过量铁粉: |
D.硫酸铵溶液和氢氧化钡溶液反应: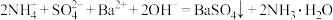 |
您最近一年使用:0次
7 . 单质硼可以溶于热的浓硝酸生成硼酸(H3BO3),硼酸是有重要用途的一元弱酸,能溶于水,可用作防腐剂;硼烷(B2H6,常温下为气态)是一种潜在的高能燃料,在O2中完全燃烧生成B2O3固体和液态水,燃烧热为2165 kJ·mol-1,Al2O3熔点很高,是两性氧化物,可溶于强酸、强碱,下列化学反应表示错误的是
A.硼与热的浓硝酸反应:B+3HNO3  H3BO3+3NO2↑ H3BO3+3NO2↑ |
| B.硼酸与NaOH溶液反应:H++OH- = H2O |
C.Al2O3和NaOH溶液反应:Al2O3+2OH-+3H2O= 2 |
| D.硼烷的燃烧热:B2H6(g)+3O2(g) =B2O3(s)+3H2O(l) ΔH=-2165 kJ·mol-1 |
您最近一年使用:0次
名校
8 .  的燃烧热为
的燃烧热为 。下列化学反应表示正确的是
。下列化学反应表示正确的是
 的燃烧热为
的燃烧热为 。下列化学反应表示正确的是
。下列化学反应表示正确的是A.在空气中煅烧 的反应: 的反应: |
B.在弱碱性条件下,FeS与 反应: 反应: |
C.FeS与 反应的离子方程式: 反应的离子方程式: |
D. 的燃烧: 的燃烧:  |
您最近一年使用:0次
名校
9 . 下列物质热值最大的是
| A.CO:283.4kJ/mol | B.H2:143 kJ/g |
| C.C:33kJ/g | D.CH4:890 kJ/mol |
您最近一年使用:0次
名校
10 . 两份2 mol H2分别与足量的O2充分反应,生成液态水时放出的热量为571.6 kJ、生成水蒸气的反应热为ΔH2。下列说法正确 的是
| A.ΔH2>-571.6 kJ/mol |
| B.用热化学方程式表示氢气的燃烧热为:2H2(g) + O2(g) = 2H2O (l) ΔH1=-571.6 kJ/mol |
| C.2 mol H2(g)和1 mol O2(g)所具有的总能量低于2 mol H2O (l)具有的能量 |
| D.反应2H2(g) + O2(g) = 2H2O (l)的ΔH<0,ΔS>0 |
您最近一年使用:0次
2021-11-17更新
|
937次组卷
|
4卷引用:江苏省连云港市东海县石榴高级中学2023-2024学年高二上学期开学考试化学试题



