1 . ①H2O(l)=H2(g)+ O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是___________ 。(填序号)
(2)H2的燃烧热为___________ 。
(3)燃烧10gH2生成液态水,放出的热量为___________ 。
 O2(g) ΔH=+285.8kJ·mol-1
O2(g) ΔH=+285.8kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110.5kJ·mol-1
O2(g)=CO(g) ΔH=-110.5kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
回答下列问题:
(1)上述反应中属于放热反应的是
(2)H2的燃烧热为
(3)燃烧10gH2生成液态水,放出的热量为
您最近半年使用:0次
2 . 在25℃、101 kPa下,1g液态甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式:___________ 。
您最近半年使用:0次
3 . 下列燃烧热相同的是
| A.1mol C2H4 0.5mol C4H8 | B.2mol正丁烷2mol异丁烷 |
| C.1mol 金刚石12g石墨 | D.3mol乙醇2mol乙醇 |
您最近半年使用:0次
4 . 下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol |
| C.化合反应一定是放热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
您最近半年使用:0次
解题方法
5 . 依据下列热化学方程式得出的结论中,正确的是
A.已知 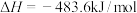 ,则氢气的燃烧热 ,则氢气的燃烧热 为 为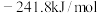 |
B.已知C(石墨,s)= C(金刚石,s)  ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.已知 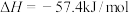 ,则含 ,则含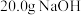 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出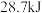 的热量 的热量 |
D.已知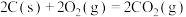  ; ;  ,则 ,则 |
您最近半年使用:0次
解题方法
6 . 研究化学反应中的能量变化具有重要的意义。回答下列问题:
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
①由上述热化学方程式可知甲醇的燃烧热△H=____________ 。
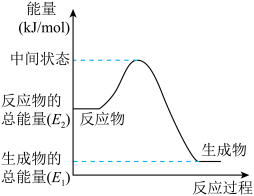
②上述第二个反应的能量变化如图所示,则△H2=___________ k/mol。(用E1、E2的相关式子表示)。.
(2)已知反应N2(g)+3H2(g) 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=________ 。
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是__________ (填化学式)。
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:_____________ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol①由上述热化学方程式可知甲醇的燃烧热△H=
②上述第二个反应的能量变化如图所示,则△H2=

(2)已知反应N2(g)+3H2(g)
 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近半年使用:0次
解题方法
7 . 25℃,1.01×105Pa下,4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,则表示CO燃烧热的热化学方程式为___________ 。
您最近半年使用:0次
8 . 已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)  =﹣2bkJ•mol﹣1 =﹣2bkJ•mol﹣1 |
B.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)  =﹣4bkJ•mol﹣1 =﹣4bkJ•mol﹣1 |
C.C2H2(g)+ O2(g)=2CO2(g)+H2O(l) O2(g)=2CO2(g)+H2O(l)  =+bkJ•mol﹣1 =+bkJ•mol﹣1 |
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)  =﹣4bkJ•mol﹣1 =﹣4bkJ•mol﹣1 |
您最近半年使用:0次
2024-03-12更新
|
78次组卷
|
2卷引用:天津市第八中学2023-2024学年高二上学期第一次大单元教学(9月月考)化学试题
9 . Ⅰ.已知下列热化学方程式:
①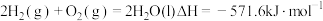
②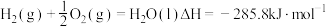
③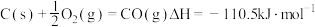
④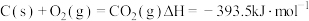
回答下列问题:
(1)上述反应中属于放热反应的是_______ (填序号)。
(2) 的燃烧热为
的燃烧热为_______ 。
(3)写出 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
Ⅱ.室温下,有浓度均为 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。
① ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离平衡常数,醋酸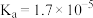 ;碳酸
;碳酸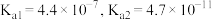 。
。
(4)上述溶液中水的电离被抑制的是_______ (填序号),溶液⑤中溶质与水作用的离子方程式表示为_______ 。
(5)上述②④⑤溶液的 由大到小的顺序为
由大到小的顺序为_______ (填序号)。
(6)比较溶液③和④中 的物质的量浓度:③
的物质的量浓度:③_______ ④(4)(填“<”、“=”或“>”)。
(7)向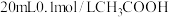 溶液中滴加
溶液中滴加 溶液的过程中,
溶液的过程中, 变化如图所示。
变化如图所示。
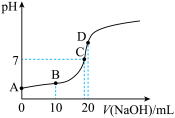
①滴加过程中发生反应的离子方程式是_______ 。
②列说法正确的是_______ 。
a. A、C两点水的电离程度:
b.B点溶液中微粒浓度满足:
c.D点溶液中微粒浓度满足: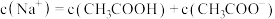
①
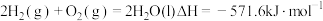
②
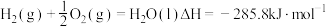
③
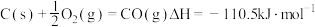
④
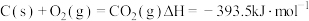
回答下列问题:
(1)上述反应中属于放热反应的是
(2)
 的燃烧热为
的燃烧热为(3)写出
 燃烧热的热化学方程式
燃烧热的热化学方程式Ⅱ.室温下,有浓度均为
 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。①
 ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离平衡常数,醋酸
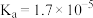 ;碳酸
;碳酸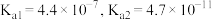 。
。(4)上述溶液中水的电离被抑制的是
(5)上述②④⑤溶液的
 由大到小的顺序为
由大到小的顺序为(6)比较溶液③和④中
 的物质的量浓度:③
的物质的量浓度:③(7)向
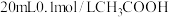 溶液中滴加
溶液中滴加 溶液的过程中,
溶液的过程中, 变化如图所示。
变化如图所示。
①滴加过程中发生反应的离子方程式是
②列说法正确的是
a. A、C两点水的电离程度:

b.B点溶液中微粒浓度满足:

c.D点溶液中微粒浓度满足:
您最近半年使用:0次
10 . 下列有关热化学方程式的叙述正确的是
A.已知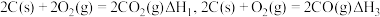 ,则 ,则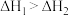 |
B. ,则 ,则 的燃烧热 的燃烧热 |
C.已知正丁烷(g)→异丁烷(g) ,则异丁烷比正丁烷稳定 ,则异丁烷比正丁烷稳定 |
D. 和 和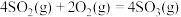 的 的 相等 相等 |
您最近半年使用:0次



