解题方法
1 . 研究化学反应中的能量变化具有重要的意义。回答下列问题:
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
①由上述热化学方程式可知甲醇的燃烧热△H=____________ 。
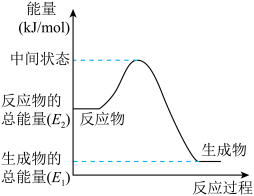
②上述第二个反应的能量变化如图所示,则△H2=___________ k/mol。(用E1、E2的相关式子表示)。.
(2)已知反应N2(g)+3H2(g) 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=________ 。
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是__________ (填化学式)。
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:_____________ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___________ 。
(1)甲醇是人们开发和利用的一种新能源。已知:
2H2(g)+O2(g)=2H2O(1) △H1=-571.8kJ/mol
CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol
O2(g)=CO2(g)+2H2(g) △H2=-192.9kJ/mol①由上述热化学方程式可知甲醇的燃烧热△H=
②上述第二个反应的能量变化如图所示,则△H2=

(2)已知反应N2(g)+3H2(g)
 2NH3(g),试根据表中所列键能数据估算该反应的△H=
2NH3(g),试根据表中所列键能数据估算该反应的△H=| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
(3)1molH2和1molCH4完全燃烧放出的热量分别为286kJ、890kJ,等质量的H2和CH4完全燃烧,放出热量较多的是
(4)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢,当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态过氧化氢反应,生成氮气和水蒸气,放出256kJ的热量。
①写出该反应的热化学方程式:
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
2 . 化学用语可表达化学过程,下列化学用语的表达正确的是
A.用电子云轮廓图表示H—Cl σ键形成的示意图: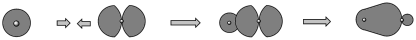 |
B.用热化学方程式表示C的燃烧热: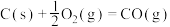 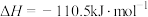 |
C.用化学方程式表示甲醛与苯酚制备线型酚醛树脂: |
D.用电子式表示CaCl2的形成过程: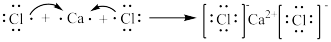 |
您最近一年使用:0次
2024-03-15更新
|
469次组卷
|
3卷引用:天津市北辰区2024届高三下学期高考模拟考试(三模)化学试卷
天津市北辰区2024届高三下学期高考模拟考试(三模)化学试卷2024届湖北省八市高三下学期3月联考化学试卷(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
3 . Ⅰ.已知下列热化学方程式:
①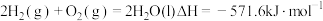
②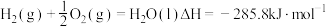
③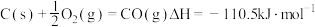
④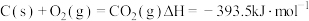
回答下列问题:
(1)上述反应中属于放热反应的是_______ (填序号)。
(2) 的燃烧热为
的燃烧热为_______ 。
(3)写出 燃烧热的热化学方程式
燃烧热的热化学方程式_______ 。
Ⅱ.室温下,有浓度均为 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。
① ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离平衡常数,醋酸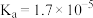 ;碳酸
;碳酸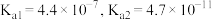 。
。
(4)上述溶液中水的电离被抑制的是_______ (填序号),溶液⑤中溶质与水作用的离子方程式表示为_______ 。
(5)上述②④⑤溶液的 由大到小的顺序为
由大到小的顺序为_______ (填序号)。
(6)比较溶液③和④中 的物质的量浓度:③
的物质的量浓度:③_______ ④(4)(填“<”、“=”或“>”)。
(7)向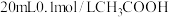 溶液中滴加
溶液中滴加 溶液的过程中,
溶液的过程中, 变化如图所示。
变化如图所示。
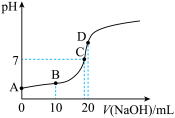
①滴加过程中发生反应的离子方程式是_______ 。
②列说法正确的是_______ 。
a. A、C两点水的电离程度:
b.B点溶液中微粒浓度满足:
c.D点溶液中微粒浓度满足: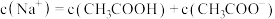
①
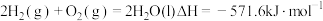
②
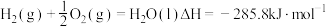
③
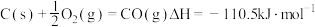
④
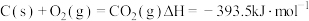
回答下列问题:
(1)上述反应中属于放热反应的是
(2)
 的燃烧热为
的燃烧热为(3)写出
 燃烧热的热化学方程式
燃烧热的热化学方程式Ⅱ.室温下,有浓度均为
 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。①
 ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离平衡常数,醋酸
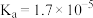 ;碳酸
;碳酸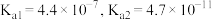 。
。(4)上述溶液中水的电离被抑制的是
(5)上述②④⑤溶液的
 由大到小的顺序为
由大到小的顺序为(6)比较溶液③和④中
 的物质的量浓度:③
的物质的量浓度:③(7)向
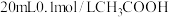 溶液中滴加
溶液中滴加 溶液的过程中,
溶液的过程中, 变化如图所示。
变化如图所示。
①滴加过程中发生反应的离子方程式是
②列说法正确的是
a. A、C两点水的电离程度:

b.B点溶液中微粒浓度满足:

c.D点溶液中微粒浓度满足:
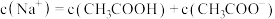
您最近一年使用:0次
名校
解题方法
4 . 下列说法错误的是
| A.明矾和漂白粉用于自来水的净化和杀菌消毒,两者的作用原理不相同 |
B.用 作阴极, 作阴极, 作阳极,可实现在 作阳极,可实现在 上镀 上镀 |
C.在工业废水处理过程中,以 作沉淀剂除去 作沉淀剂除去 、 、 等 等 |
D.由 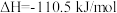 ,可知碳的燃烧热大于 ,可知碳的燃烧热大于 |
您最近一年使用:0次
名校
5 . 下列有关的推论正确的是
A.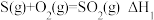 , ,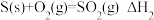 ,则 ,则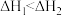 |
B.已知 时,向密闭容器中加入 时,向密闭容器中加入 和 和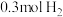 ,达平衡时放出的热量为 ,达平衡时放出的热量为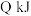 则该反应的热化学方程式为 则该反应的热化学方程式为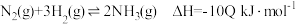 |
C.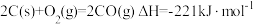 ,则碳的燃烧热的数值小于 ,则碳的燃烧热的数值小于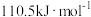 |
D.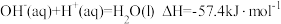 ,则含有 ,则含有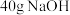 的稀溶液与过量稀醋酸充分反应,最终放出的热量为 的稀溶液与过量稀醋酸充分反应,最终放出的热量为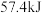 |
您最近一年使用:0次
名校
解题方法
6 . 在 、
、 下,
下,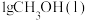 完全燃烧生成稳定氧化物放热
完全燃烧生成稳定氧化物放热 ,下列
,下列 燃烧的热化学方程式正确的是
燃烧的热化学方程式正确的是
 、
、 下,
下,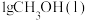 完全燃烧生成稳定氧化物放热
完全燃烧生成稳定氧化物放热 ,下列
,下列 燃烧的热化学方程式正确的是
燃烧的热化学方程式正确的是A.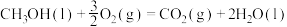 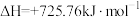 |
B.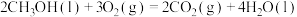 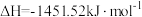 |
C.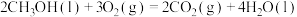 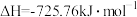 |
D.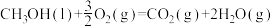 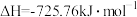 |
您最近一年使用:0次
2024-01-29更新
|
336次组卷
|
9卷引用:天津市第十四中学2021-2022学年高二上学期第一次月考化学试题
天津市第十四中学2021-2022学年高二上学期第一次月考化学试题新疆乌鲁木齐市第二十中学2019-2020学年高二上学期期中考试化学试题安徽省灵璧一中2021-2022学年高二上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期第一次月考化学试题陕西省西安市周至县第四中学2021-2022学年高二上学期期中考试化学(理科)试题陕西省西安中学2023-2024学年高二上学期第一次综合评价化学试题四川省攀枝花市2023-2024学年高二上学期普通高中教学质量监测化学试题江苏省2023-2024学年高一下学期学期3月月考化学试题江苏省新海高级中学2023-2024学年高一下学期第一次月考化学试题
7 . Ⅰ.次磷酸 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。
(1) 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:___________ 。
(2)用电渗析法制备 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
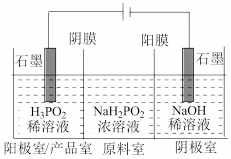
①写出阴极的电极反应:___________ 。
② 的移动方向是:
的移动方向是: 移向
移向___________ (填“阴极室”或“原料室”)。
③阳极室得到 ,
, 的浓度逐渐增大。
的浓度逐渐增大。
a.结合电极反应说明其原因是___________ 。
b.该方法得到的产品 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是___________ 。
Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时, 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,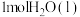 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(4)氢氧燃料电池中氢气在___________ (填“正”或“负”)极发生反应。
(5)在允许 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,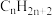 放电的电极反应式为
放电的电极反应式为___________ 。
(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→___________ (用b~j等代号表示)。

 具有较强的还原性,可用于制药工业。
具有较强的还原性,可用于制药工业。(1)
 是一元酸,25℃时,
是一元酸,25℃时, 。写出其电离方程式:
。写出其电离方程式:(2)用电渗析法制备
 的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
的工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。
①写出阴极的电极反应:
②
 的移动方向是:
的移动方向是: 移向
移向③阳极室得到
 ,
, 的浓度逐渐增大。
的浓度逐渐增大。a.结合电极反应说明其原因是
b.该方法得到的产品
 溶液中会混有
溶液中会混有 。产生
。产生 的原因是
的原因是Ⅱ.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(3)298K时,
 燃烧生成
燃烧生成 放热121kJ,
放热121kJ,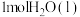 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(4)氢氧燃料电池中氢气在
(5)在允许
 自由迁移的固体电解质燃料电池中,
自由迁移的固体电解质燃料电池中,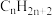 放电的电极反应式为
放电的电极反应式为(6)甲醇燃料电池中,吸附在催化剂表面的甲醇分子逐步脱氢得到CO,四步可能脱氢产物及其相对能量如图,则最可行途径为a→

您最近一年使用:0次
名校
解题方法
8 . 汽车发动机代用燃料包括乙醇、氢气和甲烷等。回答下列问题:
(1)在25℃、 下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量
下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量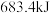 ,则乙醇燃烧热的热化学方程式为
,则乙醇燃烧热的热化学方程式为___________ 。
(2)根据图甲中的能量关系,可求得 键的键能为
键的键能为___________  。
。

(3)甲烷完全燃烧反应的能量关系如图乙所示。

①

___________ (用含 和
和 的关系式表示)。
的关系式表示)。
②为提高燃料利用率,加入甲烷燃烧的催化剂,则
___________ (填“变大”、“变小”或“不变”,下同),该反应的
___________ 。
(4)已知氢气的燃烧热为 ,甲烷的燃烧热为
,甲烷的燃烧热为 ,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点:
,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点:___________ 。
(5)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:___________ 。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是___________ ,元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
(1)在25℃、
 下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量
下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量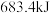 ,则乙醇燃烧热的热化学方程式为
,则乙醇燃烧热的热化学方程式为(2)根据图甲中的能量关系,可求得
 键的键能为
键的键能为 。
。
(3)甲烷完全燃烧反应的能量关系如图乙所示。

①


 和
和 的关系式表示)。
的关系式表示)。②为提高燃料利用率,加入甲烷燃烧的催化剂,则


(4)已知氢气的燃烧热为
 ,甲烷的燃烧热为
,甲烷的燃烧热为 ,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点:
,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点:(5)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是
您最近一年使用:0次
名校
解题方法
9 . 下列依据热化学方程式得出的结论正确的是
A.已知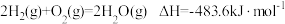 ;则氢气的燃烧热为 ;则氢气的燃烧热为 |
B.已知 ;则金刚石比石墨稳定 ;则金刚石比石墨稳定 |
C.已知 ;则含 ;则含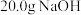 的稀溶液与稀盐酸完全中和,放出 的稀溶液与稀盐酸完全中和,放出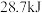 的热量 的热量 |
D.已知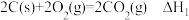 , ,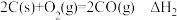 ;则 ;则 |
您最近一年使用:0次
2024-01-09更新
|
234次组卷
|
37卷引用:天津市南蔡村中学2023-2024学年高二上学期第二次月考化学试卷
天津市南蔡村中学2023-2024学年高二上学期第二次月考化学试卷(已下线)2015届广西桂林市第十八中学高三上学期第二次月考化学试卷河北省深州中学2016-2017学年高一下学期期末考试化学试题安徽省定远县第三中学2018-2019学年度下学期高二化学开学检测卷【全国百强校】内蒙古自治区鄂尔多斯市第一中学2018-2019学年高一下学期期中考试化学试题山西省朔州市怀仁一中2018-2019学年高二上学期第三次月考化学试题山西省朔州市怀仁县第一中学2018-2019学年高二上学期期中考试化学试题江苏省南菁高级中学2020-2021学年度高二上学期第一次阶段性考试化学(强化班)试题内蒙古鄂尔多斯市第一中学2020-2021学年高一下学期第三次月考化学试题北京市第三十一中学2021-2022学年高二上学期期中考试化学试题黑龙江省双鸭山市第一中学2022-2023学年高二10月月考化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题河南省郑州外国语学校2022-2023学年高二上学期期中考试化学试题北京市顺义牛栏山第一中学2022-2023学年高二上学期10月月考化学试题河南省郑州外国语学校2022-2023学年高二上学期期中考试化学试题湖南省永州市宁远县明德湘南中学2022-2023学年高二上学期第一次月考化学试题黑龙江省肇东市第四中学2022-2023学年高二上学期期末考试化学试题湖南省长沙市第一中学2022-2023学年高二下学期入学考试化学试题 河南省南阳市2022-2023学年高二上学期期终质量评估化学试题广东番禺中学2022-2023学年高二上学期期末测试化学试题广东省佛山市实验中学2022-2023学年高二上学期第一次段考化学试题辽宁省名校联盟2023-2024学年高二上学期期初考试化学试题辽宁省锦州市黑山县名校联盟试2023-2024学年高二上学期开学考试化学试题四川省南充高级中学2023-2024学年高二上学期10月月考化学试题江西省九江市庐山市第一中学2022-2023学年高二上学期期末考试化学试题广东省湛江市第二十一中学2023-2024学年高二10月月考化学试题黑龙江省鹤岗市第三中学2023-2024学年高二上学期10月月考化学试题辽宁省辽西联合校2023-2024学年高二上学期期中考试化学试题福建省厦门市松柏中学2023-2024学年高二上学期10月月考化学试题黑龙江省齐齐哈尔市恒昌中学校2023-2024学年高二上学期期中考试化学试题四川省绵竹中学2023-2024学年高二上学期第二次月考化学试题广东省广州市真光中学2023-2024学年高二上学期12月月考化学试题四川省阆中东风中学校2023-2024学年高二上学期第二次段考化学试题四川省绵阳南山中学实验学校2023-2024学年高二上学期12月月考化学试题广东省江门市鹤山市第一中学2023-2024学年高二上学期第二阶段考试化学试题山东省威海大光华学校2023-2024学年高二11月月考化学试题广东省梅州市梅雁中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . 填空
(1)在 、101kPa下,
、101kPa下, 的液态甲醇
的液态甲醇 在空气中完全燃烧生成
在空气中完全燃烧生成 气体和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为
气体和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为________________ 。
(2) 、101kPa下,稀强酸与稀强碱溶液反应生成1mol水放出热量
、101kPa下,稀强酸与稀强碱溶液反应生成1mol水放出热量 。写出表示稀
。写出表示稀 与稀烧碱溶液反应的中和热的热化学方程式:
与稀烧碱溶液反应的中和热的热化学方程式:___________________ 。
(3)学生甲用 硫酸与
硫酸与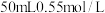 烧碱溶液测定中和反应反应热的装置如图。
烧碱溶液测定中和反应反应热的装置如图。
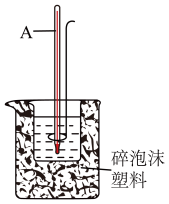
①该装置中仪器A的名称:____________ 。
②该装置中有一处错误是:_____________ 。如果用该错误装置测定,测得该反应的反应热 会
会_______  填“偏大、偏小、无影响”
填“偏大、偏小、无影响” 。
。
③如果用 硫酸与
硫酸与 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热_________  填“相等、不相等”
填“相等、不相等” 。
。
④若反应前溶液以及中和后的混合液的密度均设为 ,混合前酸与碱的温度均为
,混合前酸与碱的温度均为 ,混合后溶液的温度为
,混合后溶液的温度为 ,比热容为
,比热容为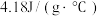 ,则该中和反应生成1mol水的反应热
,则该中和反应生成1mol水的反应热
______________ 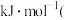 用含
用含 、
、 表达式表达
表达式表达 。
。
(4)学生乙用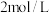 的硫酸来测定与锌粒和锌粉(Zn足量)反应的快慢,设计如图装置:
的硫酸来测定与锌粒和锌粉(Zn足量)反应的快慢,设计如图装置:
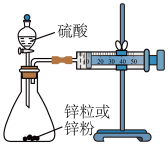
①该生两次实验测定时间均设定为 ,则他还要测定的另一个数据是:
,则他还要测定的另一个数据是:________________ 。
②若要减小产生 的速率而又不影响产生
的速率而又不影响产生 的总量,应向硫酸中加入
的总量,应向硫酸中加入__________  填字母
填字母
 溶液
溶液 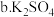 溶液
溶液  溶液
溶液 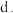 水
水 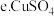 溶液
溶液
(1)在
 、101kPa下,
、101kPa下, 的液态甲醇
的液态甲醇 在空气中完全燃烧生成
在空气中完全燃烧生成 气体和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为
气体和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为(2)
 、101kPa下,稀强酸与稀强碱溶液反应生成1mol水放出热量
、101kPa下,稀强酸与稀强碱溶液反应生成1mol水放出热量 。写出表示稀
。写出表示稀 与稀烧碱溶液反应的中和热的热化学方程式:
与稀烧碱溶液反应的中和热的热化学方程式:(3)学生甲用
 硫酸与
硫酸与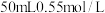 烧碱溶液测定中和反应反应热的装置如图。
烧碱溶液测定中和反应反应热的装置如图。
①该装置中仪器A的名称:
②该装置中有一处错误是:
 会
会 填“偏大、偏小、无影响”
填“偏大、偏小、无影响” 。
。③如果用
 硫酸与
硫酸与 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热 填“相等、不相等”
填“相等、不相等” 。
。④若反应前溶液以及中和后的混合液的密度均设为
 ,混合前酸与碱的温度均为
,混合前酸与碱的温度均为 ,混合后溶液的温度为
,混合后溶液的温度为 ,比热容为
,比热容为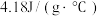 ,则该中和反应生成1mol水的反应热
,则该中和反应生成1mol水的反应热
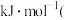 用含
用含 、
、 表达式表达
表达式表达 。
。(4)学生乙用
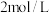 的硫酸来测定与锌粒和锌粉(Zn足量)反应的快慢,设计如图装置:
的硫酸来测定与锌粒和锌粉(Zn足量)反应的快慢,设计如图装置:
①该生两次实验测定时间均设定为
 ,则他还要测定的另一个数据是:
,则他还要测定的另一个数据是:②若要减小产生
 的速率而又不影响产生
的速率而又不影响产生 的总量,应向硫酸中加入
的总量,应向硫酸中加入 填字母
填字母
 溶液
溶液 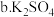 溶液
溶液  溶液
溶液 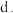 水
水 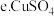 溶液
溶液
您最近一年使用:0次



