名校
1 . 已知反应:①

②

相关化学键的键能数据如下:
下列说法正确的是


②


相关化学键的键能数据如下:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ/mol) | a | b | c | d |
| A.①中反应物的总能量小于生成物的总能量 |
B. |
C. |
D.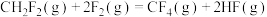 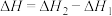 |
您最近一年使用:0次
2023-01-05更新
|
437次组卷
|
11卷引用:北京市密云区第二中学2023-2024学年高二上学期期中(选考)化学试卷
北京市密云区第二中学2023-2024学年高二上学期期中(选考)化学试卷 北京市东城区2022-2023学年高二上学期期末统一检测化学试卷 北京市第一七一中学2023-2024学年高二上学期10月月考化学试题北京市海淀区2023-2024学年高二上学期期中考试化学试题福建省南平市高级中学2023-2024学年高二上学期期中考试化学试题北京市第五十五中学2023-2024学年高二上学期12月月考调研化学试题北京市第三十五中学2023-2024学年高二上学期期中考试化学试题 北京市第三中学2023-2024学年高二上学期期中练习化学试题北京市第十三中学2023-2024学年高二上学期期中考试化学试题北京市2023-2024学年北京三中高二(上)期中化学试卷 云南省开远市第一中学校2023-2024学年高二上学期12月月考化学试题
2 . 2NO(g) + O2(g) 2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
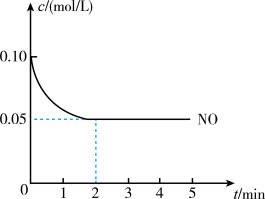
请回答:
(1)2 min内,v(O2) =_______ mol/(L·min)。
(2)800℃时,该反应的化学平衡常数数值为_______ 。
(3)平衡时,NO的转化率是_______ 。
(4)下列能说明反应达平衡状态的是_______(填字母)。
(5)NO会造成大气污染,在工业上采用多种方法进行处理。
氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如下:
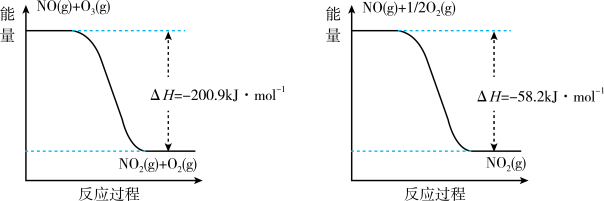
①请写出反应过程Ⅰ的热化学方程式_______ 。
②反应3NO(g) + O3(g)=3NO2(g) ΔH=_______ kJ•mol-1
③用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为_______ 。
 2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
请回答:
(1)2 min内,v(O2) =
(2)800℃时,该反应的化学平衡常数数值为
(3)平衡时,NO的转化率是
(4)下列能说明反应达平衡状态的是_______(填字母)。
| A.单位时间内生成a mol O2的同时生成2a mol NO2 |
| B.混合气体的颜色不再改变 |
| C.混合气体的密度不再改变 |
| D.混合气体的平均相对分子质量不再改变 |
氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如下:

①请写出反应过程Ⅰ的热化学方程式
②反应3NO(g) + O3(g)=3NO2(g) ΔH=
③用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为
您最近一年使用:0次
解题方法
3 . 煤的综合利用是合理利用资源,实现“绿色发展”的重要途径。图是某煤化工产业链的一部分
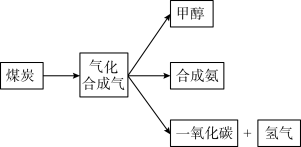
(1)已知:
a. C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
b. 2H2(g)+O2(g)=2H2O(g) ΔH=-484.0 kJ·mol-1
c. CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
①计算反应a消耗24 g C(s)时,反应放出的热量为_______ kJ。
②为加快水煤气(CO和H2混合气)的生产速率可采取措施有_______ 。
A. 将煤炭粉碎 B. 降低温度 C. 增大反应容器体积 D. 使用催化剂
③根据已知,写出 C(s)与H2O(g)反应制备水煤气的热化学方程式是_______ 。
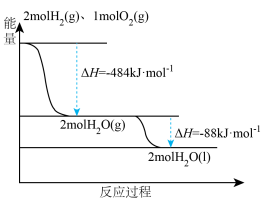
(2)煤气化后得到气体中的氢气是一种新型的绿色能源,根据如图,写出表示氢气燃烧热的热化学方程式为_______
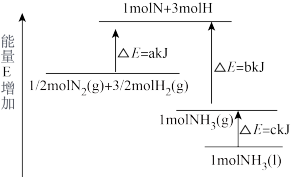
(3)工业合成氨用途广泛,其能量变化如图所示,根据图示,写出合成N2(g)和H2(g)合成液态氨的热化学方程式_______ 。

(1)已知:
a. C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
b. 2H2(g)+O2(g)=2H2O(g) ΔH=-484.0 kJ·mol-1
c. CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1①计算反应a消耗24 g C(s)时,反应放出的热量为
②为加快水煤气(CO和H2混合气)的生产速率可采取措施有
A. 将煤炭粉碎 B. 降低温度 C. 增大反应容器体积 D. 使用催化剂
③根据已知,写出 C(s)与H2O(g)反应制备水煤气的热化学方程式是
(2)煤气化后得到气体中的氢气是一种新型的绿色能源,根据如图,写出表示氢气燃烧热的热化学方程式为

(3)工业合成氨用途广泛,其能量变化如图所示,根据图示,写出合成N2(g)和H2(g)合成液态氨的热化学方程式

您最近一年使用:0次



