2NO(g) + O2(g) 2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
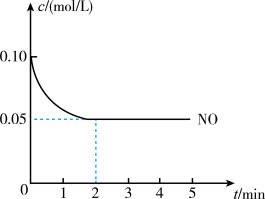
请回答:
(1)2 min内,v(O2) =_______ mol/(L·min)。
(2)800℃时,该反应的化学平衡常数数值为_______ 。
(3)平衡时,NO的转化率是_______ 。
(4)下列能说明反应达平衡状态的是_______(填字母)。
(5)NO会造成大气污染,在工业上采用多种方法进行处理。
氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如下:
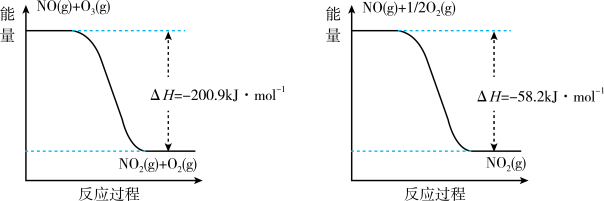
①请写出反应过程Ⅰ的热化学方程式_______ 。
②反应3NO(g) + O3(g)=3NO2(g) ΔH=_______ kJ•mol-1
③用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为_______ 。
 2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
2NO2(g) ∆H<0是制造硝酸的重要反应之一,在800℃时,向容积为2 L的密闭容器中充入0.20 mol NO和0.1 mol O2,反应过程中NO的浓度从随时间变化如图所示,
请回答:
(1)2 min内,v(O2) =
(2)800℃时,该反应的化学平衡常数数值为
(3)平衡时,NO的转化率是
(4)下列能说明反应达平衡状态的是_______(填字母)。
| A.单位时间内生成a mol O2的同时生成2a mol NO2 |
| B.混合气体的颜色不再改变 |
| C.混合气体的密度不再改变 |
| D.混合气体的平均相对分子质量不再改变 |
氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知NO与O3反应过程的能量变化如下:

①请写出反应过程Ⅰ的热化学方程式
②反应3NO(g) + O3(g)=3NO2(g) ΔH=
③用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为
更新时间:2022-10-26 11:32:40
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
I.脱硝:已知:H2的热值为142.9 kJ/g(热值是表示单位质量燃料完全燃烧时所放出的热量);
N2(g) + 2O2(g)==2NO2(g) △H= +133 kJ/mol
H2O(g)==H2O(l) △H=- 44 kJ/mol
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式__________________ 。
Ⅱ.脱碳:向2L密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应CO2(g)+3H2(g) CH3OH(l) + H2O(l)。
CH3OH(l) + H2O(l)。
(1)①该反应自发进行的条件是_________________ (填“低温”“高温”或“任意温度”)。②下列叙述能说明此反应达到平衡状态的是________________________ 。
a.混合气体的平均式量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
(2)改变温度,使反应CO2(g)+3H2(g) CH3OH(g) + H2O(g) △H<0中的所有物质都为气态。起始温度体积相同(T1℃、2L.密闭容器)。反应过程中部分数据见下表:
CH3OH(g) + H2O(g) △H<0中的所有物质都为气态。起始温度体积相同(T1℃、2L.密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应I、II对比:平衡常数K( I )______ K(II)(填“>”“<”或“=”,下同);平衡时CH3OH的浓度c(I)_______ c(II)。
②对反应I,前10 min内的平均反应速率v(CH3OH) =________ ,在其他条件不变下,若30 min时只改变温度为T2℃,此时H2的物质的量为3.2 mol,则T1_____ T2(填填“>”“<”或“=”)。若30 min时只向容器中再充入1 mol CO2(g)和1mol H2O(g),则平衡______ 移动(填“正向”、“逆向”或“不”)。
I.脱硝:已知:H2的热值为142.9 kJ/g(热值是表示单位质量燃料完全燃烧时所放出的热量);
N2(g) + 2O2(g)==2NO2(g) △H= +133 kJ/mol
H2O(g)==H2O(l) △H=- 44 kJ/mol
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式
Ⅱ.脱碳:向2L密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应CO2(g)+3H2(g)
 CH3OH(l) + H2O(l)。
CH3OH(l) + H2O(l)。(1)①该反应自发进行的条件是
a.混合气体的平均式量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
(2)改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g) + H2O(g) △H<0中的所有物质都为气态。起始温度体积相同(T1℃、2L.密闭容器)。反应过程中部分数据见下表:
CH3OH(g) + H2O(g) △H<0中的所有物质都为气态。起始温度体积相同(T1℃、2L.密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2 (mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
| 反应II绝热恒容 | 0 min | 0 | 0 | 2 | 2 |
①达到平衡时,反应I、II对比:平衡常数K( I )
②对反应I,前10 min内的平均反应速率v(CH3OH) =
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲醇是应用广泛的化工原料和前景乐观的无色液体燃料。请按要求回答下列问题。
(1)已知25℃、101 kpa时一些物质的燃烧热如下表:
写出由CO和H2反应生成CH3OH(l)的热化学方程式: _________________________ 。
(2)一定温度下,在容积为2L的恒容密闭容器中进行反应:CO(g)+2H2(g)=CH3OH(g),其相关数据如图所示。
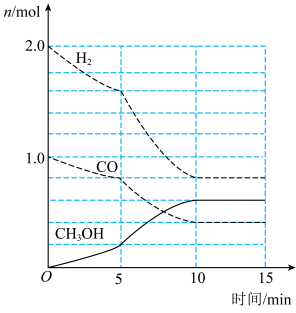
①从反应开始至5min时,用CH3OH表示的反应平均速度为____________ 。
②图中反应达平衡时,K=_______ (mol/L)-2;CO的平衡转化率为________________ 。
(3)人们利用甲醇制得能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,该装置工作时,a极反应式为____________________ 。
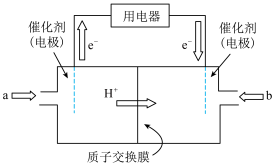
若用该电池及惰性电极电解2L饱和食盐水产生224mL(标准误差2)Cl2时(假设全部句逸出并收集,忽略溶液体积的变化),常温下所得溶液的pH为________ 。
(4)甲醇在一定条件下可转化为甲酸。常温下,向0.1mol/L HCOOH溶液中滴加0.1mol/LNaOH溶液至pH=7[已知,K(HCOOH)=1.8×10-4]。此时混合溶液中两溶质的物质的量之比n(HCOOH):n(HCOONa)____________ 。
(1)已知25℃、101 kpa时一些物质的燃烧热如下表:
| 物质 | CH3OH(l) | CO(g) | H2(g) |
| 燃烧热/(kJ/mol) | 726.8 | 283.0 | 285.8 |
(2)一定温度下,在容积为2L的恒容密闭容器中进行反应:CO(g)+2H2(g)=CH3OH(g),其相关数据如图所示。

①从反应开始至5min时,用CH3OH表示的反应平均速度为
②图中反应达平衡时,K=
(3)人们利用甲醇制得能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,该装置工作时,a极反应式为

若用该电池及惰性电极电解2L饱和食盐水产生224mL(标准误差2)Cl2时(假设全部句逸出并收集,忽略溶液体积的变化),常温下所得溶液的pH为
(4)甲醇在一定条件下可转化为甲酸。常温下,向0.1mol/L HCOOH溶液中滴加0.1mol/LNaOH溶液至pH=7[已知,K(HCOOH)=1.8×10-4]。此时混合溶液中两溶质的物质的量之比n(HCOOH):n(HCOONa)
您最近一年使用:0次
【推荐3】李克强总理在《2018年国务院政府工作报告》中强调“今年二氧化硫、氮氧化物排放量要下降3%。”研究烟气的脱硝(除NOx)、脱硫(除SO2)有着积极的环保意义。
Ⅰ.汽车排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g) 2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。

(1)图中a、b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是___ (填“a”或“b”)。
(2)在a曲线所示反应中,0~10min内,CO的平均反应速率v(CO)=____ ;T℃时,该反应的化学平衡常数K=___ ;平衡时若保持温度不变,再向容器中充入CO、CO2各0.2mol,则平衡将移动____ (填“向左”、“向右”或“不”)。
(3)15min时,n(NO)发生图中所示变化,则改变的条件可能是___ (填序号)
A.充入少量CO B.将N2液化移出体系 C.升高温度 D.加入催化剂
(4)Ⅱ.已知有下列反应:
①5O2(g)+4NH3(g) 6H2O(g)+4NO(g)△H1
6H2O(g)+4NO(g)△H1
②N2(g)+O2(g) 2NO(g)△H2
2NO(g)△H2
③2NO(g)+O2(g) 2NO2(g)△H3
2NO2(g)△H3
若在高效催化剂作用下可发生8NH3(g)+6NO2(g) 7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=
7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=___ (用△H1,△H2,△H3表示),△S___ 0。
(5)某温度下,向某恒容密闭容器中充入一定量的NH3和NO2,按照(4)的原理模拟污染物的处理。若容器中观察到___ (填序号),可判断该反应达到平衡状态。
A.混合气体颜色不再改变
B.混合气体的密度不再改变
C.混合气体平均相对分子质量不再改变
D.NH3和NO2的物质的量之比不再改变
Ⅰ.汽车排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g)
 2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
2CO2(g)+N2(g)ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min)NO的物质的量随时间变化如图。
(1)图中a、b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是
(2)在a曲线所示反应中,0~10min内,CO的平均反应速率v(CO)=
(3)15min时,n(NO)发生图中所示变化,则改变的条件可能是
A.充入少量CO B.将N2液化移出体系 C.升高温度 D.加入催化剂
(4)Ⅱ.已知有下列反应:
①5O2(g)+4NH3(g)
 6H2O(g)+4NO(g)△H1
6H2O(g)+4NO(g)△H1②N2(g)+O2(g)
 2NO(g)△H2
2NO(g)△H2③2NO(g)+O2(g)
 2NO2(g)△H3
2NO2(g)△H3若在高效催化剂作用下可发生8NH3(g)+6NO2(g)
 7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=
7N2(g)+ 12H2O(g)的反应,对NO2进行处理则该反应的△H=(5)某温度下,向某恒容密闭容器中充入一定量的NH3和NO2,按照(4)的原理模拟污染物的处理。若容器中观察到
A.混合气体颜色不再改变
B.混合气体的密度不再改变
C.混合气体平均相对分子质量不再改变
D.NH3和NO2的物质的量之比不再改变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】I.在恒温2L密闭容器中通入气体X并发生放热反应:2X(g) Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)
Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)______ 。
(2)图中c点对应的速率关系是v(正)______ v(逆)(填“>”或“<”或“=”);b曲线与a比改变的条件是______ 。
(3)反应进行到a点时放出的热量______ 反应进行到b点时放出的热量(填“>”或“<”或“=”)。
II.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。______ (计算保留2位有效数字)。
(5)能说明上述反应达到平衡状态的是______ (填字母)。
(6)平衡时CH3OH的体积分数为______ 。平衡混合气体中CO2(g)和H2(g)的质量之比是______ 。
(7)第3分钟时v正(CH3OH)______ 第9分钟时v逆(CH3OH)(填“>”“<”“=”或“无法比较”)。
III.在恒温条件下将一定量X和Y的混合气体通入容积为2L的密闭容器中,X和Y两物质的浓度随时间的变化情况如图所示。______ 。
(9)a、b、c、d四个点中,表示化学反应处于平衡状态的点是______ 。
 Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)
Y(g),X的物质的量n(x)随时间t变化的曲线如图所示(图中两曲线分别代表有无使用催化剂的情形)
| A.升高温度 | B.加入适量X |
| C.增大压强 | D.及时分离出Y |
(2)图中c点对应的速率关系是v(正)
(3)反应进行到a点时放出的热量
II.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。CO2可转化成有机物实现碳循环。在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(5)能说明上述反应达到平衡状态的是
| A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点) |
| B.混合气体的压强不随时间的变化而变化 |
| C.单位时间内生成1molH2,同时生成1molCH3OH |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
(6)平衡时CH3OH的体积分数为
(7)第3分钟时v正(CH3OH)
III.在恒温条件下将一定量X和Y的混合气体通入容积为2L的密闭容器中,X和Y两物质的浓度随时间的变化情况如图所示。

(9)a、b、c、d四个点中,表示化学反应处于平衡状态的点是
您最近一年使用:0次
【推荐2】CH4超干重整CO2技术可得到富含CO的化工原料。回答下列问题:
(1)CH4超干重整CO2的催化转化如图所示:

①已知相关反应的能量变化如图所示:
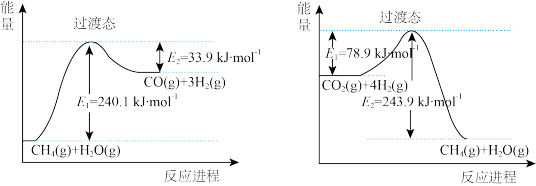
过程I的热化学方程式为____ 。
②关于上述过程II的说法正确的是____ (填序号)。
a.实现了含碳物质与含氢物质的分离 b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应 d.Fe3O4、CaO为催化剂,降低了反应的△H
③其他条件不变,在不同催化剂(I、II、III)作用下,反应CH4(g)+CO2(g)=2CO(g)+2H2(g)进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态____ (填“是”或“不是”)平衡状态;b点CH4的转化率高于c点,原因是____ 。
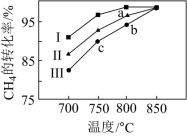
(2)在一刚性密闭容器中,CH4和CO2的分压分别为20kPa、25kPa,加入Ni/α-A12O3催化剂并加热至1123K使其发生反应CH4(g)+CO2(g)=2CO(g)+2H2(g)。
①研究表明CO的生成速率v(CO)=1.3×10-2•p(CH4)•p(CO2)mol•g-1•s-1,某时刻测得p(CO)=20kPa,则p(CO2)=_____ kPa,v(CO)=_____ mol•g-1•s-1。
②达到平衡后测得体系压强是起始时的1.8倍,则该反应的平衡常数的计算式为:Kp=____ (kPa)2。(用各物质的分压代替物质的量浓度计算)。
(1)CH4超干重整CO2的催化转化如图所示:

①已知相关反应的能量变化如图所示:

过程I的热化学方程式为
②关于上述过程II的说法正确的是
a.实现了含碳物质与含氢物质的分离 b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应 d.Fe3O4、CaO为催化剂,降低了反应的△H
③其他条件不变,在不同催化剂(I、II、III)作用下,反应CH4(g)+CO2(g)=2CO(g)+2H2(g)进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态

(2)在一刚性密闭容器中,CH4和CO2的分压分别为20kPa、25kPa,加入Ni/α-A12O3催化剂并加热至1123K使其发生反应CH4(g)+CO2(g)=2CO(g)+2H2(g)。
①研究表明CO的生成速率v(CO)=1.3×10-2•p(CH4)•p(CO2)mol•g-1•s-1,某时刻测得p(CO)=20kPa,则p(CO2)=
②达到平衡后测得体系压强是起始时的1.8倍,则该反应的平衡常数的计算式为:Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】合成氨是人类科技发展史上的一项重大突破。
(1)在一定条件下,N2(g)和H2(g)反应生成0.2 molNH3(g),放出9.24kJ的热量。在下图中画出合成氨反应中用焓(H)变表示反应热的示意图________ 。

(2)将N2和H2通入体积为2L的恒温恒容密闭容器中,5min后达到化学平衡,测得NH3的浓度为0.2mol/L,这段时间内用N2的浓度变化表示的化学反应速率为______________ mol/(L.min)。
(3)理论上,为了增大平衡时H2的转化率,可采取的措施是______________ (写出一条)。
(4)下图是某压强下N2和H2按物质的量之比1:3投料进行反应,反应混合物中NH3的物质的量分数随温度的变化曲线。I是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是______________ 。

a.图中a点,容器内n(N2):n(NH3)=1:4
b.图中b点,v正<v逆
c.400~530℃,Ⅱ中NH3的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
(1)在一定条件下,N2(g)和H2(g)反应生成0.2 molNH3(g),放出9.24kJ的热量。在下图中画出合成氨反应中用焓(H)变表示反应热的示意图

(2)将N2和H2通入体积为2L的恒温恒容密闭容器中,5min后达到化学平衡,测得NH3的浓度为0.2mol/L,这段时间内用N2的浓度变化表示的化学反应速率为
(3)理论上,为了增大平衡时H2的转化率,可采取的措施是
(4)下图是某压强下N2和H2按物质的量之比1:3投料进行反应,反应混合物中NH3的物质的量分数随温度的变化曲线。I是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是

a.图中a点,容器内n(N2):n(NH3)=1:4
b.图中b点,v正<v逆
c.400~530℃,Ⅱ中NH3的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】乙酸乙酯在工业上有着广泛的用途。科学家以乙烯、乙酸为原料,杂多酸作催化剂制备乙酸乙酯,反应原理为 。回答下列问题:
。回答下列问题:
(1)在热力学标态下由指定单质(大多是稳定单质)生成1 mol物质的反应焓变,称为该物质的标准摩尔生成焓( )。。相关物质的标准摩尔生成焓数据如表所示。
)。。相关物质的标准摩尔生成焓数据如表所示。
以乙烯(g)、乙酸(g)为原料制备乙酸乙酯(1)的反应的热化学方程式为___________ 。
(2)一定条件下,在一个密闭容器中,通入各1 mol的乙烯和乙酸气体,发生上述反应。
①若保持温度和压强不变,下列描述能说明反应已达化学平衡的是___________ (填字母)。
A.单位时间内,消耗乙烯和生成乙酸的物质的量相同
B.容器内混合气体的密度不再变化
C. 不再变化
不再变化
D.体系中乙烯和乙酸的转化率相等
②若想提高乙酸乙酯的产率,可以采取的措施有___________ (写两种)。
③分别在压强 、
、 下,相同时间内测得乙酸乙酯的产率随温度的变化如图。
下,相同时间内测得乙酸乙酯的产率随温度的变化如图。


___________  (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。A点后乙酸乙酯产率随温度升高反而下降的原因可能是___________ 。A点该反应的压强平衡常数
___________ (用含 的代数式表示)。
的代数式表示)。
(3)科学家设想通过电化学方法实现乙烯的转化,其原理如图所示(均为惰性电极)。图中b极为___________ 极,M极上的电极反应式为___________ 。

 。回答下列问题:
。回答下列问题:(1)在热力学标态下由指定单质(大多是稳定单质)生成1 mol物质的反应焓变,称为该物质的标准摩尔生成焓(
 )。。相关物质的标准摩尔生成焓数据如表所示。
)。。相关物质的标准摩尔生成焓数据如表所示。| 物质 | 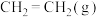 | 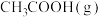 |  |
 /(kJ·mol /(kJ·mol ) ) | +52.3 | -436.4 | -463.2 |
(2)一定条件下,在一个密闭容器中,通入各1 mol的乙烯和乙酸气体,发生上述反应。
①若保持温度和压强不变,下列描述能说明反应已达化学平衡的是
A.单位时间内,消耗乙烯和生成乙酸的物质的量相同
B.容器内混合气体的密度不再变化
C.
 不再变化
不再变化D.体系中乙烯和乙酸的转化率相等
②若想提高乙酸乙酯的产率,可以采取的措施有
③分别在压强
 、
、 下,相同时间内测得乙酸乙酯的产率随温度的变化如图。
下,相同时间内测得乙酸乙酯的产率随温度的变化如图。

 (填“>”或“<”),理由是
(填“>”或“<”),理由是
 的代数式表示)。
的代数式表示)。(3)科学家设想通过电化学方法实现乙烯的转化,其原理如图所示(均为惰性电极)。图中b极为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) ⇌2NO(g) ΔH>0,已知该反应在2404℃,平衡常数K=6.4×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为_______ ,N2的转化率是_______ 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是_______。
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下图变化趋势正确的是_______ (填字母序号)。
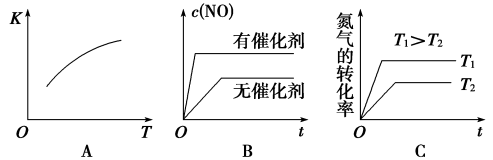
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数_______ (填“变大”、“变小”或“不变”)
(5)高炉炼铁发生的反应有:Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g) ΔH < 0,该反应平衡常数的表达式K=_______ 。
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是_______。
| A.消耗1molN2同时生成1molO2 |
| B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 |
| D.2v正(N2)=v逆(NO) |

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)高炉炼铁发生的反应有:Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g) ΔH < 0,该反应平衡常数的表达式K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】I.我国提出争取在2060年实现碳中和,这对于改善环境、实现绿色发展至关重要。“碳中和”是指CO2的排放总量和减少总量相当。工业上有一种方法是利用CO2生产甲醇(CH3OH):CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:
CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:

(1)该反应是_____ (填“放热”或“吸热”)反应,若有1molCO2(g)参加反应,则变化的能量是_____ kJ。
(2)一定条件下,将2molCO2和6molH2在2L恒容密闭容器中发生上述反应,经过2min反应达到了平衡,此时CH3OH浓度为0.8mol/L。
①2min内用CO2表示该反应的速率为v(CO2)=_____ 。
②平衡时体系内气体压强与开始时的压强之比为_____ 。
③一定能说明该反应达到平衡的标志是_____ 。
A.CO2和CH3OH的物质的量浓度相等
B.CO2和CH3OH物质的量浓度的比值不变
C.混合气体的平均摩尔质量不再改变
D.混合气体的密度保持不变
E.2v(CO2)=v(H2O)
F.单位时间内3molH-H键断裂,同时水中有2molO-H键断裂
Ⅱ.有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。

(3)a电极上的电极反应式是______ 。
(4)该电池在工作过程中溶液的pH值不断_____ (填“增大”或“减小”),假设放电过程中电解质溶液的体积不变,当溶液中 的物质的量改变0.8mol时,理论上电池能为外电路提供
的物质的量改变0.8mol时,理论上电池能为外电路提供_____ mol电子。
 CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:
CH3OH(g)+H2O(g),该反应过程中的能量变化如图所示:
(1)该反应是
(2)一定条件下,将2molCO2和6molH2在2L恒容密闭容器中发生上述反应,经过2min反应达到了平衡,此时CH3OH浓度为0.8mol/L。
①2min内用CO2表示该反应的速率为v(CO2)=
②平衡时体系内气体压强与开始时的压强之比为
③一定能说明该反应达到平衡的标志是
A.CO2和CH3OH的物质的量浓度相等
B.CO2和CH3OH物质的量浓度的比值不变
C.混合气体的平均摩尔质量不再改变
D.混合气体的密度保持不变
E.2v(CO2)=v(H2O)
F.单位时间内3molH-H键断裂,同时水中有2molO-H键断裂
Ⅱ.有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。

(3)a电极上的电极反应式是
(4)该电池在工作过程中溶液的pH值不断
 的物质的量改变0.8mol时,理论上电池能为外电路提供
的物质的量改变0.8mol时,理论上电池能为外电路提供
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】我国向国际社会承诺,2023年买现“碳达峰”,2060年实现“碳中和”。已知500℃时,在2L恒容密闭容器中充入2mol  和6mol
和6mol  ,发生反应:
,发生反应: ,∆H=-49kJ/mol平衡时体系压强为
,∆H=-49kJ/mol平衡时体系压强为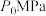 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
_______ mol/(L∙min)。 H2和CO2转化率关系_______ (相等、不相等),15分钟后平衡,平衡时H2的转化率为_______ 。
(2)下列能说明该反应已达到平衡状态的是_________ 。
A.气体的密度不再变化
B.容器内气体的压强不再变化
C.
D. 、
、 、
、 和
和 浓度之比为1:3:1:1
浓度之比为1:3:1:1
该温度下平衡常数
________ (用各气体分压代入K的公式,用含 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
一定比例的 和
和 在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。________ (填是或不是)处于平衡状态,如果P不是平衡的,继续反应则平衡转化率________ 。490K之后,甲醇产率下降的原因是________________ 。
电解法转化 可实现
可实现 的资源化利用,电解
的资源化利用,电解 制
制 的原理示意图如图所示:
的原理示意图如图所示:______ 极相连,反应时阴极电极反应式为_____________ 。
 和6mol
和6mol  ,发生反应:
,发生反应: ,∆H=-49kJ/mol平衡时体系压强为
,∆H=-49kJ/mol平衡时体系压强为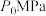 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

(2)下列能说明该反应已达到平衡状态的是
A.气体的密度不再变化
B.容器内气体的压强不再变化
C.

D.
 、
、 、
、 和
和 浓度之比为1:3:1:1
浓度之比为1:3:1:1该温度下平衡常数

 的代数式表示,
的代数式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。一定比例的
 和
和 在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。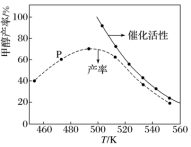
电解法转化
 可实现
可实现 的资源化利用,电解
的资源化利用,电解 制
制 的原理示意图如图所示:
的原理示意图如图所示: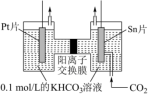
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】丙烯是产量仅次于乙烯的重要基本有机原料之一,丙烷脱氢制丙烯技术已经工业化。
I.无氧脱氢法: 。
。
(1)有利于该反应自发进行的条件是___________ (填“高温”“低温”或“任意温度”)。
(2)在压强分别为 和
和 的条件下,在密闭容器中充入等量的
的条件下,在密闭容器中充入等量的 ,发生脱氢反应,平衡时
,发生脱氢反应,平衡时 和
和 的物质的量分数随温度的变化如图所示。
的物质的量分数随温度的变化如图所示。

①在a、b、c、d四条曲线中,分别表示 时
时 和
和 物质的量分数的是
物质的量分数的是___________ 、___________ 。
②p点对应的平衡常数
___________ MPa(以分压表示,分压=总压×物质的量分数)。
Ⅱ.氧化脱氢法: 。
。
(3)在催化剂作用下,相同时间内,不同温度下 氧化脱氢的转化率和
氧化脱氢的转化率和 的产率如下:
的产率如下:
已知:
 。随着温度升高,
。随着温度升高, 的选择性
的选择性___________ (填“升高”“降低”或“不变”),可能的原因是___________ 。
I.无氧脱氢法:
 。
。(1)有利于该反应自发进行的条件是
(2)在压强分别为
 和
和 的条件下,在密闭容器中充入等量的
的条件下,在密闭容器中充入等量的 ,发生脱氢反应,平衡时
,发生脱氢反应,平衡时 和
和 的物质的量分数随温度的变化如图所示。
的物质的量分数随温度的变化如图所示。
①在a、b、c、d四条曲线中,分别表示
 时
时 和
和 物质的量分数的是
物质的量分数的是②p点对应的平衡常数

Ⅱ.氧化脱氢法:
 。
。(3)在催化剂作用下,相同时间内,不同温度下
 氧化脱氢的转化率和
氧化脱氢的转化率和 的产率如下:
的产率如下:| 反减温度/℃ | 465 | 480 | 495 | 510 |
 的转化率/% 的转化率/% | 5.5 | 12.1 | 17.3 | 28.4 |
 的产率% 的产率% | 4.7 | 9.5 | 12.8 | 18.5 |

 。随着温度升高,
。随着温度升高, 的选择性
的选择性
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染,研究其脱除方式意义重大。回答下列问题:
(1)COS与CO2为等电子体,COS的电子式为___________ 。
(2)已知:①CO(g)+H2O(g) H2(g)+CO2(g) ΔH1=-41.2kJ·mol-1
H2(g)+CO2(g) ΔH1=-41.2kJ·mol-1
②COS(g)+H2O(g) H2S(g)+CO2(g) ΔH2=-35.5kJ·mol-1
H2S(g)+CO2(g) ΔH2=-35.5kJ·mol-1
则氢气脱除COS生成CO和H2S的热化学方程式为___________ 。
(3)利用反应②可在高温下脱除COS,在T℃下,向密闭容器中充入5molH2O(g)和5molCOS(g),测得混合气体中H2S体积分数(φ)与时间(t)的关系如图所示。

①下列能说明该反应达到平衡状态的是___________ (填标号)。
A.v消耗(H2O)=v生成(CO2) B. 不变
不变
C.压强保持不变 D.混合气体的密度保持不变
②该条件下COS的平衡转化率为___________ ,T℃时该反应的平衡常数K= ___________ 。
(4)将含COS和H2O的某工业气体按一定流速通过以Al2O3为载体的催化剂,在不同温度下测得COS水解转化率如图所示。在催化剂不变时,为提高COS的转化率可采取的措施有___________ 、___________ 。


(5)工业生产中产生的SO2废气可用如上图方法获得H2SO4.写出电解的阳极反应式___________ 。
(1)COS与CO2为等电子体,COS的电子式为
(2)已知:①CO(g)+H2O(g)
 H2(g)+CO2(g) ΔH1=-41.2kJ·mol-1
H2(g)+CO2(g) ΔH1=-41.2kJ·mol-1②COS(g)+H2O(g)
 H2S(g)+CO2(g) ΔH2=-35.5kJ·mol-1
H2S(g)+CO2(g) ΔH2=-35.5kJ·mol-1则氢气脱除COS生成CO和H2S的热化学方程式为
(3)利用反应②可在高温下脱除COS,在T℃下,向密闭容器中充入5molH2O(g)和5molCOS(g),测得混合气体中H2S体积分数(φ)与时间(t)的关系如图所示。

①下列能说明该反应达到平衡状态的是
A.v消耗(H2O)=v生成(CO2) B.
 不变
不变C.压强保持不变 D.混合气体的密度保持不变
②该条件下COS的平衡转化率为
(4)将含COS和H2O的某工业气体按一定流速通过以Al2O3为载体的催化剂,在不同温度下测得COS水解转化率如图所示。在催化剂不变时,为提高COS的转化率可采取的措施有


(5)工业生产中产生的SO2废气可用如上图方法获得H2SO4.写出电解的阳极反应式
您最近一年使用:0次



