解题方法
1 . 1-丁烯是仅次于乙烯和丙烯的重要石油化工基本原料,可以利用正丁烷催化脱氢制备,催化脱氢又分为无氧催化脱氢和有氧催化脱氢。实际化工生产中需对反应条件(催化剂、温度等)进行探究,以获取最佳效益。
已知:I.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
II.产物收率=生成某产物的原料量/投入的原料量×100%。
(1)利用正丁烷无氧催化脱氢制备1-丁烯反应原理如下:
CH3CH2CH2CH3 H2C=CHCH2CH3+H2 ΔH
H2C=CHCH2CH3+H2 ΔH
已知CH3 CH2CH2CH3、CH2 =CHCH2CH3、H2的燃烧热分别为2 878 kJ/mol、2 720 kJ/mol、286 kJ/mol,计算ΔH=___________ 。
(2)无氧催化脱氢用Pt系催化剂时,正丁烷单位时间转化率和1-丁烯选择性如表所示。
①仅从1-丁烯选择性的角度考虑,应选择的催化剂为___________ (填催化剂序号,下同)。
②工业上,从1-丁烯单位时间收率的角度考虑,应选择的最佳催化剂为___________ 。
(3)其他条件相同,30 min时测得正丁烷转化率、1-丁烯收率随温度的变化关系如图所示。
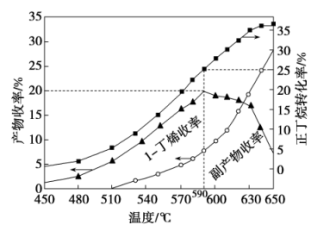
温度高于590 ℃时1-丁烯收率降低的原因是_________________ 。
(4)有氧催化脱氢通常选择O2或CO2为氧化剂,VOx-MgO为催化剂,反应原理如下:
2CH3CH2CH2CH3+O2 2CH2 =CHCH2CH3 +2H2O i
2CH2 =CHCH2CH3 +2H2O i
CH3 CH2CH2CH3+CO2 H2C=CHCH2CH3+H2O+CO ii
H2C=CHCH2CH3+H2O+CO ii
一定温度下,在体积为10 L的恒容密闭容器中,加入10 mol CH3CH2CH2CH3、7 mol O2、3 mol CO2进行反应i和ii.测得初始压强为20kPa,经过10h,反应达到平衡,此时压强变成25kPa,其中O2的体积分数为16%。回答下列问题:
①v(O2)=___________ kPa/h (用O2分压表示速率)。
②该温度下,反应ii的平衡常数Kp=___________ kPa。
③O2为氧化剂时,1-丁烯的选择性明显低于CO2为氧化剂时的选择性,分析可能原因:______________ 。
已知:I.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
II.产物收率=生成某产物的原料量/投入的原料量×100%。
(1)利用正丁烷无氧催化脱氢制备1-丁烯反应原理如下:
CH3CH2CH2CH3
 H2C=CHCH2CH3+H2 ΔH
H2C=CHCH2CH3+H2 ΔH已知CH3 CH2CH2CH3、CH2 =CHCH2CH3、H2的燃烧热分别为2 878 kJ/mol、2 720 kJ/mol、286 kJ/mol,计算ΔH=
(2)无氧催化脱氢用Pt系催化剂时,正丁烷单位时间转化率和1-丁烯选择性如表所示。
| 催化剂 | 单位时间转化率/% | 1-丁烯选择性/% |
| 催化剂1:PtSn/γ-Al2O3 | 23.0 | 92.0 |
| 催化剂2:PtSnSr0.2/γ-Al2O3 | 38.5 | 88.1 |
| 催化剂3:PtSn(0.3%)/MgAl2O4 | 27.0 | 98.9 |
②工业上,从1-丁烯单位时间收率的角度考虑,应选择的最佳催化剂为
(3)其他条件相同,30 min时测得正丁烷转化率、1-丁烯收率随温度的变化关系如图所示。

温度高于590 ℃时1-丁烯收率降低的原因是
(4)有氧催化脱氢通常选择O2或CO2为氧化剂,VOx-MgO为催化剂,反应原理如下:
2CH3CH2CH2CH3+O2
 2CH2 =CHCH2CH3 +2H2O i
2CH2 =CHCH2CH3 +2H2O iCH3 CH2CH2CH3+CO2
 H2C=CHCH2CH3+H2O+CO ii
H2C=CHCH2CH3+H2O+CO ii一定温度下,在体积为10 L的恒容密闭容器中,加入10 mol CH3CH2CH2CH3、7 mol O2、3 mol CO2进行反应i和ii.测得初始压强为20kPa,经过10h,反应达到平衡,此时压强变成25kPa,其中O2的体积分数为16%。回答下列问题:
①v(O2)=
②该温度下,反应ii的平衡常数Kp=
③O2为氧化剂时,1-丁烯的选择性明显低于CO2为氧化剂时的选择性,分析可能原因:
您最近一年使用:0次
解题方法
2 . CO2的回收与利用是科学家研究的热点课题。
已知:反应ICO2(g)+3H2(g) CH3OH(g)+H2O(g)△H1=-58kJ·mol-1
CH3OH(g)+H2O(g)△H1=-58kJ·mol-1
反应ICO2(g)+H2(g) CO(g)+H2O(g)△H2=+41kJ·mol-1
CO(g)+H2O(g)△H2=+41kJ·mol-1
(1)CO(g)和H2(g)反应生成CH3OH(g)的热化学方程式为______________ 。
(2)某实验过程中,控制压强一定,将CO2和H2按一定的初始投料比、一定流速通过催化剂,经过相同时间测得如下实验数据(反应未达到平衡状态):
表中实验数据表明,升高温度,CO2实际转化率提高而甲醇的选择性降低。其原因是____________________________ 。
(3)在一定条件下,选择合适的催化剂只进行反应CO2(g)+H2(g) CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
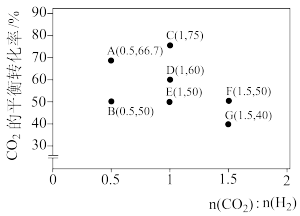
已知:Kx是以物质的量分数表示的化学平衡常数。
①经分析,A、E和G三点对应的反应温度相同,结合数据说明判断理由_______________ 。
②已知反应速率v=v正-v逆=k正x(CO2)x(H2)-k逆x(CO)x(H2O),k正、k逆分别为正、逆向反应速率常数,x为物质的量分数。C、D、E三点中k正-k逆最大的是___________ ,A、B、F三点中v逆最大的是___________ 。计算E点所示的投料比在从起始到平衡的过程中,当CO2转化率达到50%时, =
=___________ 。
(4)关于合成甲醇过程中用到的催化剂,下列说法错误的是___________ (填字母)。
A.参与了反应,改变了反应历程和△HB.使k正和k逆增大,但二者增大倍数不同
C.降低了反应的活化能D.提高了CO2的平衡转化率
已知:反应ICO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H1=-58kJ·mol-1
CH3OH(g)+H2O(g)△H1=-58kJ·mol-1反应ICO2(g)+H2(g)
 CO(g)+H2O(g)△H2=+41kJ·mol-1
CO(g)+H2O(g)△H2=+41kJ·mol-1(1)CO(g)和H2(g)反应生成CH3OH(g)的热化学方程式为
(2)某实验过程中,控制压强一定,将CO2和H2按一定的初始投料比、一定流速通过催化剂,经过相同时间测得如下实验数据(反应未达到平衡状态):
T/K | CO2实际转化率/% | 甲醇的选择性/% |
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
(3)在一定条件下,选择合适的催化剂只进行反应CO2(g)+H2(g)
 CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
CO(g)+H2O(g)。调整CO2和H2初始投料比,测得在一定投料比和一定温度下,该反应CO2的平衡转化率如图(各点对应的反应温度可能相同,也可能不同)。
已知:Kx是以物质的量分数表示的化学平衡常数。
①经分析,A、E和G三点对应的反应温度相同,结合数据说明判断理由
②已知反应速率v=v正-v逆=k正x(CO2)x(H2)-k逆x(CO)x(H2O),k正、k逆分别为正、逆向反应速率常数,x为物质的量分数。C、D、E三点中k正-k逆最大的是
 =
=(4)关于合成甲醇过程中用到的催化剂,下列说法错误的是
A.参与了反应,改变了反应历程和△HB.使k正和k逆增大,但二者增大倍数不同
C.降低了反应的活化能D.提高了CO2的平衡转化率
您最近一年使用:0次



