解题方法
1 . 氨的催化氧化过程是当下研究的重要课题。
(1) 与
与 在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:

反应ii: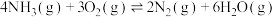
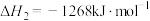
①该条件下 与
与 反应生成NO的热化学方程式为
反应生成NO的热化学方程式为___________ 。
②在恒温恒容密闭容器中,下列说法可以证明反应i已达到平衡状态的是___________ (填序号)。
A.
B.n个 键断裂的同时,有n个
键断裂的同时,有n个 键形成
键形成
C.混合气体的密度不变
D.容器内压强不变
③反应i与反应ii有关物质产率与温度的关系如图。下列说法正确 的是___________ 。
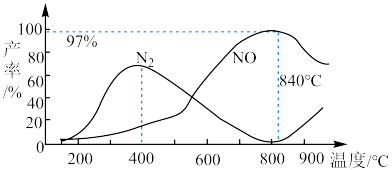
A.氨催化氧化生成 时,温度应控制在400℃左右
时,温度应控制在400℃左右
B.对反应升温可提高反应物转化率
C.提高物料比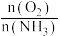 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率
D.840℃后,NO产率下降的主要原因是以反应(ii)为主
(2)在两个恒压密闭容器中分别充入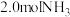 、
、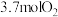 ,仅发生反应ii,测得
,仅发生反应ii,测得 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。
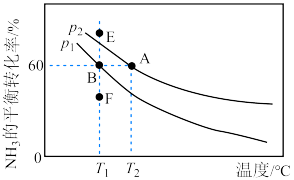
①
___________  (填“>”或“<”),理由是
(填“>”或“<”),理由是___________ 。
②若容器的初始体积为2.0L,则在A点状态下平衡时容器中
___________  。
。
③B点的平衡常数
___________ 。(用分压表示,气体分压=气体总压 气体的物质的量分数。写出代数式,无需计算具体结果)
气体的物质的量分数。写出代数式,无需计算具体结果)
④若温度为 ,压强为
,压强为 ,容器的初始体积为2.0L时,分别充入
,容器的初始体积为2.0L时,分别充入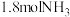 、
、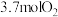 、0.2molAr发生反应ii,此时
、0.2molAr发生反应ii,此时 的平衡转化率为图中的点
的平衡转化率为图中的点___________ (选填“E”、“B”或“F”)。
(1)
 与
与 在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:反应i:


反应ii:
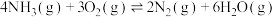
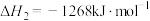
①该条件下
 与
与 反应生成NO的热化学方程式为
反应生成NO的热化学方程式为②在恒温恒容密闭容器中,下列说法可以证明反应i已达到平衡状态的是
A.

B.n个
 键断裂的同时,有n个
键断裂的同时,有n个 键形成
键形成C.混合气体的密度不变
D.容器内压强不变
③反应i与反应ii有关物质产率与温度的关系如图。下列说法

A.氨催化氧化生成
 时,温度应控制在400℃左右
时,温度应控制在400℃左右B.对反应升温可提高反应物转化率
C.提高物料比
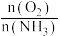 的值,主要目的的是提高反应速率
的值,主要目的的是提高反应速率D.840℃后,NO产率下降的主要原因是以反应(ii)为主
(2)在两个恒压密闭容器中分别充入
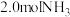 、
、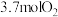 ,仅发生反应ii,测得
,仅发生反应ii,测得 的平衡转化率随温度的变化如图所示。
的平衡转化率随温度的变化如图所示。
①

 (填“>”或“<”),理由是
(填“>”或“<”),理由是②若容器的初始体积为2.0L,则在A点状态下平衡时容器中

 。
。③B点的平衡常数

 气体的物质的量分数。写出代数式,无需计算具体结果)
气体的物质的量分数。写出代数式,无需计算具体结果)④若温度为
 ,压强为
,压强为 ,容器的初始体积为2.0L时,分别充入
,容器的初始体积为2.0L时,分别充入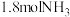 、
、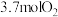 、0.2molAr发生反应ii,此时
、0.2molAr发生反应ii,此时 的平衡转化率为图中的点
的平衡转化率为图中的点
您最近一年使用:0次
解题方法
2 . 我国力争于2030年前实现碳达峰,2060年前实现碳中和。研发二氧化碳的碳捕集和碳利用技术是科学研究的热点问题。实现碳达峰、碳中和目标的有效方式之一是CO2加氢生产甲醇(CH3OH),反应体系中发生如下反应:
ⅰ.CO(g)+2H2(g) CH3OH(g) ∆H1=-90.77kJ/mol
CH3OH(g) ∆H1=-90.77kJ/mol
ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=+41.21kJ/mol
CO(g)+H2O(g) ∆H2=+41.21kJ/mol
ⅲ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H3
CH3OH(g)+H2O(g) ∆H3
(1)∆H3=___________ kJ/mol;反应ⅰ、ⅱ、ⅲ在不同温度下对应的平衡常数如图1所示,220℃时,反应ⅰ的平衡常数K=8.1×10-3,则220℃时,反应ⅲ的平衡常数K=___________ 。

(2)在催化剂作用下,往容积为2L的刚性容器中通入1molCO2(g)和3molH2(g),发生反应ⅰ、ⅱ、ⅲ,不同温度下CO2的平衡转化率和甲醇的选择性【甲醇的选择性=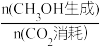 】如图2所示。
】如图2所示。
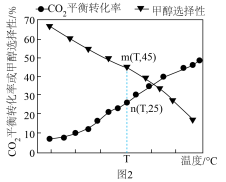
①在T℃时,若仅发生反应ⅲ,下列说法能证明反应ⅲ达到平衡状态的是___________ (填标号)。
A.容器内混合气体的密度不再改变
B.容器内二氧化碳与水的物质的量之比不再改变
C.容器内总压强不再改变
D.碳原子数目不再改变
②甲醇的选择性随温度的升高而降低的原因可能是___________ ;T℃下反应ⅱ的平衡常数K=___________ (保留小数点后3位)。
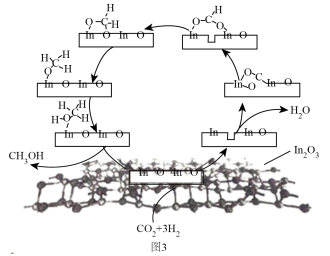
(3)在In2O3表面可以实现CO2加氢合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H3,反应历程如图3,下列说法正确的是___________(填标号)。
CH3OH(g)+H2O(g) ∆H3,反应历程如图3,下列说法正确的是___________(填标号)。
(4)利用光电催化原理,由CO2和H2O也可制备CH3OH,装置如图4所示,不同催化剂下生成CH3OH的法拉第效率与电极电势的关系如图5所示(已知法拉第效率是指实际生成物和理论生成物的百分比)。
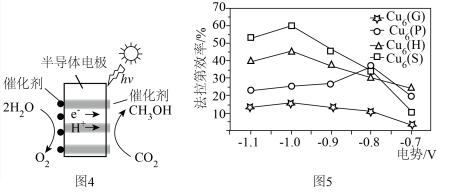
①为了保证生成甲醇的法拉第效率在较高水平,最合适的电势及最佳催化剂是___________ 。
②写出光电催化装置图中右侧的电极反应式:___________ 。
ⅰ.CO(g)+2H2(g)
 CH3OH(g) ∆H1=-90.77kJ/mol
CH3OH(g) ∆H1=-90.77kJ/molⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2=+41.21kJ/mol
CO(g)+H2O(g) ∆H2=+41.21kJ/molⅲ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H3
CH3OH(g)+H2O(g) ∆H3(1)∆H3=

(2)在催化剂作用下,往容积为2L的刚性容器中通入1molCO2(g)和3molH2(g),发生反应ⅰ、ⅱ、ⅲ,不同温度下CO2的平衡转化率和甲醇的选择性【甲醇的选择性=
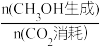 】如图2所示。
】如图2所示。
①在T℃时,若仅发生反应ⅲ,下列说法能证明反应ⅲ达到平衡状态的是
A.容器内混合气体的密度不再改变
B.容器内二氧化碳与水的物质的量之比不再改变
C.容器内总压强不再改变
D.碳原子数目不再改变
②甲醇的选择性随温度的升高而降低的原因可能是
(3)在In2O3表面可以实现CO2加氢合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H3,反应历程如图3,下列说法正确的是___________(填标号)。
CH3OH(g)+H2O(g) ∆H3,反应历程如图3,下列说法正确的是___________(填标号)。
| A.In2O3能提高CO2的平衡转化率 | B.反应过程中,CO2发生了还原反应 |
| C.In2O3会使|∆H3|的数值减小 | D.In2O3提高了活化分子百分数 |
(4)利用光电催化原理,由CO2和H2O也可制备CH3OH,装置如图4所示,不同催化剂下生成CH3OH的法拉第效率与电极电势的关系如图5所示(已知法拉第效率是指实际生成物和理论生成物的百分比)。

①为了保证生成甲醇的法拉第效率在较高水平,最合适的电势及最佳催化剂是
②写出光电催化装置图中右侧的电极反应式:
您最近一年使用:0次
3 .  资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:
反应I:

反应II: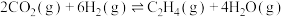

(1)基态镍原子核外电子的轨道表示式为____________
(2)将反应后气体通入______ (填试剂名称),可证明反应II发生。
(3)计算

______ (用 和
和 表示)
表示)
(4)相同投料比时,体系内 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为________ 。
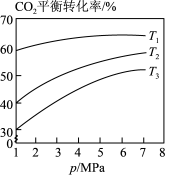
(5)向1 L恒压、密闭容器中通入1 mol 和4 mol
和4 mol  ,测得有关物质的物质的量随温度变化如图。
,测得有关物质的物质的量随温度变化如图。
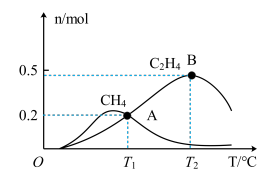
①催化剂在较低温度时主要选择______ (填“反应I”或“反应II”)
② 时
时 的转化率为
的转化率为______ ,反应I的平衡常数
______ 。
(6)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:
 +75 kJ/mol
+75 kJ/mol
消碳反应:
 -173 kJ/mol
-173 kJ/mol
其他条件相同时,催化剂表面积碳量与温度的关系如图所示, ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是______ 。

 资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使
资源化利用对缓解碳减排压力具有重要意义,使用镍氢催化剂可使 转化为
转化为 。反应体系中主要反应的热化学方程式为:
。反应体系中主要反应的热化学方程式为:反应I:


反应II:
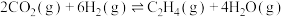

(1)基态镍原子核外电子的轨道表示式为
(2)将反应后气体通入
(3)计算


 和
和 表示)
表示)(4)相同投料比时,体系内
 的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
的平衡转化率与温度T和压强p的关系如图,温度从高到低的顺序为
(5)向1 L恒压、密闭容器中通入1 mol
 和4 mol
和4 mol  ,测得有关物质的物质的量随温度变化如图。
,测得有关物质的物质的量随温度变化如图。
①催化剂在较低温度时主要选择
②
 时
时 的转化率为
的转化率为
(6)镍氢催化剂活性会因为甲烷分解产生积碳而降低,同时二氧化碳可与碳发生消碳反应:
积碳反应:

 +75 kJ/mol
+75 kJ/mol消碳反应:

 -173 kJ/mol
-173 kJ/mol其他条件相同时,催化剂表面积碳量与温度的关系如图所示,
 ℃之后,温度升高积碳量减小的主要原因是
℃之后,温度升高积碳量减小的主要原因是
您最近一年使用:0次
名校
解题方法
4 . 工业上制硫酸的主要反应之一为: ,反应过程中能量的变化如图所示。
,反应过程中能量的变化如图所示。
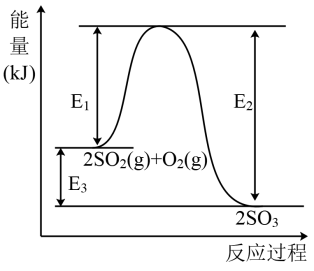
(1)向反应体系中加入催化剂后,图中
_______ (填“增大”、“减小”或“不变”,下同),
_______ 。
(2)已知:
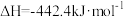

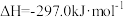
若 与
与 反应产生
反应产生 和
和 ,则反应的热化学方程式为
,则反应的热化学方程式为_______ 。
(3)某温度下,反应的起始浓度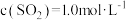 ,
,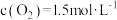 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为_______ 。
(4)在 温度时,该反应的平衡常数
温度时,该反应的平衡常数 ,若在此温度下,向
,若在此温度下,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入 、
、 和
和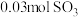 ,则反应开始时正反应速率
,则反应开始时正反应速率_______ (填“>”、“=”或“<”)逆反应速率。
(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是_______。(填字母)
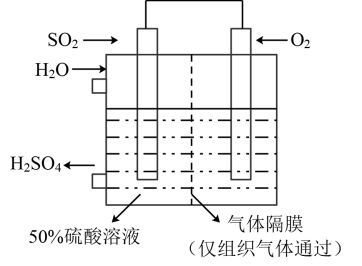
(6)若以如图所示装置生产硫酸,将 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为_______ 。
 ,反应过程中能量的变化如图所示。
,反应过程中能量的变化如图所示。
(1)向反应体系中加入催化剂后,图中


(2)已知:

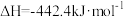

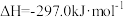
若
 与
与 反应产生
反应产生 和
和 ,则反应的热化学方程式为
,则反应的热化学方程式为(3)某温度下,反应的起始浓度
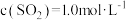 ,
,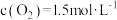 ,达到平衡后,
,达到平衡后, 的转化率为50%,则此温度下该反应的平衡常数K的数值为
的转化率为50%,则此温度下该反应的平衡常数K的数值为(4)在
 温度时,该反应的平衡常数
温度时,该反应的平衡常数 ,若在此温度下,向
,若在此温度下,向 的恒容密闭容器中,充入
的恒容密闭容器中,充入 、
、 和
和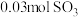 ,则反应开始时正反应速率
,则反应开始时正反应速率(5)恒温恒容条件下,下列叙述能证明该反应已达化学平衡状态的是_______。(填字母)
A. 的体积分数不再发生变化 的体积分数不再发生变化 |
| B.恒容时,容器内压强不再发生变化 |
| C.容器内,气体原子总数不再发生变化 |
D.相同时间内消耗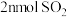 的同时生成 的同时生成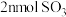 |
 、
、 以一定压强喷到活性电极上反应。负极的电极反应式为
以一定压强喷到活性电极上反应。负极的电极反应式为
您最近一年使用:0次
2022-01-21更新
|
283次组卷
|
2卷引用:北京市丰台区2021~2022学年高二上学期期末考试化学试题
5 . 还原法处理氮的氧化物是环境保护的热门课题。
Ⅰ.CO还原法:
(1)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh作催化剂时该反应的过程示意图如下:
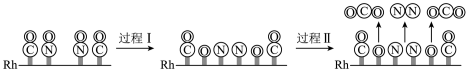
已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为_______ 。
Ⅱ.焦炭还原法:
(2)用焦炭还原 的反应为:
的反应为: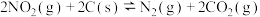 ∆H>0。
∆H>0。
①在一定条件下,下列事实一定能证明该反应已经达到平衡状态的是_______ 。
A.恒温恒容条件下,
B.绝热恒容条件下,体系的温度不再改变
C.恒温恒压条件下,混合气体密度不再改变
D.恒温恒容条件下, 与
与 的体积比不再改变
的体积比不再改变
②在恒温条件下,1mol 和足量C发生该反应,测得平衡时
和足量C发生该反应,测得平衡时 和
和 的物质的量浓度与平衡总压强的关系如图所示,则A、B两点的反应速率关系为v(A)
的物质的量浓度与平衡总压强的关系如图所示,则A、B两点的反应速率关系为v(A) _______ v(B)(填“>”、“<”或“=”),C点时该反应的分压平衡常数
_______ ( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。

③下列措施既能加快反应速率,又能提高平衡转化率的是_______ 。
A.升高温度 B.增加炭的用量 C.增大压强 D.使用催化剂
Ⅲ. 还原法:
还原法:
(3)以氨气作还原剂,可除去烟气中的氮氧化物。其中除去NO的反应原理如下: ∆H=-1980kJ/mol,反应速率与浓度之间存在如下关系:
∆H=-1980kJ/mol,反应速率与浓度之间存在如下关系: ,
,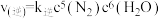 ,k正,k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9mol
,k正,k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9mol  和1.2mol
和1.2mol  发生反应,保持温度不变,平衡时NO的转化率为50%,则此温度下
发生反应,保持温度不变,平衡时NO的转化率为50%,则此温度下
_______ ;温度升高时,k正增大m倍,k逆增大n倍,则m_______ n(填“>”、“<”或“=”)。
Ⅰ.CO还原法:
(1)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh作催化剂时该反应的过程示意图如下:

已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为
Ⅱ.焦炭还原法:
(2)用焦炭还原
 的反应为:
的反应为: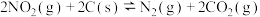 ∆H>0。
∆H>0。①在一定条件下,下列事实一定能证明该反应已经达到平衡状态的是
A.恒温恒容条件下,

B.绝热恒容条件下,体系的温度不再改变
C.恒温恒压条件下,混合气体密度不再改变
D.恒温恒容条件下,
 与
与 的体积比不再改变
的体积比不再改变②在恒温条件下,1mol
 和足量C发生该反应,测得平衡时
和足量C发生该反应,测得平衡时 和
和 的物质的量浓度与平衡总压强的关系如图所示,则A、B两点的反应速率关系为v(A)
的物质的量浓度与平衡总压强的关系如图所示,则A、B两点的反应速率关系为v(A) 
 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
③下列措施既能加快反应速率,又能提高平衡转化率的是
A.升高温度 B.增加炭的用量 C.增大压强 D.使用催化剂
Ⅲ.
 还原法:
还原法:(3)以氨气作还原剂,可除去烟气中的氮氧化物。其中除去NO的反应原理如下:
 ∆H=-1980kJ/mol,反应速率与浓度之间存在如下关系:
∆H=-1980kJ/mol,反应速率与浓度之间存在如下关系: ,
,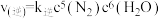 ,k正,k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9mol
,k正,k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9mol  和1.2mol
和1.2mol  发生反应,保持温度不变,平衡时NO的转化率为50%,则此温度下
发生反应,保持温度不变,平衡时NO的转化率为50%,则此温度下
您最近一年使用:0次
6 . 工业上可溶性的钡盐常用重晶石(BaSO4)与焦炭在高温下还原得到,按物质的量之比1:3投料。主要发生如下反应:
①BaSO4(s)+2C(s) BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1
BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1
②BaSO4(s)+4C(s) BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1
BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1
③BaSO4(s)+4CO(g) BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1
BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1
④CO2(g)+C(s) 2CO(g)ΔH4
2CO(g)ΔH4
按要求回答下列问题:
(1)ΔH4=___ kJ•mol-1。
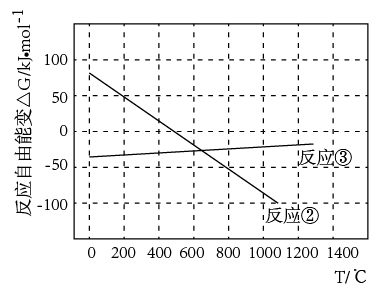
(2)已知体系自由能变ΔG=ΔH-TΔS,ΔG<0时反应自发进行。由下图可知工业上用焦炭还原重晶石发生反应②,至少需控制反应温度___ ℃以上。
(3)将重晶石与焦炭(固体均足量)在恒压密闭容器中控制1000℃温度下发生反应,下列能证明反应③达到平衡状态的是___ 。
A.气体的压强不变
B.CO2的体积分数保持不变
C.v(CO):v(CO2)=1:1
D.容器内气体密度不变
(4)T℃温度下,碳热还原硫酸钡反应达到平衡时,混合气体的总压强为P,其中CO的物质的量分数为α,则反应③的平衡常数Kp=__ 。[说明:对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)可表示平衡常数,记作Kp,如p(B)=p•x(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数]。
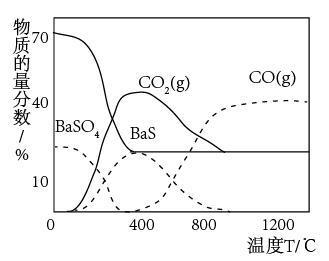
(5)常压下,不同反应温度下碳热还原硫酸钡反应体系各物质的组成如图所示。400℃以,反应①可以看成反应②和反应③连续进行的结果,由图可判断在400℃以下时反应②的速率___ 反应③(填“>”、“<”或“=”),理由是__ 。
①BaSO4(s)+2C(s)
 BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1
BaS(s)+2CO2(g)ΔH1=-98kJ•mol-1②BaSO4(s)+4C(s)
 BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1
BaS(s)+4CO(g)ΔH2=+571.2kJ•mol-1③BaSO4(s)+4CO(g)
 BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1
BaS(s)+4CO2(g)ΔH3=-118.8kJ•mol-1④CO2(g)+C(s)
 2CO(g)ΔH4
2CO(g)ΔH4
按要求回答下列问题:
(1)ΔH4=
(2)已知体系自由能变ΔG=ΔH-TΔS,ΔG<0时反应自发进行。由下图可知工业上用焦炭还原重晶石发生反应②,至少需控制反应温度
(3)将重晶石与焦炭(固体均足量)在恒压密闭容器中控制1000℃温度下发生反应,下列能证明反应③达到平衡状态的是
A.气体的压强不变
B.CO2的体积分数保持不变
C.v(CO):v(CO2)=1:1
D.容器内气体密度不变
(4)T℃温度下,碳热还原硫酸钡反应达到平衡时,混合气体的总压强为P,其中CO的物质的量分数为α,则反应③的平衡常数Kp=
(5)常压下,不同反应温度下碳热还原硫酸钡反应体系各物质的组成如图所示。400℃以,反应①可以看成反应②和反应③连续进行的结果,由图可判断在400℃以下时反应②的速率

您最近一年使用:0次
7 . 合成气(CO+H2)是制备合成油和烯烃等众多化工产品的枢纽原料,而催化甲烷部分氧化是生产合成气的主要工艺之一,涉及的反应为:
①2CH4(g)+O2(g) 2CO(g)+4H2(g) △H
2CO(g)+4H2(g) △H
已知如下反应:
②CH4(g)+2O2(g) CO2(g)+2H2O(g) △H1=-810kJ/mol
CO2(g)+2H2O(g) △H1=-810kJ/mol
③CH4(g)+H2O(g) CO(g)+3H2(g) △H2=+225kJ/mol
CO(g)+3H2(g) △H2=+225kJ/mol
④CO(g)+H2O(g) CO2(g)+H2(g) △H3=-35kJ/mol
CO2(g)+H2(g) △H3=-35kJ/mol
请回答下列问题:
(1)试计算反应①的△H=___ 。
(2)在某体积固定的绝热密闭容器中发生反应④,下列事实能证明反应已达平衡的是___ 。
(3)在某恒容密闭容器中加入一定量的甲烷和氧气发生反应③,使其充分反应,测得不同温度和压强下甲烷的转化率如图1所示,由该图可得出的结论是___ 。

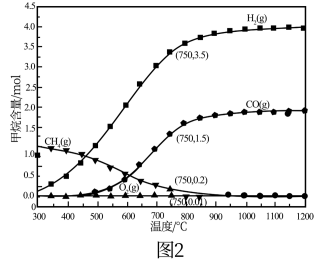
(4)现将2molCH4和1molO2加入某体积可变的密闭容器中,发生反应①。控制压强为1atm,测得不同温度下反应体系中各组分平衡含量如图2所示。实际生产中控制的温度为750℃,则此温度下CO的产率为___ ,若平衡时容器的体积为VL,则该反应的平衡常数K=___ 。(用含V代数式表示,不必化简)。
①2CH4(g)+O2(g)
 2CO(g)+4H2(g) △H
2CO(g)+4H2(g) △H已知如下反应:
②CH4(g)+2O2(g)
 CO2(g)+2H2O(g) △H1=-810kJ/mol
CO2(g)+2H2O(g) △H1=-810kJ/mol③CH4(g)+H2O(g)
 CO(g)+3H2(g) △H2=+225kJ/mol
CO(g)+3H2(g) △H2=+225kJ/mol④CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-35kJ/mol
CO2(g)+H2(g) △H3=-35kJ/mol请回答下列问题:
(1)试计算反应①的△H=
(2)在某体积固定的绝热密闭容器中发生反应④,下列事实能证明反应已达平衡的是
| A.容器内温度不再变化 | B.混合气体的平均分子量不再变化 |
| C.各组分的物质的量相等 | D.1molH—O键断裂同时有1molH—H键断裂 |

(4)现将2molCH4和1molO2加入某体积可变的密闭容器中,发生反应①。控制压强为1atm,测得不同温度下反应体系中各组分平衡含量如图2所示。实际生产中控制的温度为750℃,则此温度下CO的产率为

您最近一年使用:0次
8 . NO、NO2是空气中的污染物,将NO、NO2转化为N2(g)是化学工作者的重要研究课题,回答下列问题:
(1)已知反应Ⅰ: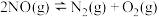 △H1=-180.5 kJ/mol
△H1=-180.5 kJ/mol
反应Ⅱ: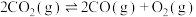 △H2=+566 kJ/mol
△H2=+566 kJ/mol
反应Ⅲ: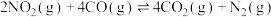 △H3=-1200 kJ/mol
△H3=-1200 kJ/mol
则反应Ⅳ: △H4=
△H4=___________ kJ/mol。
(2)已知NO和O2经反应a和反应b转化为NO2,其能量随反应进程的变化如图所示。

反应a:
 K1
K1
反应b:
 K2
K2
下列说法正确的是___________ (填标号)。
A.反应b的速率大小决定了NO2(g)的生成速率
B.2NO(g)+O2(g) 2NO2(g)的平衡常数K=K1+K2
2NO2(g)的平衡常数K=K1+K2
C.从热力学角度分析,2NO(g)+O2(g) 2NO2(g)能自发进行的原因是熵变的影响大于焓变的影响
2NO2(g)能自发进行的原因是熵变的影响大于焓变的影响
(3)已知
 。T℃时,将一定量的NO2(g)、N2O4(g)充入一个容积为2 L的恒容密闭容器中,各物质浓度随时间变化的关系如下表所示:
。T℃时,将一定量的NO2(g)、N2O4(g)充入一个容积为2 L的恒容密闭容器中,各物质浓度随时间变化的关系如下表所示:
①下列说法可以说明反应达到平衡状态的是___________ (填标号)。
A.混合气体的密度不再发生变化
B.NO2的体积分数不再发生变化
C.
D.混合气体的颜色不再发生变化
②5min时,v正(NO2)___________ (填“>”或“<”)v逆(NO2);0~10 min内,v(N2O4)___________ mol/(L·min);N2O4的平衡转化率为___________ 。
③在该温度下,K=___________ mol/L。
(1)已知反应Ⅰ:
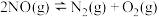 △H1=-180.5 kJ/mol
△H1=-180.5 kJ/mol 反应Ⅱ:
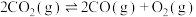 △H2=+566 kJ/mol
△H2=+566 kJ/mol 反应Ⅲ:
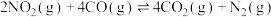 △H3=-1200 kJ/mol
△H3=-1200 kJ/mol 则反应Ⅳ:
 △H4=
△H4=(2)已知NO和O2经反应a和反应b转化为NO2,其能量随反应进程的变化如图所示。

反应a:

 K1
K1反应b:

 K2
K2下列说法正确的是
A.反应b的速率大小决定了NO2(g)的生成速率
B.2NO(g)+O2(g)
 2NO2(g)的平衡常数K=K1+K2
2NO2(g)的平衡常数K=K1+K2C.从热力学角度分析,2NO(g)+O2(g)
 2NO2(g)能自发进行的原因是熵变的影响大于焓变的影响
2NO2(g)能自发进行的原因是熵变的影响大于焓变的影响(3)已知

 。T℃时,将一定量的NO2(g)、N2O4(g)充入一个容积为2 L的恒容密闭容器中,各物质浓度随时间变化的关系如下表所示:
。T℃时,将一定量的NO2(g)、N2O4(g)充入一个容积为2 L的恒容密闭容器中,各物质浓度随时间变化的关系如下表所示:| 时间/min | 0 | 5 | 10 | 20 | 50 |
| c(NO2)/(mol/L) | 0.2 | c | 0.6 | 0.7 | 0.7 |
| c(N2O4)/(mol/L) | 0.6 | c | 0.4 | 0.35 | 0.35 |
A.混合气体的密度不再发生变化
B.NO2的体积分数不再发生变化
C.

D.混合气体的颜色不再发生变化
②5min时,v正(NO2)
③在该温度下,K=
您最近一年使用:0次
2023-07-30更新
|
192次组卷
|
2卷引用:广西壮族自治区贵港市2022-2023学年高二上学期期末考试化学试题
9 . 乙烯的产量是衡量一个国家石油化工发展水平的重要标志,工业上有多种方法制备乙烯。回答下列问题:
Ⅰ.以乙烷为原料制备乙烯
已知:①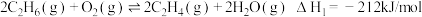
②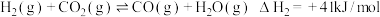
③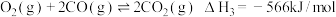
(1)写出反应④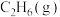 分解制备
分解制备 的热化学方程式
的热化学方程式_______
(2)某温度下,只发生反应④,向 的恒容密闭容器中通入
的恒容密闭容器中通入 ,初始压强为
,初始压强为 ,测得
,测得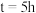 时该反应达到平衡状态,此时
时该反应达到平衡状态,此时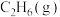 的体积分数为
的体积分数为 ,反应从开始到平衡,用
,反应从开始到平衡,用 表示的该反应的平均反应速率
表示的该反应的平均反应速率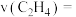
_______ ;该温度下反应的压强平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
Ⅱ.以二氧化碳为原料制备乙烯已知 和
和 在铁系催化剂作用下发生化学反应⑤
在铁系催化剂作用下发生化学反应⑤ ,会有副反应②发生
,会有副反应②发生
(3)在三个容积均为 的密闭容器中以不同的氢碳比
的密闭容器中以不同的氢碳比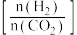 充入
充入 和
和 ,在一定条件下
,在一定条件下 的平衡转化率与温度的关系如图1所示
的平衡转化率与温度的关系如图1所示
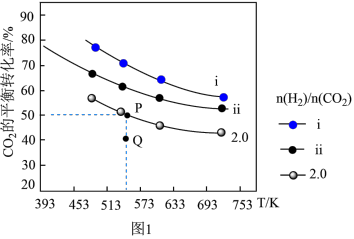
下列关于反应⑤的说法不正确的是______
(4)在密闭容器中通入 和
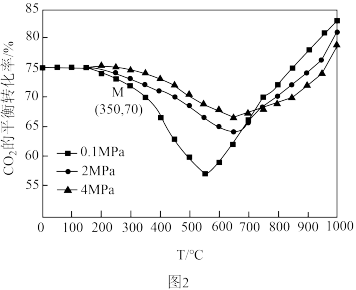
和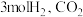 平衡转化率随温度和压强的变化如图2所示。温度大于
平衡转化率随温度和压强的变化如图2所示。温度大于 ,随着压强的增大,
,随着压强的增大, 的平衡转化率减小,解释其原因
的平衡转化率减小,解释其原因_______
Ⅲ.以碘甲烷 为原料制备乙烯
为原料制备乙烯
已知反应⑥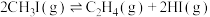 ;⑦
;⑦ ;⑧
;⑧ .维持温度为
.维持温度为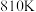 ,压强为
,压强为 ,起始时投入
,起始时投入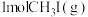 ,达到平衡时,测得平衡体系中
,达到平衡时,测得平衡体系中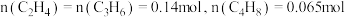
(5)平衡时 的转化率为
的转化率为_______
(6)已知在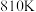 条件下,存在等式
条件下,存在等式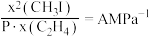 (
( 为常数,
为常数, 为平衡时的总压强,
为平衡时的总压强,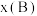 为平衡时
为平衡时 的物质的量分数)。保持其它条件不变,请在图3中画出
的物质的量分数)。保持其它条件不变,请在图3中画出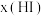 随压强
随压强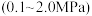 变化的图像
变化的图像______
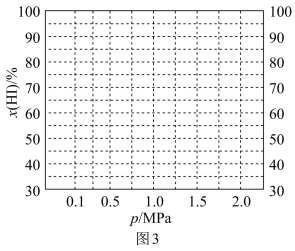
Ⅰ.以乙烷为原料制备乙烯
已知:①
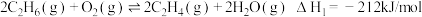
②
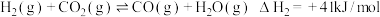
③
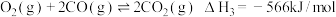
(1)写出反应④
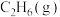 分解制备
分解制备 的热化学方程式
的热化学方程式(2)某温度下,只发生反应④,向
 的恒容密闭容器中通入
的恒容密闭容器中通入 ,初始压强为
,初始压强为 ,测得
,测得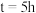 时该反应达到平衡状态,此时
时该反应达到平衡状态,此时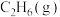 的体积分数为
的体积分数为 ,反应从开始到平衡,用
,反应从开始到平衡,用 表示的该反应的平均反应速率
表示的该反应的平均反应速率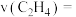

 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数) Ⅱ.以二氧化碳为原料制备乙烯已知
 和
和 在铁系催化剂作用下发生化学反应⑤
在铁系催化剂作用下发生化学反应⑤ ,会有副反应②发生
,会有副反应②发生(3)在三个容积均为
 的密闭容器中以不同的氢碳比
的密闭容器中以不同的氢碳比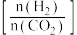 充入
充入 和
和 ,在一定条件下
,在一定条件下 的平衡转化率与温度的关系如图1所示
的平衡转化率与温度的关系如图1所示
下列关于反应⑤的说法不正确的是______
| A.该反应的正反应活化能>逆反应活化能 |
| B.图1中,氢碳比:ⅰ>ⅱ |
| C.图1中,当氢碳比为2.0时,Q点:v(正)<v(逆) |
D.图1中,当反应处于 点状态时,形成 点状态时,形成 碳碳双键的同时断裂 碳碳双键的同时断裂 碳氧双键 碳氧双键 |
 和
和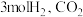 平衡转化率随温度和压强的变化如图2所示。温度大于
平衡转化率随温度和压强的变化如图2所示。温度大于 ,随着压强的增大,
,随着压强的增大, 的平衡转化率减小,解释其原因
的平衡转化率减小,解释其原因
Ⅲ.以碘甲烷
 为原料制备乙烯
为原料制备乙烯已知反应⑥
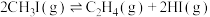 ;⑦
;⑦ ;⑧
;⑧ .维持温度为
.维持温度为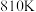 ,压强为
,压强为 ,起始时投入
,起始时投入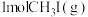 ,达到平衡时,测得平衡体系中
,达到平衡时,测得平衡体系中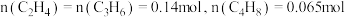
(5)平衡时
 的转化率为
的转化率为(6)已知在
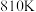 条件下,存在等式
条件下,存在等式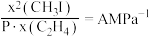 (
( 为常数,
为常数, 为平衡时的总压强,
为平衡时的总压强,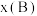 为平衡时
为平衡时 的物质的量分数)。保持其它条件不变,请在图3中画出
的物质的量分数)。保持其它条件不变,请在图3中画出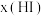 随压强
随压强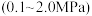 变化的图像
变化的图像
您最近一年使用:0次
10 . 化学反应过程中释放或吸收的热量在生活、生产、科技及科研中应用广泛。
(1)生活中的冷敷袋是利用___________ (填“放热”或“吸热”)的化学变化或物理变化,下列有关化学变化中能量变化的说法中,正确的是___________ 。
A.需要加热才能发生的反应也可能是放热反应
B.化学键断裂时会放出能量
C.反应物的总能量高于生成物的总能量表现为吸热反应
D.反应物的总键能高于生成物的总键能表现为吸热反应
(2)甲烷可用于生产合成气,其反应为
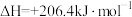 ,已知断裂1mol相关化学键所需的能量如下表:
,已知断裂1mol相关化学键所需的能量如下表:
则a=___________ ,若加入催化剂改变上述反应历程,上述反应的 △H___________ (填“变大”“变小”或“不变”)
(3)联氨(又称肼, ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
①联氨分子的电子式为___________ 。
②已知:N2(g)+2O2(g)=2NO2(g) △H=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-534kJ/mol
H2O(g) =H2O(l) △H=-44.0kJ/mol
则 △H=
△H=__________ 。
(1)生活中的冷敷袋是利用
A.需要加热才能发生的反应也可能是放热反应
B.化学键断裂时会放出能量
C.反应物的总能量高于生成物的总能量表现为吸热反应
D.反应物的总键能高于生成物的总键能表现为吸热反应
(2)甲烷可用于生产合成气,其反应为

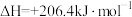 ,已知断裂1mol相关化学键所需的能量如下表:
,已知断裂1mol相关化学键所需的能量如下表:| 化学键 |  |  |  |  |
键能/ | 436 | a | 415.1 | 1076 |
(3)联氨(又称肼,
 ,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。①联氨分子的电子式为
②已知:N2(g)+2O2(g)=2NO2(g) △H=+66.4kJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-534kJ/mol
H2O(g) =H2O(l) △H=-44.0kJ/mol
则
 △H=
△H=
您最近一年使用:0次



