解题方法
1 . 含碳化合物的合成与转化具有重要的研究价值。
(1)热力学规定,在标准压强和指定温度下,由元素最稳定的单质生成 化合物时的反应热称为该化合物的标准摩尔生成焓。常温下,
化合物时的反应热称为该化合物的标准摩尔生成焓。常温下, 、
、 的标准摩尔生成焓分别为
的标准摩尔生成焓分别为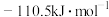 、
、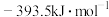 ,则表示
,则表示 标准摩尔生成焓的热化学反应方程式为
标准摩尔生成焓的热化学反应方程式为___________ 。
(2) 与
与 在某催化剂作用下的反应如图所示:
在某催化剂作用下的反应如图所示:
该反应的热化学反应方程式为___________ 。
(3)汽车尾气中的 和
和 在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。
在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。
(4) 与
与 可发生反应:
可发生反应: ,2L密闭容器中通入
,2L密闭容器中通入
 和
和
 ,在不同催化剂(A、B)作用下,进行相同时间后,
,在不同催化剂(A、B)作用下,进行相同时间后, 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: 、
、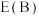 表示,则
表示,则
___________ 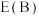 (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。
②y点对应的v(逆)___________ z点对应的v(正)。
③若w点的时间为5min,则 的平均反应速率为
的平均反应速率为___________  。此温度下的化学平衡常数为
。此温度下的化学平衡常数为___________ 。
(1)热力学规定,在标准压强和指定温度下,由元素最稳定的单质生成
 化合物时的反应热称为该化合物的标准摩尔生成焓。常温下,
化合物时的反应热称为该化合物的标准摩尔生成焓。常温下, 、
、 的标准摩尔生成焓分别为
的标准摩尔生成焓分别为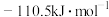 、
、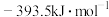 ,则表示
,则表示 标准摩尔生成焓的热化学反应方程式为
标准摩尔生成焓的热化学反应方程式为(2)
 与
与 在某催化剂作用下的反应如图所示:
在某催化剂作用下的反应如图所示: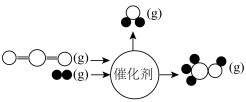
| 化学键 |
|
|
|
|
|
键能/( ) ) | 438 | 326 | 802 | 464 | 414 |
(3)汽车尾气中的
 和
和 在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。
在催化转化器中可反应生成两种无毒无害的气体(该反应为放热反应),若该反应在恒温、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到时刻达到平衡状态的是___________(填标号)。A.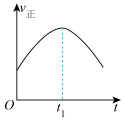 | B.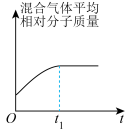 | C.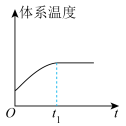 | D.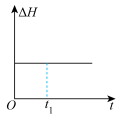 |
(4)
 与
与 可发生反应:
可发生反应: ,2L密闭容器中通入
,2L密闭容器中通入
 和
和
 ,在不同催化剂(A、B)作用下,进行相同时间后,
,在不同催化剂(A、B)作用下,进行相同时间后, 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: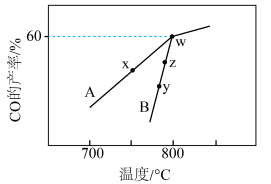
 、
、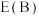 表示,则
表示,则
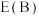 (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。②y点对应的v(逆)
③若w点的时间为5min,则
 的平均反应速率为
的平均反应速率为 。此温度下的化学平衡常数为
。此温度下的化学平衡常数为
您最近半年使用:0次
2 . 利用二氧化碳合成有机燃料是目前二氧化碳利用的研究方向。试回答以下问题:
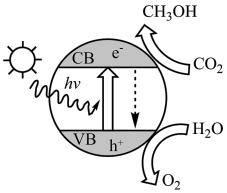
(1)如图为光催化转化二氧化碳的示意图,写出二氧化碳转化为甲醇的化学方程式___________ 。 :CO2(g)+3H2(g)
:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 

反应 :CO2(g)+H2(g)
:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g) 

试写出一氧化碳和氢气合成甲醇的热化学方程式___________ 。
(3)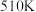 下,在压强为
下,在压强为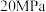 的恒压容器中通入
的恒压容器中通入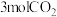 和
和 ,让其发生反应
,让其发生反应 后达到平衡,此时
后达到平衡,此时 的转化率为
的转化率为 ,则达到平衡时甲醇的物质的量分数为
,则达到平衡时甲醇的物质的量分数为___________ ,平衡常数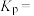
___________  (保留
(保留 位有效数字
位有效数字 。
。
(4)下图为在一定压强下二氧化碳与氢气合成甲醇时,二氧化碳的转化率和甲醇的选择性随温度的变化示意图: 随着温度的升高,二氧化碳的转化率升高而甲醇的选择性下降的原因是
随着温度的升高,二氧化碳的转化率升高而甲醇的选择性下降的原因是___________ 。
 对于反应
对于反应 来说,
来说, 点平衡常数
点平衡常数___________  填“
填“ ”“
”“ ”或者“
”或者“ ”
”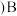 点平衡常数。
点平衡常数。
(5)下图为在 溶液中,通过电解的方法将二氧化碳转化为甲酸的机理图,试写出阴极的电极方程式
溶液中,通过电解的方法将二氧化碳转化为甲酸的机理图,试写出阴极的电极方程式___________ 。
(1)如图为光催化转化二氧化碳的示意图,写出二氧化碳转化为甲醇的化学方程式
 :CO2(g)+3H2(g)
:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 

反应
 :CO2(g)+H2(g)
:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g) 

试写出一氧化碳和氢气合成甲醇的热化学方程式
(3)
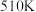 下,在压强为
下,在压强为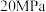 的恒压容器中通入
的恒压容器中通入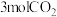 和
和 ,让其发生反应
,让其发生反应 后达到平衡,此时
后达到平衡,此时 的转化率为
的转化率为 ,则达到平衡时甲醇的物质的量分数为
,则达到平衡时甲醇的物质的量分数为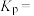
 (保留
(保留 位有效数字
位有效数字 。
。(4)下图为在一定压强下二氧化碳与氢气合成甲醇时,二氧化碳的转化率和甲醇的选择性随温度的变化示意图:
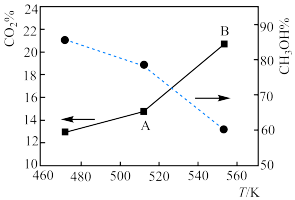
 随着温度的升高,二氧化碳的转化率升高而甲醇的选择性下降的原因是
随着温度的升高,二氧化碳的转化率升高而甲醇的选择性下降的原因是 对于反应
对于反应 来说,
来说, 点平衡常数
点平衡常数 填“
填“ ”“
”“ ”或者“
”或者“ ”
”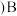 点平衡常数。
点平衡常数。(5)下图为在
 溶液中,通过电解的方法将二氧化碳转化为甲酸的机理图,试写出阴极的电极方程式
溶液中,通过电解的方法将二氧化碳转化为甲酸的机理图,试写出阴极的电极方程式
您最近半年使用:0次
解题方法
3 . 甲烷干重整(DRM)是利用 和
和 在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
Ⅰ.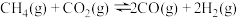
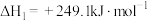
Ⅱ.
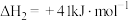
该过程中还伴随积碳反应的发生。
(1)一定压强下,由最稳定单质生成 化合物的焓变为该物质的摩尔生成焓。已知
化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为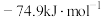 、
、 。则
。则 的摩尔生成焓为
的摩尔生成焓为_______  。
。
(2)甲烷和二氧化碳的起始物质的量均为 ,实验测得在
,实验测得在 下,平衡时各组分的量随温度变化如图所示。
下,平衡时各组分的量随温度变化如图所示。_______ mol,反应Ⅱ的压强平衡常数
_______ 。
②为了消除积碳带来的影响,反应选择在_______ (填“高温”或“低温”)下进行。
(3)在不同压强下,按照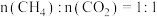 投料,假设只发生反应Ⅰ和Ⅱ。
投料,假设只发生反应Ⅰ和Ⅱ。 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。 、
、 、
、 ,三者由大到小顺序为
,三者由大到小顺序为________ 。
②压强 、
、 、
、 、
、 由小到大的顺序为
由小到大的顺序为________ 。
③ ,四条曲线几乎交于一点的原因是
,四条曲线几乎交于一点的原因是________ 。
 和
和 在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:Ⅰ.
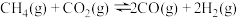
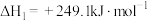
Ⅱ.

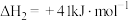
该过程中还伴随积碳反应的发生。
(1)一定压强下,由最稳定单质生成
 化合物的焓变为该物质的摩尔生成焓。已知
化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为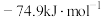 、
、 。则
。则 的摩尔生成焓为
的摩尔生成焓为 。
。(2)甲烷和二氧化碳的起始物质的量均为
 ,实验测得在
,实验测得在 下,平衡时各组分的量随温度变化如图所示。
下,平衡时各组分的量随温度变化如图所示。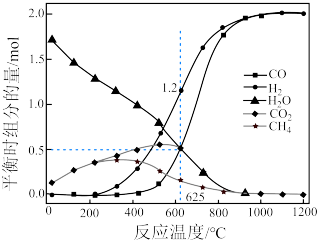

②为了消除积碳带来的影响,反应选择在
(3)在不同压强下,按照
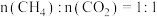 投料,假设只发生反应Ⅰ和Ⅱ。
投料,假设只发生反应Ⅰ和Ⅱ。 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。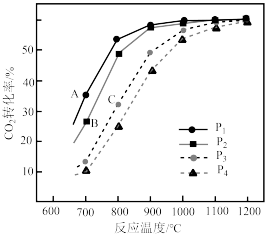
 、
、 、
、 ,三者由大到小顺序为
,三者由大到小顺序为②压强
 、
、 、
、 、
、 由小到大的顺序为
由小到大的顺序为③
 ,四条曲线几乎交于一点的原因是
,四条曲线几乎交于一点的原因是
您最近半年使用:0次
解题方法
4 . 燃煤脱硫是科研工作者的重要研究课题,石灰法是其中之一,相关反应如下:
请回答下列问题:
(1) 、
、 、
、 之间的关系为
之间的关系为
___________ (用含 、
、 的代数式表示);图中能表示
的代数式表示);图中能表示 随
随 变化的直线为
变化的直线为___________ (填“Ⅰ”或“Ⅱ”)。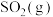 、
、 ,并加入足量的
,并加入足量的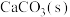 ,总压强保持8MPa不变的条件下仅发生上述反应ⅲ,测得在两种温度下
,总压强保持8MPa不变的条件下仅发生上述反应ⅲ,测得在两种温度下 的平衡转化率
的平衡转化率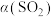 与混合气体的投料比
与混合气体的投料比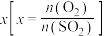 之间的关系如图所示。
之间的关系如图所示。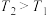 ,理由是
,理由是___________ 。
②在 温度下,该反应的平衡常数
温度下,该反应的平衡常数
___________  (用分数表示,
(用分数表示, 是用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
是用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
③其他条件不变,若向M点反应体系中充入一定量的 (
( 不参与反应),则
不参与反应),则 的平衡转化率
的平衡转化率___________ (填“增大”“减小”或“不变”),原因是___________ 。
| 相关反应 | 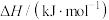 | 平衡常数( ) ) | |
| ⅰ | 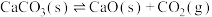 |  |  |
| ⅱ | 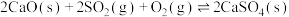 |  |  |
| ⅲ | 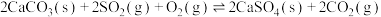 |  |  |
(1)
 、
、 、
、 之间的关系为
之间的关系为
 、
、 的代数式表示);图中能表示
的代数式表示);图中能表示 随
随 变化的直线为
变化的直线为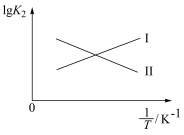
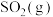 、
、 ,并加入足量的
,并加入足量的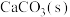 ,总压强保持8MPa不变的条件下仅发生上述反应ⅲ,测得在两种温度下
,总压强保持8MPa不变的条件下仅发生上述反应ⅲ,测得在两种温度下 的平衡转化率
的平衡转化率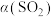 与混合气体的投料比
与混合气体的投料比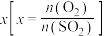 之间的关系如图所示。
之间的关系如图所示。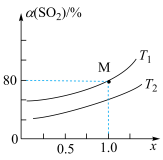
 ,理由是
,理由是②在
 温度下,该反应的平衡常数
温度下,该反应的平衡常数
 (用分数表示,
(用分数表示, 是用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。
是用平衡分压代替平衡浓度计算的平衡常数,分压=总压×物质的量分数)。③其他条件不变,若向M点反应体系中充入一定量的
 (
( 不参与反应),则
不参与反应),则 的平衡转化率
的平衡转化率
您最近半年使用:0次
解题方法
5 . 在催化剂的作用下,利用合成气(主要成分为CO、 和
和 )合成甲醇时涉及了如下反应:
)合成甲醇时涉及了如下反应:
反应Ⅰ.
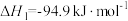
反应Ⅱ.
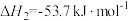
反应Ⅲ.
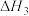
回答下列问题:
(1)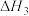 =
=______  。
。
某温度下,盛有1mol CO的密闭容器通入 发生反应Ⅰ,测得平衡时
发生反应Ⅰ,测得平衡时 (g)的体积分数变化如图所示。
(g)的体积分数变化如图所示。 转化率最大的是
转化率最大的是_______ (填字母)。
(3)图中,n=______ mol,此时CO的转化率为50%,反应体系总压为pPa,则该温度下反应Ⅰ的平衡常数Kp=____ Pa-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
一定条件下,某密闭容器中投入1mol 和3mol
和3mol 发生反应Ⅱ和Ⅲ。
发生反应Ⅱ和Ⅲ。
(4)升高反应体系温度,合成甲醇的反应速率______ (填“增大”“减小”或“不变”)。
(5)加入少量CO,平衡时甲醇的量____ (填“增多”“减少”或“不变”)。
(6)达到平衡后,缩小容器体积,反应Ⅲ的平衡______ (填“正向”“逆向”或“不”)移动。
改变温度和投气比[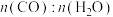 ]发生反应:
]发生反应: ,测得CO平衡转化率如表所示(其他反应条件相同)。
,测得CO平衡转化率如表所示(其他反应条件相同)。
(7)a、b、c三点对应的反应温度由高到低顺序是_____ 。
研究表明,反应 的速率方程为
的速率方程为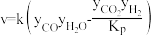 ,式中yCO、yH2O、yCO2、yH2分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。
,式中yCO、yH2O、yCO2、yH2分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。 时v逐渐减小的原因是
时v逐渐减小的原因是________ 。
 和
和 )合成甲醇时涉及了如下反应:
)合成甲醇时涉及了如下反应:反应Ⅰ.

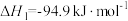
反应Ⅱ.

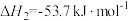
反应Ⅲ.

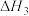
回答下列问题:
(1)
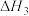 =
= 。
。某温度下,盛有1mol CO的密闭容器通入
 发生反应Ⅰ,测得平衡时
发生反应Ⅰ,测得平衡时 (g)的体积分数变化如图所示。
(g)的体积分数变化如图所示。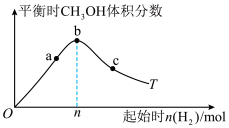
 转化率最大的是
转化率最大的是(3)图中,n=
一定条件下,某密闭容器中投入1mol
 和3mol
和3mol 发生反应Ⅱ和Ⅲ。
发生反应Ⅱ和Ⅲ。(4)升高反应体系温度,合成甲醇的反应速率
(5)加入少量CO,平衡时甲醇的量
(6)达到平衡后,缩小容器体积,反应Ⅲ的平衡
改变温度和投气比[
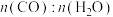 ]发生反应:
]发生反应: ,测得CO平衡转化率如表所示(其他反应条件相同)。
,测得CO平衡转化率如表所示(其他反应条件相同)。| 平衡点 | a | b | c |
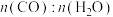 | 0.5 | 0.5 | 1 |
| CO平衡转化率 | 50 | 33.3 | 50 |
(7)a、b、c三点对应的反应温度由高到低顺序是
研究表明,反应
 的速率方程为
的速率方程为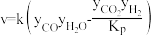 ,式中yCO、yH2O、yCO2、yH2分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。
,式中yCO、yH2O、yCO2、yH2分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。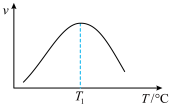
 时v逐渐减小的原因是
时v逐渐减小的原因是
您最近半年使用:0次
6 . 将 还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
Ⅰ.用铜铝催化剂可将 加氢合成甲醇,已知过程中发生的反应如下:
加氢合成甲醇,已知过程中发生的反应如下:
ⅰ.


ⅱ.


ⅲ.


(1)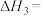
_____ (用含 、
、 的代数式表示),
的代数式表示),
_____ (用含 、
、 的代数式表示)。
的代数式表示)。
(2)查阅资料可知, ,则
,则_____ (填“低温"“商温”或“任意温度”)条件下有利于反应ⅲ自发进行。
Ⅱ. 和
和 以1:3的物质的量之比通入某密闭容器中,仅发生反应
以1:3的物质的量之比通入某密闭容器中,仅发生反应 ,
, 的平衡转化率与温度、气体的总压强的关系如图所示:
的平衡转化率与温度、气体的总压强的关系如图所示: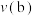
______ (填“>”“<”或“=”)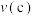 。
。
(4)平衡常数: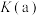
____ (填“>”“<”或“=”)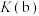 。
。
(5)压强:
______ (填“>”“<”或“=”) 。
。
(6)b点时,该反应的平衡常数
______ (分压=总压×物质的量分数,用含x、 的代数式表示)。
的代数式表示)。
Ⅲ.常温下,CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示: 和
和 的体积比为
的体积比为______ 。
 还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:
还原转化为有用的化学产品是目前研究的热点之一、回答下列问题:Ⅰ.用铜铝催化剂可将
 加氢合成甲醇,已知过程中发生的反应如下:
加氢合成甲醇,已知过程中发生的反应如下:ⅰ.



ⅱ.



ⅲ.



(1)
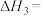
 、
、 的代数式表示),
的代数式表示),
 、
、 的代数式表示)。
的代数式表示)。(2)查阅资料可知,
 ,则
,则Ⅱ.
 和
和 以1:3的物质的量之比通入某密闭容器中,仅发生反应
以1:3的物质的量之比通入某密闭容器中,仅发生反应 ,
, 的平衡转化率与温度、气体的总压强的关系如图所示:
的平衡转化率与温度、气体的总压强的关系如图所示:
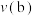
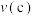 。
。(4)平衡常数:
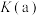
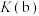 。
。(5)压强:

 。
。(6)b点时,该反应的平衡常数

 的代数式表示)。
的代数式表示)。Ⅲ.常温下,CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
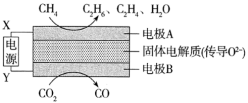
 和
和 的体积比为
的体积比为
您最近半年使用:0次
7 . 某团队报道了高温富水环境下,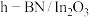 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:
i.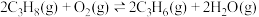

ii.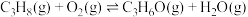

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因___________ 。
(2)已知:丙烷、丙烯的燃烧热分别为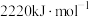 、
、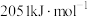 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
___________  。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是___________ (填标号)。
A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
①一定温度下,反应速率与浓度( )关系如下表所示:
)关系如下表所示:
根据数据计算,α+β+γ+δ=___________ 。
②速率常数与温度、活化能关系式为 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图:___________ (填“Cat1”或“Cat2”)。
(4)在密闭容器中充入 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:___________ 。
② 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为___________ 。
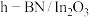 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:i.
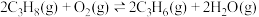

ii.
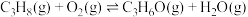

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、
 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因(2)已知:丙烷、丙烯的燃烧热分别为
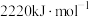 、
、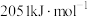 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
 。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为
 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。①一定温度下,反应速率与浓度(
 )关系如下表所示:
)关系如下表所示:| 序号 |  | 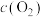 | 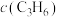 | 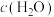 | v |
| Ⅰ | 0.1 | 0.1 | 0.1 | 0.1 | k |
| Ⅱ | 0.2 | 0.1 | 0.1 | 0.1 | 4k |
| Ⅲ | 0.2 | 0.4 | 0.1 | 0.1 | 8k |
| Ⅳ | 0.4 | 0.1 | 0.2 | 0.1 | 8k |
| Ⅴ | 0.4 | 0.4 | 0.1 | 0.2 | 16k |
②速率常数与温度、活化能关系式为
 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图: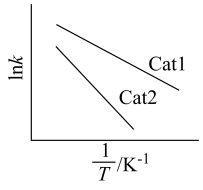
(4)在密闭容器中充入
 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示: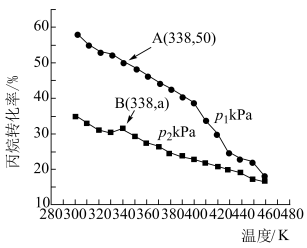
②
 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为
您最近半年使用:0次
名校
解题方法
8 . 回答下列问题
(1)已知:
则2H2(g)+O2(g) =2H2O(g) ΔH=___________ kJ·mol-1。
(2)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:

①N2(g)+O2(g) =2NO(g) ΔH1=___________
②2CO(g)+O2(g) = 2CO2(g) ΔH2=-565 kJ·mol-1
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式:___________ 。
(3)CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。
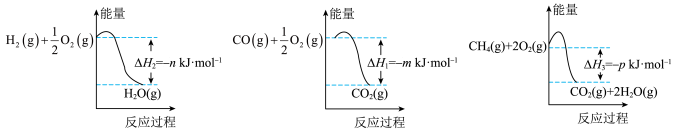
CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。
(4)下图是锌锰干电池基本构造图,
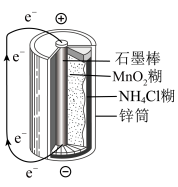
该电池的负极材料是___________ ,工作时NH 在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是___________ ;电路中每通过0.2 mol e-,负极质量减少___________ 。
(1)已知:
| 化学键 | H-H | O=O | O-H |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
(2)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:

①N2(g)+O2(g) =2NO(g) ΔH1=
②2CO(g)+O2(g) = 2CO2(g) ΔH2=-565 kJ·mol-1
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式:
(3)CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。

CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为
(4)下图是锌锰干电池基本构造图,

该电池的负极材料是
 在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
您最近半年使用:0次
9 . 一氯甲烷主要用于生产甲基氯硅烷,一氯乙烯主要用于生产聚氯乙烯等高聚物,1,2-二氯乙烷常用作有机溶剂和化工原料。回答下列问题:
I.在加热或光照条件下,“甲烷一氯气”法得到一氯甲烷是按自由基机理进行的,即CH4(g)+Cl2(g) CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
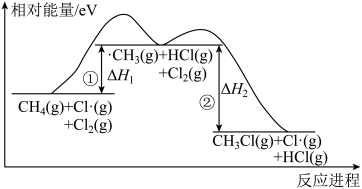
(1)已知H3C-H键能为4.56eV,H-Cl键能为4.46eV,1eV相当于96.5kJ/mol。则步骤①的焓变△H1=_______ kJ/mol;一氯取代反应的总焓变△H=______ (用△H1、△H2表示)。
Ⅱ.一氯乙烯(CH2=CHC1)的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
乙烯氯化加成:CH2=CH2(g)+Cl2(g) ClCH2CH2Cl(g) △H1=-171.7kJ/mol
ClCH2CH2Cl(g) △H1=-171.7kJ/mol
1,2-二氯乙烷裂解:ClCH2CH2Cl(g) CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol
CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol
(2)乙烯氯化加成反应在热力学上进行的趋势很大,原因是______ 。1,2-二氯乙烷裂解反应的△S=+145.7J mol/K,则该裂解反应能自发进行的最低温度约为
mol/K,则该裂解反应能自发进行的最低温度约为______ K(保留整数)。
(3)在某恒压密闭容器中通入一定量的ClCH2CH2Cl(g),仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢,实验测得ClCH2CH2Cl(g)的转化率随温度和反应时间的关系如图所示。

①T1、T2、T3的大小关系为_______ ,原因是_______ 。
②若M点刚好达到平衡状态,则N点的v正_____ v逆(填“大于”“小于”或“等于”)。Ka是以物质的量分数表示的平衡常数,则T2温度下1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应的Kx=_____ 保留2位小数)。
Ⅲ.一种电化学合成1,2-二氯乙婉的实验装置如图所示
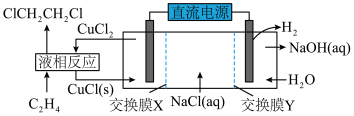
(4)交换膜X是______ 离子交换膜(填“阴”或“阳”),该实验装置合成1,2-二氯乙烷的总反应的化学方程式为______ 。
I.在加热或光照条件下,“甲烷一氯气”法得到一氯甲烷是按自由基机理进行的,即CH4(g)+Cl2(g)
 CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
(1)已知H3C-H键能为4.56eV,H-Cl键能为4.46eV,1eV相当于96.5kJ/mol。则步骤①的焓变△H1=
Ⅱ.一氯乙烯(CH2=CHC1)的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
乙烯氯化加成:CH2=CH2(g)+Cl2(g)
 ClCH2CH2Cl(g) △H1=-171.7kJ/mol
ClCH2CH2Cl(g) △H1=-171.7kJ/mol1,2-二氯乙烷裂解:ClCH2CH2Cl(g)
 CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol
CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol(2)乙烯氯化加成反应在热力学上进行的趋势很大,原因是
 mol/K,则该裂解反应能自发进行的最低温度约为
mol/K,则该裂解反应能自发进行的最低温度约为(3)在某恒压密闭容器中通入一定量的ClCH2CH2Cl(g),仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢,实验测得ClCH2CH2Cl(g)的转化率随温度和反应时间的关系如图所示。

①T1、T2、T3的大小关系为
②若M点刚好达到平衡状态,则N点的v正
Ⅲ.一种电化学合成1,2-二氯乙婉的实验装置如图所示

(4)交换膜X是
您最近半年使用:0次
2024-03-18更新
|
118次组卷
|
2卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题
名校
10 . “21世纪的清洁燃料”二甲醚具有含氢量高,廉价易得,无毒等优点。回答下列问题:
(1)以 、
、 为原料制备二甲醚(CH3OCH3)涉及的主要反应如下:
为原料制备二甲醚(CH3OCH3)涉及的主要反应如下:
i.
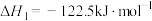 ;
;
ⅱ.
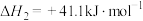 。
。
反应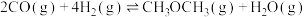 的
的 =
=______ 。
(2)二甲醚水蒸气重整制氢体系中会发生如下反应:
主反应: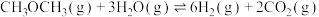
副反应: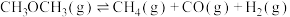

温度为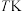 时,向压强为
时,向压强为 的恒压体系中按物质的量之比为1:3充入
的恒压体系中按物质的量之比为1:3充入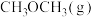 、
、 ,测得在催化剂HZSM-5催化下反应达到平衡时,二甲醚转化率为25%,且产物中
,测得在催化剂HZSM-5催化下反应达到平衡时,二甲醚转化率为25%,且产物中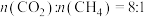 。
。
①能判断主反应达到平衡状态的标志为______ (填字母)。
A.混合气体中各物质分压保持不变 B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变 D.消耗1mol 时,有2molCO2生成
时,有2molCO2生成
②反应达到平衡时, 的转化率为
的转化率为______ ,二甲醚水蒸气重整制氢主反应的 =
=______ (列出含 的计算式即可,用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数)。
的计算式即可,用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数)。
③已知主反应高温下可以自发进行,若升高反应温度,平衡时二甲醚的转化率______ (填“高于”或“低于”)25%。
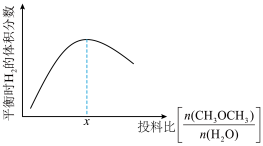
④温度压强不变,只改变反应物的投料比,平衡时 的体积分数变化趋势如图所示。投料比小于
的体积分数变化趋势如图所示。投料比小于 时,平衡时
时,平衡时 的体积分数变化趋势较投料比大于
的体积分数变化趋势较投料比大于 时更明显的原因是
时更明显的原因是____________ 。
(3)用惰性电极设计碱性二甲醚一氧气燃料电池,负极反应的电极反应式为____________ 。
(1)以
 、
、 为原料制备二甲醚(CH3OCH3)涉及的主要反应如下:
为原料制备二甲醚(CH3OCH3)涉及的主要反应如下:i.

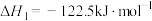 ;
;ⅱ.

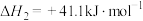 。
。反应
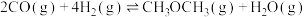 的
的 =
=(2)二甲醚水蒸气重整制氢体系中会发生如下反应:
主反应:
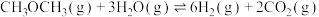
副反应:
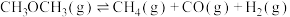

温度为
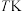 时,向压强为
时,向压强为 的恒压体系中按物质的量之比为1:3充入
的恒压体系中按物质的量之比为1:3充入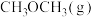 、
、 ,测得在催化剂HZSM-5催化下反应达到平衡时,二甲醚转化率为25%,且产物中
,测得在催化剂HZSM-5催化下反应达到平衡时,二甲醚转化率为25%,且产物中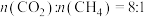 。
。①能判断主反应达到平衡状态的标志为
A.混合气体中各物质分压保持不变 B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变 D.消耗1mol
 时,有2molCO2生成
时,有2molCO2生成②反应达到平衡时,
 的转化率为
的转化率为 =
= 的计算式即可,用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数)。
的计算式即可,用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数)。③已知主反应高温下可以自发进行,若升高反应温度,平衡时二甲醚的转化率
④温度压强不变,只改变反应物的投料比,平衡时
 的体积分数变化趋势如图所示。投料比小于
的体积分数变化趋势如图所示。投料比小于 时,平衡时
时,平衡时 的体积分数变化趋势较投料比大于
的体积分数变化趋势较投料比大于 时更明显的原因是
时更明显的原因是
(3)用惰性电极设计碱性二甲醚一氧气燃料电池,负极反应的电极反应式为
您最近半年使用:0次