解题方法
1 . 应用盖斯定律的计算方法
(1)“虚拟路径”法
若反应物A变为生成物D,可以有两个途径
①由A直接变成D,反应热为ΔH;
②由A经过B变成C,再由C变成D,每步的反应热分别为ΔH1、ΔH2、ΔH3。
如图所示:
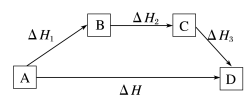
则有ΔH=_______ 。
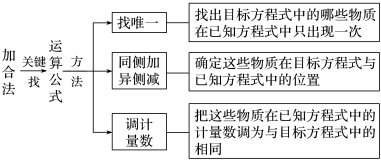
(2)加合法
加合法就是运用所给热化学方程式通过_______ 的方法得到所求的热化学方程式。
(1)“虚拟路径”法
若反应物A变为生成物D,可以有两个途径
①由A直接变成D,反应热为ΔH;
②由A经过B变成C,再由C变成D,每步的反应热分别为ΔH1、ΔH2、ΔH3。
如图所示:

则有ΔH=
(2)加合法
加合法就是运用所给热化学方程式通过

您最近一年使用:0次
2 . 盖斯定律的意义
应用盖斯定律可以_____ 以下情况(不能直接测定)的反应热:
(1)有些反应进行得很慢。
(2)有些反应不容易直接发生。
(3)有些反应的生成物不纯(有副反应发生)。
应用盖斯定律可以
(1)有些反应进行得很慢。
(2)有些反应不容易直接发生。
(3)有些反应的生成物不纯(有副反应发生)。
您最近一年使用:0次
解题方法
3 . 根据如下两个反应,选用上述两种方法,计算出C(s)+ O2(g)=CO(g)的反应热ΔH。
O2(g)=CO(g)的反应热ΔH。
I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
II.CO(g)+ O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
①“虚拟路径”法
反应C(s)+O2(g)=CO2(g)的途径可设计如下:
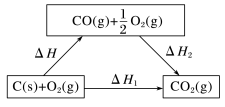
则ΔH=_______ =_______ kJ·mol-1。
②加合法
分析:找唯一:C、CO分别在I、II中出现一次
同侧加:C是I中反应物,为同侧,则“+I”
异侧减:CO是II中反应物,为异侧,则“-II”
调计量数:化学计量数相同,不用调整,则I-II即为运算式。所以ΔH=___ =___ kJ·mol-1。
 O2(g)=CO(g)的反应热ΔH。
O2(g)=CO(g)的反应热ΔH。I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
II.CO(g)+
 O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1①“虚拟路径”法
反应C(s)+O2(g)=CO2(g)的途径可设计如下:

则ΔH=
②加合法
分析:找唯一:C、CO分别在I、II中出现一次
同侧加:C是I中反应物,为同侧,则“+I”
异侧减:CO是II中反应物,为异侧,则“-II”
调计量数:化学计量数相同,不用调整,则I-II即为运算式。所以ΔH=
您最近一年使用:0次
4 . 盖斯定律的内容
大量实验证明,一个化学反应,不管是_____ 完成的还是____ 完成的,其反应热是_____ 的。换句话说,化学反应的反应热只与反应体系的_____ 和___ 有关,而与反应的____ 无关。
大量实验证明,一个化学反应,不管是
您最近一年使用:0次
名校
解题方法
5 . 下列说法不正确的是
| A.化学反应中一定伴随能量变化 |
| B.S在纯氧中燃烧是将全部化学能转化为热能 |
| C.物质所含化学键键能越大,其越稳定 |
| D.化学反应的∆H,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2021-01-28更新
|
902次组卷
|
7卷引用:课前-1.2 反应热的计算-课前、课中、课后(人教版2019选择性必修1)
课前-1.2 反应热的计算-课前、课中、课后(人教版2019选择性必修1)(已下线)第1章 化学反应的热效应(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)广东省佛山市南海区桂城中学2021-2022学年高二上学期第一次月考化学试题山东省济宁市微山县第二中学2021-2022学年高二上学期第一学段考试化学试题陕西省榆林市子洲中学2021-2022学年高二上学期期中考试化学试题广东省潮州湘桥区南春中学2021-2022学年高二上学期第一次月考化学试题黑龙江省嫩江市高级中学2020-2021学年高二上学期9月月考化学试题
名校
6 . 下列关于两个反应的△H的判断,正确的是
S(s)+O2(g)=SO2(g) △H1;2S(s)+3O2(g)=2SO3(g) △H2
S(s)+O2(g)=SO2(g) △H1;2S(s)+3O2(g)=2SO3(g) △H2
| A.△H1>0,△H2>0 | B.2△H1>△H2 |
| C.△H1<0,△H2>0 | D.△H2>△H1 |
您最近一年使用:0次
2020-10-24更新
|
446次组卷
|
3卷引用:课前-1.2 反应热的计算-课前、课中、课后(人教版2019选择性必修1)



