名校
1 . 铁及其化合物在生产、生活中有广泛的应用。
(1)中科院兰州化学物理研究所用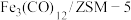 催化
催化 加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂
加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂 (也起催化作用)后可改变反应的选择性。
(也起催化作用)后可改变反应的选择性。
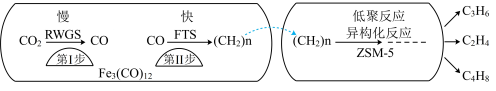
下列说法正确的是___________ 。
a.第1步所发生的反应为: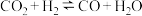
b.第1步反应的活化能低于第2步
c.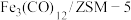 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小
d.添加不同助剂后,各反应的平衡常数不变
(2)纳米铁是重要的储氢材料,可用反应 制得。在
制得。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和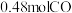 ,在
,在 不同温度下进行反应,测得
不同温度下进行反应,测得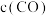 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。
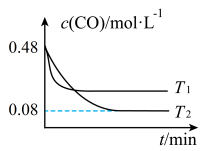

___________ 0(填“>”或“<”);
(3) 温度下,平衡时体系的压强为
温度下,平衡时体系的压强为 ,反应的标准平衡常数
,反应的标准平衡常数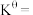
___________ (已知:标准平衡常数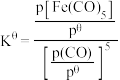 ,其中
,其中 为标准压强
为标准压强 为各组分的平衡分压。)
为各组分的平衡分压。)
(4)高铁酸钾 被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
①电解法可制得 ,装置如图,阳极电极反应式为
,装置如图,阳极电极反应式为___________ 。

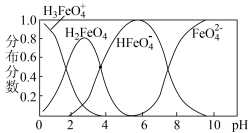
② 在水解过程中铁元素形成的微粒分布分数与
在水解过程中铁元素形成的微粒分布分数与 的关系如图所示,向
的关系如图所示,向 的溶液中加入
的溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(5)复合氧化物铁酸锰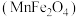 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下:
①

②

③

则: 与
与 、
、 的关系为
的关系为
___________
(1)中科院兰州化学物理研究所用
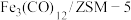 催化
催化 加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂
加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂 (也起催化作用)后可改变反应的选择性。
(也起催化作用)后可改变反应的选择性。
下列说法正确的是
a.第1步所发生的反应为:
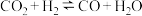
b.第1步反应的活化能低于第2步
c.
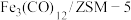 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小d.添加不同助剂后,各反应的平衡常数不变
(2)纳米铁是重要的储氢材料,可用反应
 制得。在
制得。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和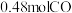 ,在
,在 不同温度下进行反应,测得
不同温度下进行反应,测得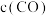 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。

(3)
 温度下,平衡时体系的压强为
温度下,平衡时体系的压强为 ,反应的标准平衡常数
,反应的标准平衡常数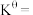
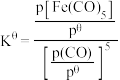 ,其中
,其中 为标准压强
为标准压强 为各组分的平衡分压。)
为各组分的平衡分压。)(4)高铁酸钾
 被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。①电解法可制得
 ,装置如图,阳极电极反应式为
,装置如图,阳极电极反应式为
②
 在水解过程中铁元素形成的微粒分布分数与
在水解过程中铁元素形成的微粒分布分数与 的关系如图所示,向
的关系如图所示,向 的溶液中加入
的溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
(5)复合氧化物铁酸锰
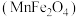 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下: ①


②


③


则:
 与
与 、
、 的关系为
的关系为
您最近一年使用:0次
解题方法
2 . 空间站内搭载萨巴蒂尔装置将 转化为
转化为 ,再通过电解水装置回收氧元素.其系统原理如图:
,再通过电解水装置回收氧元素.其系统原理如图:
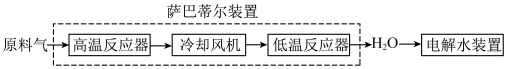
萨巴蒂尔装置内发生反应为
反应Ⅰ: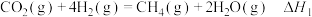
反应Ⅱ: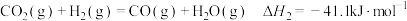
(1)已知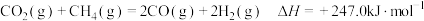 ,则
,则
_________ .
(2)在“高温反应器”中以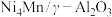 为催化剂,一段时间内不同温度
为催化剂,一段时间内不同温度 转化率如图.已知反应Ⅰ的速率方程:
转化率如图.已知反应Ⅰ的速率方程: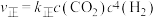 ,
, .
.
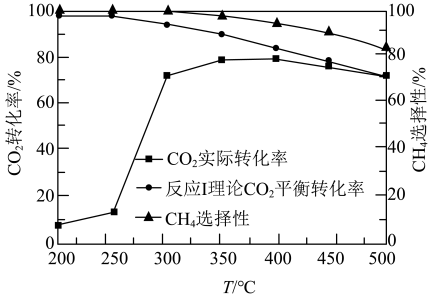
①250℃前, 实际转化率随温度变化不大的主要原因是
实际转化率随温度变化不大的主要原因是___________ .
②300℃时
__________ 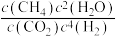 (填“>”“<”或“=”).
(填“>”“<”或“=”).
③达到平衡后,升高温度, 增大的倍数
增大的倍数_________  增大的倍数(填“>”“<”或“=”).
增大的倍数(填“>”“<”或“=”).
(3)在“低温反应器”中达平衡时,各组分物质的量分数随温度变化如图.已知原料气中含有 及
及 .
.
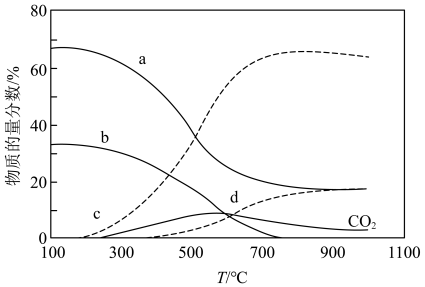
① 物质的量分数随温度变化的曲线为
物质的量分数随温度变化的曲线为____________ (填标号).
②300~500℃, 物质的量分数随温度升高而上升的原因是
物质的量分数随温度升高而上升的原因是___________ .
③某温度下达平衡时,总压为 ,剩余
,剩余 和
和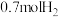 ,则反应Ⅰ的
,则反应Ⅰ的 为
为___________ (列出计算式, 为以分压表示的平衡常数,分压=总压×物质的量分数);
为以分压表示的平衡常数,分压=总压×物质的量分数);
此时氧元素的回收率为____________ [回收率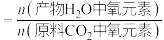 ].
].
(4)从平衡与速率角度分析萨巴蒂尔装置采用高温和低温反应器串联的优点是___________ .
 转化为
转化为 ,再通过电解水装置回收氧元素.其系统原理如图:
,再通过电解水装置回收氧元素.其系统原理如图:
萨巴蒂尔装置内发生反应为
反应Ⅰ:
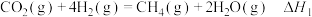
反应Ⅱ:
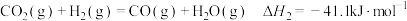
(1)已知
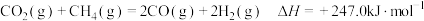 ,则
,则
(2)在“高温反应器”中以
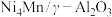 为催化剂,一段时间内不同温度
为催化剂,一段时间内不同温度 转化率如图.已知反应Ⅰ的速率方程:
转化率如图.已知反应Ⅰ的速率方程: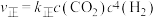 ,
, .
.
①250℃前,
 实际转化率随温度变化不大的主要原因是
实际转化率随温度变化不大的主要原因是②300℃时

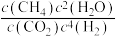 (填“>”“<”或“=”).
(填“>”“<”或“=”).③达到平衡后,升高温度,
 增大的倍数
增大的倍数 增大的倍数(填“>”“<”或“=”).
增大的倍数(填“>”“<”或“=”).(3)在“低温反应器”中达平衡时,各组分物质的量分数随温度变化如图.已知原料气中含有
 及
及 .
.
①
 物质的量分数随温度变化的曲线为
物质的量分数随温度变化的曲线为②300~500℃,
 物质的量分数随温度升高而上升的原因是
物质的量分数随温度升高而上升的原因是③某温度下达平衡时,总压为
 ,剩余
,剩余 和
和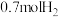 ,则反应Ⅰ的
,则反应Ⅰ的 为
为 为以分压表示的平衡常数,分压=总压×物质的量分数);
为以分压表示的平衡常数,分压=总压×物质的量分数);此时氧元素的回收率为
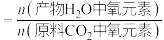 ].
].(4)从平衡与速率角度分析萨巴蒂尔装置采用高温和低温反应器串联的优点是
您最近一年使用:0次
解题方法
3 . 下列物质摩尔燃烧焓数据如下表:
下列表述正确的是
物质 | C(s,石墨) | C(s,金刚石) |
|
|
|
| -393.5 | -395.4 | -285.8 | -283.0 | -890.3 |
A.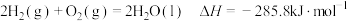 |
B.C(s,石墨)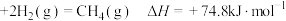 |
C.C(s,石墨)=C(s,金刚石)  |
D.C(s,石墨)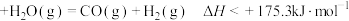 |
您最近一年使用:0次
4 . 二氧化碳的回收利用是环保领域研究的热点课题。结合所学知识回答下列问题:
Ⅰ.利用太阳能实现 制取某些物质是一种非常理想的
制取某些物质是一种非常理想的 减排途径。
减排途径。
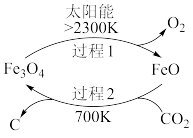
(1)在太阳能的作用下,以 为原料制取炭黑的流程如图所示。其总反应的化学方程式为
为原料制取炭黑的流程如图所示。其总反应的化学方程式为___________ 。
(2)以稀硫酸为电解质溶液,利用太阳能将 转化为低碳烯烃,工作原理如图:
转化为低碳烯烃,工作原理如图:
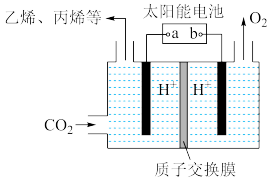
①b是电源的___________ (填“正”或“负”)极。
②生成乙烯( )的电极反应式为
)的电极反应式为___________ 。
③电场作用下,氢离子从___________ (填:“从左到右”或“从右到左”)移动。
Ⅱ.通过化学的方法实现 的资源化利用也是一种非常理想的
的资源化利用也是一种非常理想的 减排途径。
减排途径。
(3)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
 ;
;
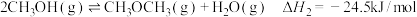 。
。
则 反应的
反应的
___________  。
。
(4)已知该反应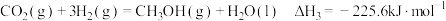 ,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
(5)工业上用 和
和 反应合成甲醇
反应合成甲醇
 ,在2L刚性密闭容器中,不同温度、不同投料比时,
,在2L刚性密闭容器中,不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。 温度下,将
温度下,将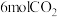 和
和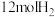 充入该密闭容器中,
充入该密闭容器中, 后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为
后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为___________ ;反应的平衡常数
___________ ,从图中可知:
___________  (填>或<或=,判断的依据是
(填>或<或=,判断的依据是___________ , 、
、 、
、 三者之间的大小关系为
三者之间的大小关系为___________ 。
Ⅰ.利用太阳能实现
 制取某些物质是一种非常理想的
制取某些物质是一种非常理想的 减排途径。
减排途径。(1)在太阳能的作用下,以
 为原料制取炭黑的流程如图所示。其总反应的化学方程式为
为原料制取炭黑的流程如图所示。其总反应的化学方程式为
(2)以稀硫酸为电解质溶液,利用太阳能将
 转化为低碳烯烃,工作原理如图:
转化为低碳烯烃,工作原理如图:
①b是电源的
②生成乙烯(
 )的电极反应式为
)的电极反应式为③电场作用下,氢离子从
Ⅱ.通过化学的方法实现
 的资源化利用也是一种非常理想的
的资源化利用也是一种非常理想的 减排途径。
减排途径。(3)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: ;
;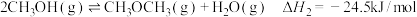 。
。则
 反应的
反应的
 。
。(4)已知该反应
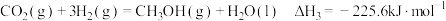 ,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。A. 和 和 的物质的量浓度之比是 的物质的量浓度之比是 |
| B.容器中混合气体的平均摩尔质量保持不变 |
| C.容器中混合气体的体积保持不变 |
D. 的消耗速率等于 的消耗速率等于 的生成速率的3倍 的生成速率的3倍 |
(5)工业上用
 和
和 反应合成甲醇
反应合成甲醇 ,在2L刚性密闭容器中,不同温度、不同投料比时,
,在2L刚性密闭容器中,不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。 温度下,将
温度下,将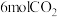 和
和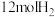 充入该密闭容器中,
充入该密闭容器中, 后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为
后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为

 (填>或<或=,判断的依据是
(填>或<或=,判断的依据是 、
、 、
、 三者之间的大小关系为
三者之间的大小关系为
您最近一年使用:0次
名校
解题方法
5 . 氨氮的生成与消除都具有重要意义。
(1)电催化氮气还原合成氨是一种常温常压条件下利用水作为氢源的低碳环保路线,电催化合成氨装置如图:
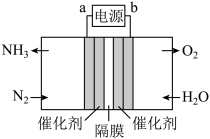
①a为___________ 极。
②该装置总反应化学方程式为___________ 。
(2)微生物燃料电池(MFC)是一种现代化氨氮去除技术,MFC碳氮联合同时去除的氮转化系统原理如图。
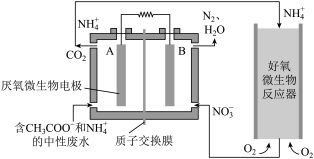
① A极的电极反应式为___________ 。
② H+通过质子交换膜向___________ (填“A”或“B”)电极区溶液移动。
③ 在好氧微生物反应器中,转化0.5mol NH ,转移的电子数目为
,转移的电子数目为___________ 。
(3)NH3(g)燃烧生成NO2和H2O,已知
①H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ/mol
O2(g)=H2O(g) ΔH=-241.8kJ/mol
②N2(g)+2O2(g)=2NO2(g) ΔH=+33.9kJ/mol
③ N2(g)+
N2(g)+ H2(g)=NH3(g) ΔH=-46.0kJ/mol
H2(g)=NH3(g) ΔH=-46.0kJ/mol
④H2O(l)=H2O(g) ΔH=+44kJ/mol
则NH3(g)的燃烧热的热化学方程式:___________ 。
(1)电催化氮气还原合成氨是一种常温常压条件下利用水作为氢源的低碳环保路线,电催化合成氨装置如图:

①a为
②该装置总反应化学方程式为
(2)微生物燃料电池(MFC)是一种现代化氨氮去除技术,MFC碳氮联合同时去除的氮转化系统原理如图。

① A极的电极反应式为
② H+通过质子交换膜向
③ 在好氧微生物反应器中,转化0.5mol NH
 ,转移的电子数目为
,转移的电子数目为(3)NH3(g)燃烧生成NO2和H2O,已知
①H2(g)+
 O2(g)=H2O(g) ΔH=-241.8kJ/mol
O2(g)=H2O(g) ΔH=-241.8kJ/mol②N2(g)+2O2(g)=2NO2(g) ΔH=+33.9kJ/mol
③
 N2(g)+
N2(g)+ H2(g)=NH3(g) ΔH=-46.0kJ/mol
H2(g)=NH3(g) ΔH=-46.0kJ/mol④H2O(l)=H2O(g) ΔH=+44kJ/mol
则NH3(g)的燃烧热的热化学方程式:
您最近一年使用:0次
解题方法
6 .  和
和 是环境污染性气体,可在
是环境污染性气体,可在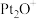 表面转化为无害气体,有关化学反应的物质变化过程如图1所示,能量变化过程如图2所示,下列说法正确的是
表面转化为无害气体,有关化学反应的物质变化过程如图1所示,能量变化过程如图2所示,下列说法正确的是
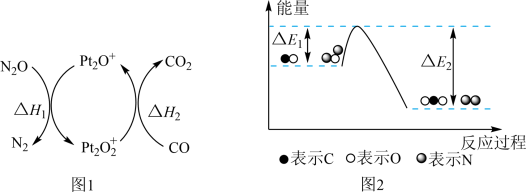
 和
和 是环境污染性气体,可在
是环境污染性气体,可在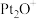 表面转化为无害气体,有关化学反应的物质变化过程如图1所示,能量变化过程如图2所示,下列说法正确的是
表面转化为无害气体,有关化学反应的物质变化过程如图1所示,能量变化过程如图2所示,下列说法正确的是
A.加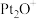 ,可使反应的 ,可使反应的 减小 减小 |
B.总反应的 |
C.该反应的方程式是: |
D.总反应的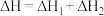 |
您最近一年使用:0次
7 . 下列科学家与其贡献匹配错误的是
| A.侯德榜——联合制碱 | B.盖斯——平衡移动原理 |
| C.徐光宪——稀土元素分离及应用 | D.门捷列夫——元素周期表 |
您最近一年使用:0次
2021-06-12更新
|
246次组卷
|
3卷引用:福建省莆田市锦江中学2023-2024学年高二上学期期末考试化学试题