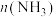1 . 回答下列问题
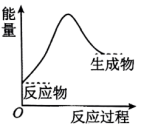
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是________ (填序号)。
b.盐酸与碳酸氢钠
c.碳酸钙分解
d. 固体与
固体与 固体
固体
e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼( )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:
该反应属于________ 反应(填“放热”或“吸热”), 和
和 的总能量
的总能量________ (填“>”“=”或“<”) 和
和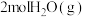 的总能量。
的总能量。
(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。________ (填化学式),负极的电极反应式为________ 。
②电池工作时, 移向
移向________ 电极(填“a”或“b”)。
③当b电极上消耗标况下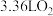 时,电路中转移的电子数为
时,电路中转移的电子数为________ 。
(4)肼( )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式________ 。
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是
b.盐酸与碳酸氢钠
c.碳酸钙分解
d.
 固体与
固体与 固体
固体e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼(
 )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:化学键 | N-H | N-N | N≡N | O=O | O-H |
能量 | 391 | 154 | 942 | 500 | 463 |
 和
和 的总能量
的总能量 和
和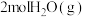 的总能量。
的总能量。(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。
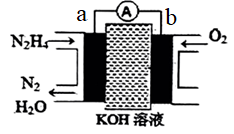
②电池工作时,
 移向
移向③当b电极上消耗标况下
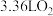 时,电路中转移的电子数为
时,电路中转移的电子数为(4)肼(
 )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
您最近一年使用:0次
2 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图示:________ 。
(2)若上述反应中X、Y、Z分别为 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入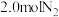 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:
0~50s内的平均反应速率
________ 。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为________ kJ/mol。
(4)CO与 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。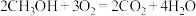 ,则c电极是
,则c电极是________ (填“正极”或“负极”)。若外电路中转移2mol电子,则上述燃料电池所消耗的 在标准状况下的体积为
在标准状况下的体积为________ L。
(5)下列反应中,属于吸热反应的是________ (填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥ 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应

(2)若上述反应中X、Y、Z分别为
 、
、 、
、 ,某温度下,在容积恒定为2.0L的密闭容器中充入
,某温度下,在容积恒定为2.0L的密闭容器中充入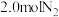 和
和 ,一段时间后反应达平衡状态,实验数据如表所示:
,一段时间后反应达平衡状态,实验数据如表所示:t/s | 0 | 50 | 150 | 250 | 350 |
| 0 | 0.36 | 0.48 | 0.50 | 0.50 |

(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成
 过程中放出46kJ的热量。则N≡N的键能为
过程中放出46kJ的热量。则N≡N的键能为(4)CO与
 反应可制备
反应可制备 ,由
,由 和
和 构成的质子交换膜燃料电池的结构示意图如下。
构成的质子交换膜燃料电池的结构示意图如下。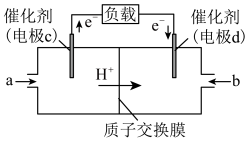
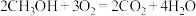 ,则c电极是
,则c电极是 在标准状况下的体积为
在标准状况下的体积为(5)下列反应中,属于吸热反应的是
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤食物因氧化而腐败
⑥
 与
与 反应 ⑦铁粉与稀盐酸反应
反应 ⑦铁粉与稀盐酸反应
您最近一年使用:0次
2024-05-04更新
|
287次组卷
|
2卷引用:山东省威海市乳山市银滩高级中学2023-2024学年高一下学期3月月考化学试题
3 . 已知反应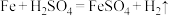 ,下列叙述不正确的是
,下列叙述不正确的是
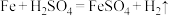 ,下列叙述不正确的是
,下列叙述不正确的是
| A.可将该反应设计成如图甲所示的原电池 |
| B.反应过程中能量关系可用图乙表示 |
| C.若Fe不纯(含有杂质碳),该反应的化学反应速率要减慢 |
D.图甲装置中, 在铜表面被还原产生气泡 在铜表面被还原产生气泡 |
您最近一年使用:0次
名校
4 . 下列说法正确的是
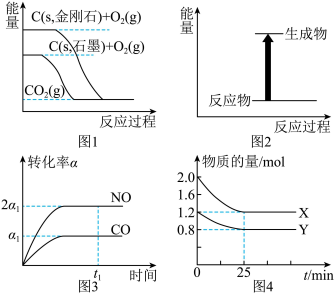
| A.由图1可知,金刚石比石墨稳定 |
| B.图2可表示碳酸氢钠和盐酸反应的能量变化 |
C.由图3可知,对于反应 ,当NO和CO转化率之比为2∶1时,可判断该反应已达到平衡状态 ,当NO和CO转化率之比为2∶1时,可判断该反应已达到平衡状态 |
D.由图4可知,对于反应 ,在0~25min内,用X表示的平均反应速率为0.032 ,在0~25min内,用X表示的平均反应速率为0.032 |
您最近一年使用:0次
名校
解题方法
5 . 下列选项中,有关实验操作、现象和结论错误的是
| 实验操作 | 现象 | 结论 | |
| A | 取无色溶液做焰色实验 | 火焰为黄色 | 该溶液中一定有 可能有 可能有 |
| B | 将 气体通入碳酸钠溶液中 气体通入碳酸钠溶液中 | 生成无色无味气体 | 非金属性硫比碳强 |
| C | 分别向两只盛有等体积等浓度的 、 、 溶液的试管中,逐滴加入相同浓度的 溶液的试管中,逐滴加入相同浓度的 溶液至过量 溶液至过量 |  溶液有白色沉淀、 溶液有白色沉淀、 溶液中无白色沉淀 溶液中无白色沉淀 | 金属性镁比铝强 |
| D | 将 固体与柠檬酸在烧杯中混合搅拌 固体与柠檬酸在烧杯中混合搅拌 | 烧杯壁变凉 | 该反应为吸热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 苯与 的催化反应历程如图所示,关于该反应历程,下列说法正确的是
的催化反应历程如图所示,关于该反应历程,下列说法正确的是
 的催化反应历程如图所示,关于该反应历程,下列说法正确的是
的催化反应历程如图所示,关于该反应历程,下列说法正确的是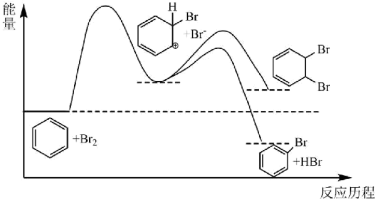
A.苯与 的催化反应一定为放热反应 的催化反应一定为放热反应 |
| B.使用催化剂可以降低该反应的活化能 |
C.该历程中,苯与 的催化反应可生成溴苯、邻二溴苯 的催化反应可生成溴苯、邻二溴苯 |
D.苯与 的催化反应主反应为取代反应,是因为从中间产物生成溴苯的反应速率较快 的催化反应主反应为取代反应,是因为从中间产物生成溴苯的反应速率较快 |
您最近一年使用:0次
7 . 化学变化常伴随能量变化,现有反应:
A. B.
B.
C. D.
D.
(1)上述四个反应中能设计成原电池的是________ (填字母)。
(2)根据该原电池回答下列问题:
①正极的电极反应式为________________________________________________ .
②当导线中有 电子通过时,理论上发生的变化是
电子通过时,理论上发生的变化是________ (填字母)。
a溶液增重32.5g b.溶液增重31.5g c.析出1g d.析出11.2L
d.析出11.2L
(3)燃料电池的工作原理是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极,
)反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极, 为燃料,采用氢氧化钠溶液为电解液,写出燃料电池负极的电极反应式
为燃料,采用氢氧化钠溶液为电解液,写出燃料电池负极的电极反应式_________________ 。
(4)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:________ (填“吸热”或“放热”)反应。
②若爆炸过程中有 非极性键生成(一个共用电子对为一个化学键),则反应放出的热量为
非极性键生成(一个共用电子对为一个化学键),则反应放出的热量为________ kJ(用含a、b的代数式表示)。
A.
 B.
B.
C.
 D.
D.
(1)上述四个反应中能设计成原电池的是
(2)根据该原电池回答下列问题:
①正极的电极反应式为
②当导线中有
 电子通过时,理论上发生的变化是
电子通过时,理论上发生的变化是a溶液增重32.5g b.溶液增重31.5g c.析出1g
 d.析出11.2L
d.析出11.2L
(3)燃料电池的工作原理是将燃料和氧化剂(如
 )反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极,
)反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极, 为燃料,采用氢氧化钠溶液为电解液,写出燃料电池负极的电极反应式
为燃料,采用氢氧化钠溶液为电解液,写出燃料电池负极的电极反应式(4)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:

②若爆炸过程中有
 非极性键生成(一个共用电子对为一个化学键),则反应放出的热量为
非极性键生成(一个共用电子对为一个化学键),则反应放出的热量为
您最近一年使用:0次
解题方法
8 . 2020年9月22日,国家主席习近平在第75届联合国大会上宣布:中国二氧化碳排放力争2030年前达到峰值,2060年前实现“碳中和”。为达成这一目标,另一方面要尽量吸收不可避免的碳排放。
(1)以TiO2为催化剂的光热化学循环分解CO2反应为吸收“碳排放”提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图1所示:_______ 转化为_______ 。
②根据数据计算,标准状况下2.24LCO2(g)分解生成CO(g)和O2(g)需要_______ (填“吸收”或“放出”)_______ kJ的能量。
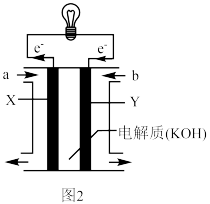
(2)CO2分解产生的CO和O2可以作为CO-O2燃料电池的原料。图2为CO-O2燃料电池的构造示意图,根据电子运动方向,可知氧气从_______ 口通入(填“a”或“b”),电极反应为_______ ;X极为电池的_______ (填“正”或“负”)极,电极反应为_______ ,K+向_______ 极移动(填“X”或“Y”)。
(1)以TiO2为催化剂的光热化学循环分解CO2反应为吸收“碳排放”提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图1所示:
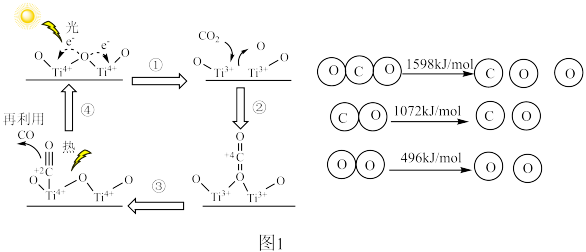
②根据数据计算,标准状况下2.24LCO2(g)分解生成CO(g)和O2(g)需要
(2)CO2分解产生的CO和O2可以作为CO-O2燃料电池的原料。图2为CO-O2燃料电池的构造示意图,根据电子运动方向,可知氧气从
您最近一年使用:0次
名校
解题方法
9 . 溴代叔丁烷与乙醇的反应进程中的能量变化如图所示。下列说法正确的是
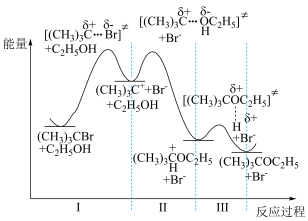
| A.溴代叔丁烷与乙醇的反应为吸热 |
| B.溴代叔丁烷和乙醇的总反应速率由反应Ⅲ决定 |
| C.氯代叔丁烷和乙醇中发生相似的反应,则反应I的活化能将增大 |
D.由该反应原理可推知,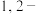 二溴乙烷和乙二醇反应可制得环丁烷 二溴乙烷和乙二醇反应可制得环丁烷 |
您最近一年使用:0次
2024-04-08更新
|
689次组卷
|
5卷引用:化学(山东卷01)-2024年高考押题预测卷
(已下线)化学(山东卷01)-2024年高考押题预测卷2024届山东省邹城市北大新世纪高级中学高三下学期第三次模拟考试化学试题湖南省益阳市2024届高三4月联考暨三模考试化学统考试题(已下线)题型8 反应热 电化学的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)湖南省衡阳市衡阳县第一中学2023-2024学年高三下学期4月月考化学试题
名校
10 . 意大利罗马大学的FulvioCacace等人获得极具理论研究意义的 分子。
分子。 分子结构如图所示,已知断裂1molN-N吸收167kJ能量,断裂1molN≡N吸收942kJ能量。下列说法正确的是
分子结构如图所示,已知断裂1molN-N吸收167kJ能量,断裂1molN≡N吸收942kJ能量。下列说法正确的是
 分子。
分子。 分子结构如图所示,已知断裂1molN-N吸收167kJ能量,断裂1molN≡N吸收942kJ能量。下列说法正确的是
分子结构如图所示,已知断裂1molN-N吸收167kJ能量,断裂1molN≡N吸收942kJ能量。下列说法正确的是
A. 比 比 更稳定 更稳定 | B.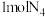 转化为 转化为 ,吸收882kJ能量 ,吸收882kJ能量 |
C. 中N原子未满足最外层 中N原子未满足最外层 结构 结构 | D. 与 与 中均含有非极性共价键 中均含有非极性共价键 |
您最近一年使用:0次
2024-04-05更新
|
262次组卷
|
2卷引用:山东省济宁市育才中学2023-2024学年高一下学期4月月考化学试题