1 . 下列反应属于吸热反应的是
| A.金属钠与水反应 | B.化石燃料的燃烧 |
| C.氢氧化钡晶体与氯化铵晶体混合 | D.氢氧化钠与盐酸反应 |
您最近一年使用:0次
解题方法
2 . 认真归纳常见的吸热反应和放热反应并回答,下列变化属于吸热反应的是
①加热KClO3和MnO2的混合物制取O2 ②蜡烛的燃烧 ③碳和二氧化碳在高温下反应 ④将氢氧化钡晶体和氯化铵晶体的混合物放入水中 ⑤将碳酸钠晶体和硝酸铵晶体混合均匀放在日光下暴晒 ⑥将黏土、石子、水混合均匀 ⑦将生石灰倒入海水中 ⑧煅烧石灰石。
①加热KClO3和MnO2的混合物制取O2 ②蜡烛的燃烧 ③碳和二氧化碳在高温下反应 ④将氢氧化钡晶体和氯化铵晶体的混合物放入水中 ⑤将碳酸钠晶体和硝酸铵晶体混合均匀放在日光下暴晒 ⑥将黏土、石子、水混合均匀 ⑦将生石灰倒入海水中 ⑧煅烧石灰石。
| A.①③④⑤⑧ | B.③④⑤⑥⑧ | C.②④⑤⑥⑦ | D.①②④⑤⑧ |
您最近一年使用:0次
3 . (1)下列反应中,属于放热反应的是_____________ ,属于吸热反应的是___________ .
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是__________ ,负极的电极反应式是_________ .
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25g,铜表面析出了氢气________ L(标准状况),导线中通过______ mol电子.
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为___________ 热反应,该反应过程可以看成________________ .
中和反应都是___________ 热反应,其实质是___________ (用化学语言填空)
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25g,铜表面析出了氢气
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为
中和反应都是
您最近一年使用:0次
名校
4 . 下列说法不正确的是
| A.天津港爆炸案中对剧毒的氰化钠(NaCN) 喷洒双氧水消毒,是利用了双氧水的氧化性 |
| B.碳酸钙分解、氢氧化钡晶体和氯化铵固体反应、高温下铝与氧化铁反应都是吸热反应 |
| C.刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 |
| D.石油原油的脱水,有色玻璃、纳米材料、塑料、橡胶及合成纤维等制造过程都会用到胶体 |
您最近一年使用:0次
2016-12-09更新
|
241次组卷
|
4卷引用:2016届浙江省温州市高三上学期第一次适应性测试理综化学试卷
2013·江苏·二模
名校
5 . 下列说法不正确的是

A.水解反应NH4++H2O NH3·H2O+H+达到平衡后,升高温度平衡正向移动 NH3·H2O+H+达到平衡后,升高温度平衡正向移动 |
| B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C.明矾水解生成Al(OH)3胶体,可用作净水剂 |
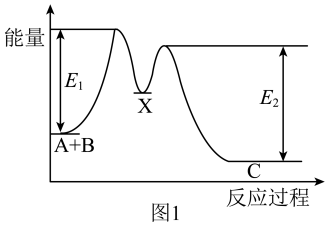
D.如图1所示的反应过程中A+B→X的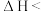 0,X→C的 0,X→C的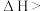 0 0 |
您最近一年使用:0次
2016-12-09更新
|
68次组卷
|
3卷引用:2013届江苏省苏北三市高三第二次调研测试化学试卷
名校
6 . 通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是
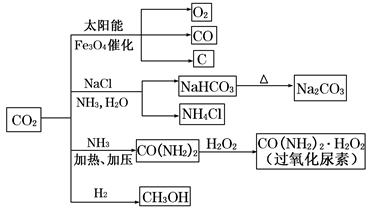

| A.CO2经催化分解为C、CO、O2的反应为放热反应 |
| B.除去Na2CO3固体中少量NaHCO3可用热分解的方法 |
| C.过氧化尿素和SO2都能使品红溶液褪色,其原理相同 |
| D.由CO2和H2合成甲醇,原子利用率达100% |
您最近一年使用:0次
2016-12-09更新
|
740次组卷
|
4卷引用:2016届内蒙古巴彦淖尔市第一中学高三上期中考试理化学试卷
2016届内蒙古巴彦淖尔市第一中学高三上期中考试理化学试卷山西省运城市河津市河津中学2019届高三上学期9月月考化学试题湘赣皖十五校(长郡中学、南昌二中等)2020届高三下学期第一次联考模拟化学试题(已下线)第11讲 碳、硅及无机非金属材料(精讲)-2022年一轮复习讲练测
7 . 下列说法正确的是
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s) △H2 = +226.2kJ•mol-1 ②
可得反应C(s) + CO2(g) =" 2CO(g)" 的△H = +172.5kJ•mol-1
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s) △H2 = +226.2kJ•mol-1 ②
可得反应C(s) + CO2(g) =" 2CO(g)" 的△H = +172.5kJ•mol-1
| A.若2H2(g)+O2(g) = 2H2O(g) ΔH ="-483.6" kJ·mol-1,则H2燃烧热为241.8 kJ·mol-1 |
| B.在稀溶液中:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol,若将含0.6 mol H2SO4的稀硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
| C.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| D.由BaSO4(s) + 4C(s) =" 4CO(g)" + BaS(s) △H1 = +571.2kJ•mol-1 ① |
您最近一年使用:0次
名校
解题方法
8 . 下列依据热化学方程式得出的结论正确的是
| A.已知C(石墨, s)=C(金刚石, s)ΔH>0,则金刚石比石墨稳定 |
| B.2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ/mol,则氢气的燃烧热为241.8kJ•mol-1 |
C.500℃、30MPa下,N2(g)+3H2(g) 2NH3(g)ΔH=-92.4kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ 2NH3(g)ΔH=-92.4kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ |
| D.H2(g)+F2(g)=2HF(g) ΔH = -270kJ•mol-1,则相同条件下,2molHF气体的能量小于1mol氢气和1mol氟气的能量之和 |
您最近一年使用:0次
2016-12-09更新
|
187次组卷
|
4卷引用:2016届山东省枣庄第三中学高三上10月阶段质检化学试卷
2016届山东省枣庄第三中学高三上10月阶段质检化学试卷(已下线)第9单元 化学反应中的能量变化(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷新疆吾尔自治区石河子第二中学2020-2021学年高二上学期第一次月考化学试题甘肃省武威第一中学2020-2021学年高二上学期期中考试化学试题
9 . 下列说法正确的是
| A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s)的ΔH<0 |
| B.常温下,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 |
| C.常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
| D.等体积、等物质的量浓度的NH3·H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3·H2O的电离程度小于NH4+的水解程度 |
您最近一年使用:0次
2016-12-09更新
|
210次组卷
|
3卷引用:2015届江苏省南京市、盐城市高三第二次模拟考试化学试卷
10 . 二氧化碳的过度排放会引发气候问题,而进行有效利用则会造福人类,如以CO2和NH3为原料合成尿素。经研究发现该反应过程为:
①CO2(g)+2NH3(g) NH2COONH4(s) △H1
NH2COONH4(s) △H1
②NH2COONH4(s) CO(NH2)2(s)+H2O(g) △H2>0
CO(NH2)2(s)+H2O(g) △H2>0
请回答下列问题:
(1)研究反应①的平衡常数(K)与温度(T)的关系,如图1所示,则△H1____ 0。(选填“>”、“<”或“=”)。

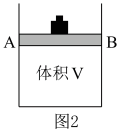
(2)有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图2所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO2(g)+2NH3(g) CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
测定不同条件、不同时间段内的CO2的转化率,得到如下数据:
①T1℃下,l0min内NH3的平均反应速率为__________ 。
②根据上表数据,请比较T1_________ T2(选填“>”、“<”或“=”);T2℃下,第30min时,a1=________ ,该温度下的化学平衡常数为_________ 。
③T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通入3molCO2,此时v(正)_____ v(逆)(选填“>”、“<”或“=”),判断的理由是______ 。
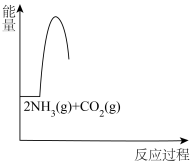
(3)请在下图中补画出合成氨总反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物〔CO(NH2)2(s)+H2O(g)〕。
CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物〔CO(NH2)2(s)+H2O(g)〕。
_____
①CO2(g)+2NH3(g)
 NH2COONH4(s) △H1
NH2COONH4(s) △H1②NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) △H2>0
CO(NH2)2(s)+H2O(g) △H2>0请回答下列问题:
(1)研究反应①的平衡常数(K)与温度(T)的关系,如图1所示,则△H1

(2)有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图2所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO2(g)+2NH3(g)
 CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
测定不同条件、不同时间段内的CO2的转化率,得到如下数据:
| CO2的转化率T(℃) | 10min | 20min | 30min | 40min |
| T1 | 30% | 65% | 75% | 75% |
| T2 | 45% | 50% | a1 | a2 |
②根据上表数据,请比较T1
③T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通入3molCO2,此时v(正)
(3)请在下图中补画出合成氨总反应2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物〔CO(NH2)2(s)+H2O(g)〕。
CO(NH2)2(s)+H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物〔CO(NH2)2(s)+H2O(g)〕。
您最近一年使用:0次



