2023·上海·模拟预测
1 . 为探究 与一元酸HA(
与一元酸HA( mol·L
mol·L )的化学反应热效应,进行了如下四组实验。已知
)的化学反应热效应,进行了如下四组实验。已知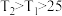 ℃。
℃。
下列说法错误的是
 与一元酸HA(
与一元酸HA( mol·L
mol·L )的化学反应热效应,进行了如下四组实验。已知
)的化学反应热效应,进行了如下四组实验。已知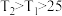 ℃。
℃。| 实验序号 | 试剂I | 试剂Ⅱ | 反应前温度 | 反应后温度 |
| ① | 40 mL  | 2.12 g  | 25℃ |  |
| ② | 20 mL HCl+20 mL  | 2.12 g  | 25℃ |  |
| ③ | 20 mL  +20 mL +20 mL  | 2.12 g  | 25℃ |  |
| ④ | 20 mL HCl | 2.12 g  与20 mL 与20 mL  形成的溶液 形成的溶液 | 25℃ |  |
A. 溶于水放热 溶于水放热 | B. 与HCl反应放热 与HCl反应放热 |
C.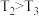 | D.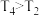 |
您最近一年使用:0次
2 . 下列说法中正确的是
| A.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定 |
| B.化学反应过程所吸收或放出的热量与参加反应的物质的物质的量成正比 |
| C.1molH2燃烧生成水时放出的热量是H2的燃烧热 |
D.已知:500℃、30MPa下,N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ 2NH3(g) △H=-92.4kJ•mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ |
您最近一年使用:0次
3 . CH4超干重整CO2的催化转化如图1所示,相关反应的能量变化如图2所示:
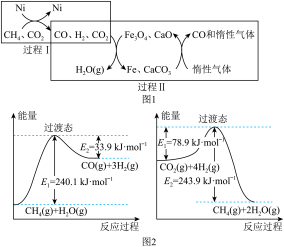
| A.过程I的热化学方程式为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4kJ•mol-1 |
| B.过程II实现了含碳物质与含氢物质的分离 |
| C.过程II中Fe3O4、CaO为中间产物 |
| D.CH4超干重整CO2的总反应为:CH4+3CO2=4CO+2H2O |
您最近一年使用:0次
名校
4 . 回答下列问题:
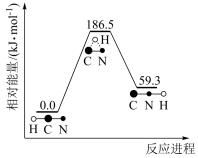
(1)理论研究表明,在101kPa和298K下,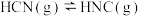 异构化反应过程的能量变化如图所示。下列说法不正确的是 。
异构化反应过程的能量变化如图所示。下列说法不正确的是 。
(2)已知共价键的健能与热化学方程式信息如下表:
则 的
的 为
为
(1)理论研究表明,在101kPa和298K下,
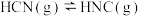 异构化反应过程的能量变化如图所示。下列说法不正确的是 。
异构化反应过程的能量变化如图所示。下列说法不正确的是 。
| A.HCN比HNC稳定 | B.该异构化反应的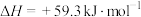 |
| C.正反应与逆反应的活化能相等 | D.使用催化剂,可以改变反应的反应热 |
(2)已知共价键的健能与热化学方程式信息如下表:
| 共价键 | H-H | H-O |
键能/( ) ) | 436 | 463 |
| 热化学方程式 |   | |
 的
的 为
为 A.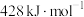 | B.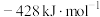 | C.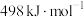 | D.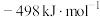 |
您最近一年使用:0次
名校
解题方法
5 . 化学研究所报道了化合物1催化 氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
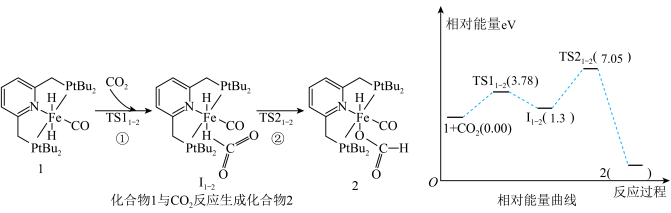
 氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
氢化机理。由单个化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如图(假设1eV=QkJ)。说法正确的是
A.化合物 是该过程的催化剂 是该过程的催化剂 |
B.图中化合物1和 的总能量小于化合物2的总能量 的总能量小于化合物2的总能量 |
| C.化合物2中,CO作为配体,由C原子提供孤电子对 |
D.过程①的热化学方程式为: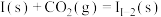  |
您最近一年使用:0次
6 . 制备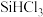 的方程式为
的方程式为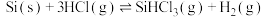 ,同时还有其他副反应发生。当反应体系的压强为
,同时还有其他副反应发生。当反应体系的压强为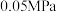 时,分别改变进料比
时,分别改变进料比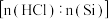 和反应温度,二者对
和反应温度,二者对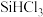 产率影响如图所示。下列说法不正确的是
产率影响如图所示。下列说法不正确的是
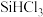 的方程式为
的方程式为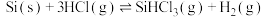 ,同时还有其他副反应发生。当反应体系的压强为
,同时还有其他副反应发生。当反应体系的压强为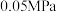 时,分别改变进料比
时,分别改变进料比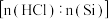 和反应温度,二者对
和反应温度,二者对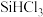 产率影响如图所示。下列说法不正确的是
产率影响如图所示。下列说法不正确的是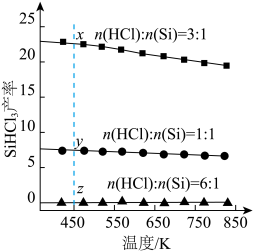
A.增加压强有利于提高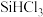 的产率 的产率 |
B.制备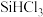 的反应为放热反应 的反应为放热反应 |
C.增加 的用量, 的用量,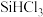 的产率一定会增加 的产率一定会增加 |
D.温度为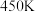 ,平衡常数: ,平衡常数: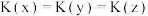 |
您最近一年使用:0次
名校
解题方法
7 . N2O是《联合国气候变化框架公约》所列六种温室气体之一。CO和N2O在Fe+作用下转化为N2和CO2,反应的能量变化及反应历程如图所示,两步基元反应为:① N2O+Fe +=N2+FeO+ K1,②CO+FeO+=CO2+Fe+ K2。下列说法不正确的是
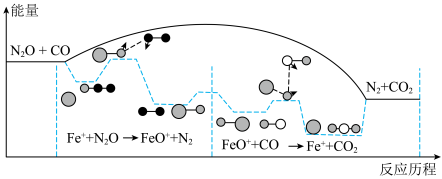

| A.该反应ΔH<0 |
| B.两步反应中,决定总反应速率的是反应① |
| C.升高温度,可提高 N2O 的平衡转化率 |
| D.Fe+增大了活化分子百分数,加快了化学反应速率,但不改变反应的ΔH |
您最近一年使用:0次
2023-07-24更新
|
853次组卷
|
5卷引用:浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题
浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题11-14河南省宜阳县第一高级中学2023-2024学年高二上学期9月开学考试化学试题
8 . 无催化剂作用下,以乙二醛和 为原料制取乙醛酸、甲酸、乙二酸的可能反应历程如图所示,其中
为原料制取乙醛酸、甲酸、乙二酸的可能反应历程如图所示,其中 表示过渡态,
表示过渡态, 表示中间体,下列说法错误的是
表示中间体,下列说法错误的是
 为原料制取乙醛酸、甲酸、乙二酸的可能反应历程如图所示,其中
为原料制取乙醛酸、甲酸、乙二酸的可能反应历程如图所示,其中 表示过渡态,
表示过渡态, 表示中间体,下列说法错误的是
表示中间体,下列说法错误的是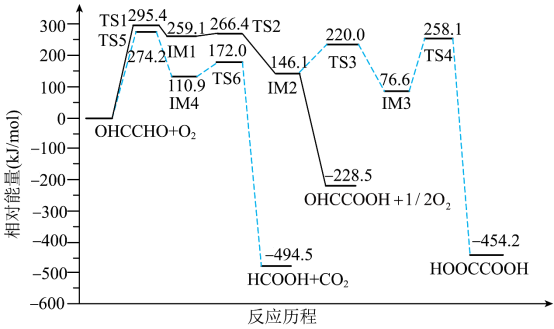
A.反应很短一段时间内, 多于 多于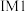 |
B.乙二醛制乙醛酸的最大能垒为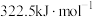 |
| C.选择合适的催化剂可提高乙二酸的选择性 |
| D.乙二醛氧化生成甲酸、乙醛酸或乙二酸均为放热反应 |
您最近一年使用:0次
2024-06-03更新
|
44次组卷
|
2卷引用:黑龙江省部分学校2024届高三下学期第三次模拟化学试题
9 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a) CH4(g)+CO2(g) ⇌ 2CO(g)+2H2(g) ∆H1
b) CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ∆H2
c) CH4(g) ⇌ C(s)+2H2(g) ∆H3
d) 2CO(g) ⇌ CO2(g)+C(s) ∆H4
e) CO(g)+H2(g) ⇌ H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=___________ (写出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
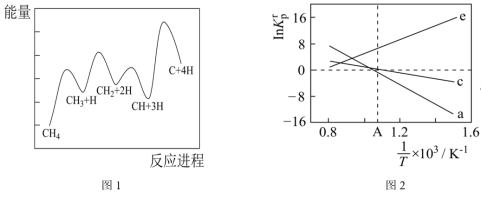
(3)一定条件下,CH4分解形成碳的反应历程如图1所示。该历程分___________ 步进行,其中,第___________ 步的正反应活化能最大。 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。
①反应a、c、e中,属于吸热反应的有___________ (填字母)。
②反应c的相对压力平衡常数表达式为K =
=___________ 。
(5)CO2用途广泛,写出基于其物理性质的一种用途:___________ 。
a) CH4(g)+CO2(g) ⇌ 2CO(g)+2H2(g) ∆H1
b) CO2(g)+H2(g) ⇌ CO(g)+H2O(g) ∆H2
c) CH4(g) ⇌ C(s)+2H2(g) ∆H3
d) 2CO(g) ⇌ CO2(g)+C(s) ∆H4
e) CO(g)+H2(g) ⇌ H2O(g)+C(s) ∆H5
(1)根据盖斯定律,反应a的∆H1=
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________。
| A.增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加 |
| B.移去部分C(s),反应c、d、e的平衡均向右移动 |
| C.加入反应a的催化剂,可提高CH4的平衡转化率 |
| D.降低反应温度,反应a~e的正、逆反应速率都减小 |
(3)一定条件下,CH4分解形成碳的反应历程如图1所示。该历程分
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100kPa)。反应a、c、e的ln K 随
随 (温度的倒数)的变化如图2所示。
(温度的倒数)的变化如图2所示。①反应a、c、e中,属于吸热反应的有
②反应c的相对压力平衡常数表达式为K
 =
=(5)CO2用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
10 . 反应 过程中的能量变化如图所示,下列有关说法正确的是
过程中的能量变化如图所示,下列有关说法正确的是
 过程中的能量变化如图所示,下列有关说法正确的是
过程中的能量变化如图所示,下列有关说法正确的是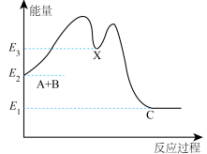
| A.A、B的能量一定高于C的能量 |
| B.该反应分为两个阶段,第一个阶段吸热,第二个阶段放热 |
| C.物质X可能是该反应的催化剂 |
D.该反应放出的能量数值为 |
您最近一年使用:0次
2024-05-29更新
|
242次组卷
|
2卷引用:2024届浙江省舟山中学高三下学期模拟预测化学试题



