真题
解题方法
1 . 磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与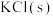 反应制备
反应制备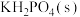 ,反应方程式为
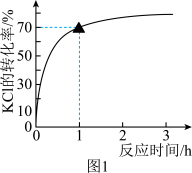
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为_______ 。
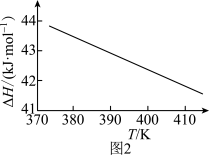
(2)该制备反应的 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为_______ 反应(填“吸热”或“放热”),且反应热随温度升高而_______ 。
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸_______ ;通入水蒸气_______ 。
(4)298K时,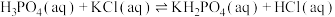 的平衡常数
的平衡常数
_______ 。(已知 的
的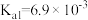 )
)
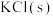 反应制备
反应制备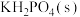 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为
(2)该制备反应的
 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸
(4)298K时,
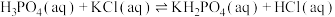 的平衡常数
的平衡常数
 的
的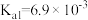 )
)
您最近一年使用:0次
名校
解题方法
2 . 2-丁烯有顺、反两种异构体, ,异构体转化的能量关系如图所示:
,异构体转化的能量关系如图所示:
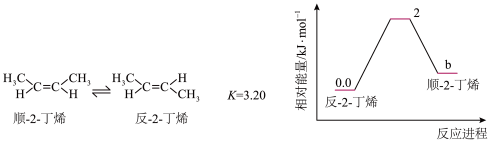
下列说法正确的是
 ,异构体转化的能量关系如图所示:
,异构体转化的能量关系如图所示:
下列说法正确的是
| A.稳定性:顺-2-丁烯>反-2-丁烯 |
B.与 氢气完全加成,所放出的热量顺-2-丁烯比反-2-丁烯多 氢气完全加成,所放出的热量顺-2-丁烯比反-2-丁烯多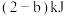 |
C. ,平衡体系中反-2-丁烯的质量分数为76.2% ,平衡体系中反-2-丁烯的质量分数为76.2% |
| D.升高温度,平衡体系中反-2-丁烯的物质的量分数增大 |
您最近一年使用:0次
名校
解题方法
3 . 一定温度下,某刚性密闭容器中按照体积比 充入X和Y两种气体,发生反应
充入X和Y两种气体,发生反应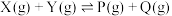 ,该反应的历程如图所示,M和N是中间产物,下列说法正确的是
,该反应的历程如图所示,M和N是中间产物,下列说法正确的是
 充入X和Y两种气体,发生反应
充入X和Y两种气体,发生反应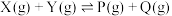 ,该反应的历程如图所示,M和N是中间产物,下列说法正确的是
,该反应的历程如图所示,M和N是中间产物,下列说法正确的是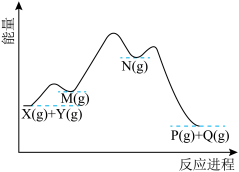
A.该反应的反应热 |
| B.该反应的历程分2步进行 |
| C.反应过程中,N比M达到的最高浓度大 |
D.若初始按照体积比 充入 充入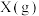 和 和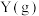 ,其他条件不变,平衡时 ,其他条件不变,平衡时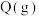 的百分含量不变 的百分含量不变 |
您最近一年使用:0次
4 . 自由基是化学键断裂时产生的含未成对电子的中间体,HNO自由基与 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是
 反应过程的能量变化如图所示,下列说法正确的是
反应过程的能量变化如图所示,下列说法正确的是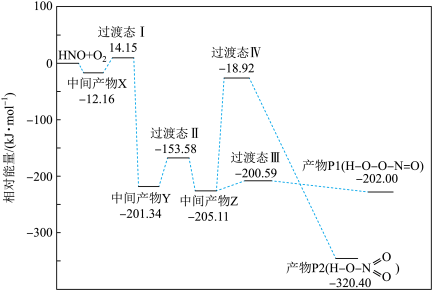
A.反应过程中,产物 的浓度先增大,后减小 的浓度先增大,后减小 |
B.过渡态能量越高,反应的活化能越高,反应的 越小 越小 |
C.其它条件相同,升高温度,达到平衡时,生成的产物中 的百分含量增大 的百分含量增大 |
D.反应过程中,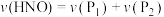 |
您最近一年使用:0次
解题方法
5 . 含氯消毒剂和过氧化物消毒剂均可有效灭杀新冠病毒。
Ⅰ.过碳酸钠(2Na2CO3·3H2O2)俗称固态双氧水,具有去污、杀菌等功效。其制备原理为:2Na2CO3(aq)+3H2O2(aq)=2Na2CO3·3H2O2(aq) △H<0。
(1)结合过氧化氢和碳酸钠的性质,推测制备过碳酸钠的过程中,碳酸钠与过氧化氢的物质的量之比应小于2:3,且加入Na2CO3溶液速率不能过快的原因是_______ 。
(2)过碳酸钠的储存稳定性是重要的品质指标。以不同种类的稳定剂制备的过碳酸钠产品,测得其活性氧的质量分数随时间变化如图所示。由图可知,制备过碳酸钠时应选择的稳定剂是_______ 。(填图中字母)
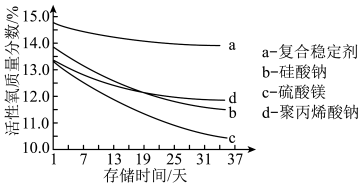
Ⅱ.NaClO2是一种更为安全有效的清洗﹑杀菌剂,特别是在NaClO使用受限制的场合,NaClO3是NaClO的安全代用品。
(3)工业上用石墨电极电解ClO2、NaCl溶液制备NaClO3。写出该反应的离子方程式:_______ 。
Ⅰ.过碳酸钠(2Na2CO3·3H2O2)俗称固态双氧水,具有去污、杀菌等功效。其制备原理为:2Na2CO3(aq)+3H2O2(aq)=2Na2CO3·3H2O2(aq) △H<0。
(1)结合过氧化氢和碳酸钠的性质,推测制备过碳酸钠的过程中,碳酸钠与过氧化氢的物质的量之比应小于2:3,且加入Na2CO3溶液速率不能过快的原因是
(2)过碳酸钠的储存稳定性是重要的品质指标。以不同种类的稳定剂制备的过碳酸钠产品,测得其活性氧的质量分数随时间变化如图所示。由图可知,制备过碳酸钠时应选择的稳定剂是

Ⅱ.NaClO2是一种更为安全有效的清洗﹑杀菌剂,特别是在NaClO使用受限制的场合,NaClO3是NaClO的安全代用品。
(3)工业上用石墨电极电解ClO2、NaCl溶液制备NaClO3。写出该反应的离子方程式:
您最近一年使用:0次
6 . 下列说法中正确的是
| A.吸热反应一定需要加热才能反应,而放热反应在常温下一定能进行 |
| B.水银和生铁都属于纯金属 |
C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有 |
| D.某硫酸铵肥料中只含一种杂质,氮元素的质量分数为20%,可能混有硝酸铵 |
您最近一年使用:0次
7 . 溴分子易极化,使分子内溴原子分别带部分正电荷和部分负电荷。在一定条件下 与
与 发生加成反应会得到两种产物,且两种产物可通过
发生加成反应会得到两种产物,且两种产物可通过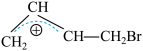 互相转化,反应历程如下:
互相转化,反应历程如下:
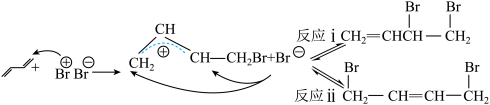
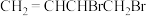 与
与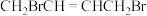 相互转化的能量变化如图所示。下列叙述错误的是
相互转化的能量变化如图所示。下列叙述错误的是
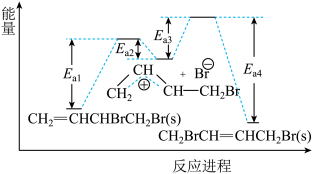
 与
与 发生加成反应会得到两种产物,且两种产物可通过
发生加成反应会得到两种产物,且两种产物可通过 互相转化,反应历程如下:
互相转化,反应历程如下:
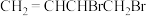 与
与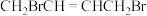 相互转化的能量变化如图所示。下列叙述错误的是
相互转化的能量变化如图所示。下列叙述错误的是
| A.相同条件下,反应i的速率比反应ii的快 |
B.升高温度,有利于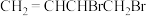 的生成 的生成 |
C.反应 的 的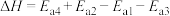 |
D.相同条件下,反应达平衡后产物中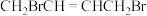 的含量更高 的含量更高 |
您最近一年使用:0次
8 .  是一种强氧化剂,能分解成
是一种强氧化剂,能分解成 和
和 。图1表示
。图1表示 分解时能量与反应进程的关系,图2表示
分解时能量与反应进程的关系,图2表示 酶的相对活性与温度、时间的关系,图3表示相同浓度的
酶的相对活性与温度、时间的关系,图3表示相同浓度的 在
在
 时分解过程中
时分解过程中 的质量分数与时间及
的质量分数与时间及 的关系。
的关系。
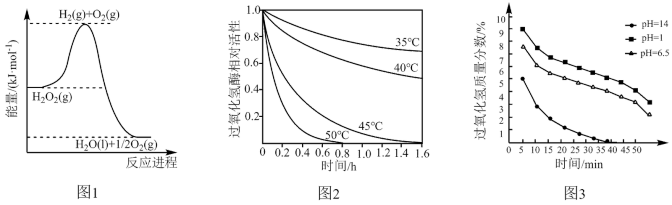
下列相关说法正确的是
 是一种强氧化剂,能分解成
是一种强氧化剂,能分解成 和
和 。图1表示
。图1表示 分解时能量与反应进程的关系,图2表示
分解时能量与反应进程的关系,图2表示 酶的相对活性与温度、时间的关系,图3表示相同浓度的
酶的相对活性与温度、时间的关系,图3表示相同浓度的 在
在
 时分解过程中
时分解过程中 的质量分数与时间及
的质量分数与时间及 的关系。
的关系。
下列相关说法正确的是
A.反应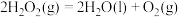 为吸热反应 为吸热反应 |
B.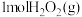 转化为 转化为 和 和 需吸收 需吸收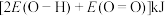 能量 能量 |
C.相同浓度的 用过氧化氢酶催化时,温度越高分解速率一定越快 用过氧化氢酶催化时,温度越高分解速率一定越快 |
D.其他条件一定时,强碱性条件有利于 的分解 的分解 |
您最近一年使用:0次
名校
9 . 乙苯与氯气在光照条件下反应生成两种一氯取代物,反应过程中的能量变化如图所示。下列说法错误的是
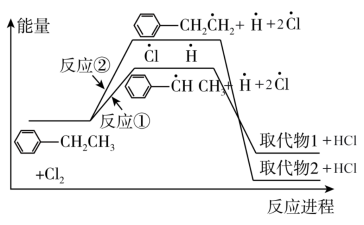

A.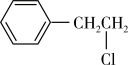 比 比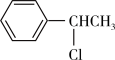 稳定 稳定 |
| B.反应①比反应②的速率快 |
| C.若升温时取代产物2的含量提高,则原因是反应②平衡正向移动 |
| D.选择合适催化剂可提高单位时间内取代产物2的含量 |
您最近一年使用:0次
解题方法
10 . CO常用于工业冶炼金属,下图所示是在不同温度下CO还原四种金属氧化物达平衡后气体中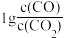 与温度(t)的关系曲线图。下列说法正确的是
与温度(t)的关系曲线图。下列说法正确的是
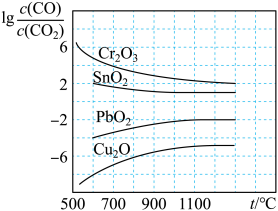
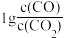 与温度(t)的关系曲线图。下列说法正确的是
与温度(t)的关系曲线图。下列说法正确的是
| A.CO还原PbO2的反应ΔH>0 |
| B.工业冶炼金属铜(Cu)时较高的温度有利于提高CO的利用率 |
| C.CO不适宜用于工业冶炼金属铬(Cr) |
| D.工业上可以通过增高反应装置来减少尾气中CO的含量 |
您最近一年使用:0次



