名校
解题方法
1 . 我国科学家研究化合物M(s)催化CO2氢化机理。由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如图所示(已知1eV=1.6×10−19J)。TS1、TS2均为过渡态。下列说法错误的是
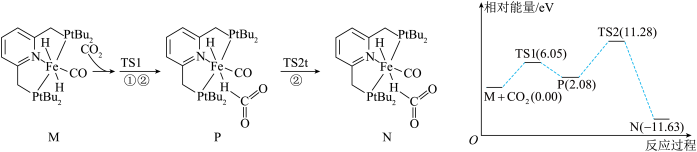

| A.过渡态TS1比TS2更稳定 |
| B.过程P→TS2为化合物M生成化合物N的决速步骤 |
| C.化合物M催化CO2氢化反应过程中一定有Fe−O键的断裂 |
| D.该过程的热化学方程式为:M(s)+CO2(g)=N(s) ΔH=−11.63 kJ·mol −1 |
您最近一年使用:0次
2022-12-21更新
|
359次组卷
|
5卷引用:湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题
解题方法
2 . 反应C(石墨) → C(金刚石)是吸热反应,由此可知
| A.石墨比金刚石更稳定 | B.金刚石和石墨可以相互转化 |
| C.金刚石比石墨稳定 | D.金刚石和石墨不能相互转化 |
您最近一年使用:0次
解题方法
3 . 一定温度下 与
与 反应生成
反应生成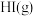 ,反应的能量变化如图所示。以下对该反应体系的描述中,正确的是
,反应的能量变化如图所示。以下对该反应体系的描述中,正确的是
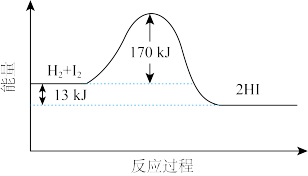
 与
与 反应生成
反应生成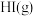 ,反应的能量变化如图所示。以下对该反应体系的描述中,正确的是
,反应的能量变化如图所示。以下对该反应体系的描述中,正确的是
| A.反应物的总能量比生成物的总能量高13kJ |
| B.反应物的总能量比生成物的总能量低13kJ |
| C.反应物化学键中储存的总能量比生成物化学键中储存的总能量低 |
| D.反应物化学键中储存的总能量比生成物化学键中储存的总能量高 |
您最近一年使用:0次
解题方法
4 . 如图是C和H2O(g)反应的能量变化图示,下列说法正确的是
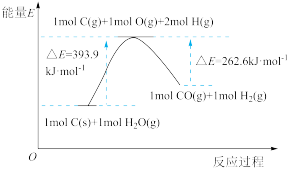

| A.该反应为吸热反应 |
| B.1 mol C(g)和1 mol H2O(g)具有的总能量低于1 mol C(s)和1 mol H2O(g)具有的总能量 |
| C.1 mol C(s)和1 mol H2O(g)反应生成1 mol CO(g)和1 mol H2(g),吸收131.3 kJ热量 |
| D.1 mol H2O(g)中O-H键断裂需要吸收393.9 kJ热量 |
您最近一年使用:0次
5 . 下列图象分别表示有关反应的反应过程与能量变化的关系。
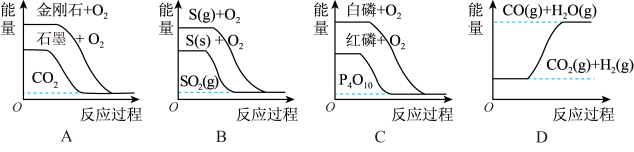
| A.石墨转变为金刚石是放热反应 |
B.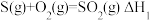 , ,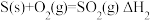 ,则 ,则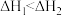 |
| C.白磷比红磷稳定 |
D. |
您最近一年使用:0次
2022-09-13更新
|
454次组卷
|
8卷引用:青海省西宁市海湖中学2021-2022学年高二上学期开学考试化学试题
解题方法
6 . 国家战略“碳达峰、碳中和”, 与
与 可合成甲醇:
可合成甲醇: ,同时会生成副产物
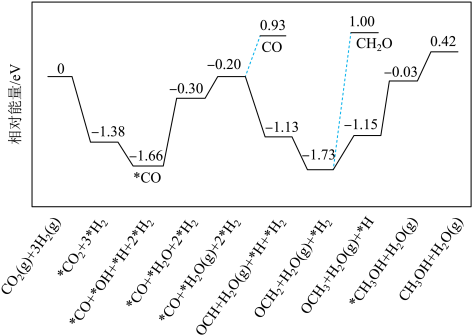
,同时会生成副产物 与甲醛,反应过程中的能量变化如图所示,吸附在催化剂表面上的物质用*标注。下列说法错误的是
与甲醛,反应过程中的能量变化如图所示,吸附在催化剂表面上的物质用*标注。下列说法错误的是
 与
与 可合成甲醇:
可合成甲醇: ,同时会生成副产物
,同时会生成副产物 与甲醛,反应过程中的能量变化如图所示,吸附在催化剂表面上的物质用*标注。下列说法错误的是
与甲醛,反应过程中的能量变化如图所示,吸附在催化剂表面上的物质用*标注。下列说法错误的是
A. |
B.主反应过程中的最大能垒(活化能)为 |
C.反应过程中生成副产物甲醛的速率大于生成 的速率 的速率 |
D.若更换催化剂种类,反应历程发生变化,但 不变 不变 |
您最近一年使用:0次
解题方法
7 . 铝热剂的主要成分为铝及氧化铁,先以火焰枪或镁带加热引发后,二者进行反应,产生熔融态的铁,可供焊接之用。下列相关化学反应的叙述,哪些正确?
| A.反应为放热反应 |
| B.反应有氧气参与 |
| C.反应属于氧化还原反应 |
| D.此反应中,铝比铁较易失去电子 |
| E.在反应中铝为氧化剂,氧化铁为还原剂 |
您最近一年使用:0次
名校
解题方法
8 . 根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mL0.1mol·L−1的FeCl3溶液中加入4mL0.1mol·L−1的KI溶液,充分反应后,分别取少量溶液于两支试管中,向其中一支试管中滴加几滴淀粉溶液,溶液变蓝,另一支试管中滴加几滴KSCN溶液,溶液变红 | KI与FeCl3的反应是可逆反应 |
| B | 室温下,向0.1mol·L−1HCl溶液中加入少量镁粉,产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| C | 向盛有2mL0.1mol·L-1的硝酸银溶液的试管中滴加2滴0.1mol·L-1的氯化钠溶液,生成白色沉淀,再滴加2滴 0.1mol·L-1的碘化钾溶液,有黄色沉淀生成 | Ksp(AgI)<Ksp(AgCl) |
| D | 用pH试纸测得:CH3COONa溶液的pH约为9,NaHCO3溶液的pH约为10 | CH3COOH电离出H+的能力比H2CO3强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
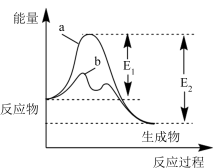
9 . 2SO2(g)+O2(g)  2SO3(g) ΔH=-2a kJ·mol-l反应过程中的能量变化如图所示。下列有关叙述
2SO3(g) ΔH=-2a kJ·mol-l反应过程中的能量变化如图所示。下列有关叙述不正确 的是
 2SO3(g) ΔH=-2a kJ·mol-l反应过程中的能量变化如图所示。下列有关叙述
2SO3(g) ΔH=-2a kJ·mol-l反应过程中的能量变化如图所示。下列有关叙述
| A.该反应的正反应为吸热反应,升高温度可使平衡常数K增大 |
| B.降低温度、增大O2浓度均有利于提高SO2转化率 |
| C.过程a与过程b对比,b使用了催化剂,反应物转化率不变,ΔH也不变 |
| D.常温常压下,加入1 mol SO2(g)和0.5 mol O2(g)于密闭容器中充分反应,放热a kJ |
您最近一年使用:0次
解题方法
10 . 下列有关实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 相同温度下,将两片质量和表面积相同的未经打磨的铝片分别投入足量等浓度的CuSO4溶液和CuCl2溶液中 | CuSO4溶液中无明显现象;CuCl2溶液中反应剧烈,铝片表面有红色物质生成 | Cl-能加速破坏铝片表面的氧化膜 |
| B | 用pH计测定Na2CO3溶液和CH3COONa溶液的pH | Na2CO3溶液的pH大于CH3 COONa | H2CO3酸性弱于CH3COOH |
| C | 分别向等体积的0.01mol L-1和0.1mol L-1和0.1mol L-1的KMnO4溶液中通入足量SO2,记录溶液褪色所需的时间 L-1的KMnO4溶液中通入足量SO2,记录溶液褪色所需的时间 | 0.1 mol L-1KMnO4溶液褪色所需时间更短 L-1KMnO4溶液褪色所需时间更短 | 其他条件相同时,增大反应物浓度,反应速率增大 |
| D | 向烧杯中加入一定量的Ca(OH)2和NH4Cl晶体的混合物,将烧杯放在有水的玻璃片上,用玻璃棒迅速搅拌 | 有刺激性气味气体生成,烧杯底部结冰,与玻璃片冻结在一起 | 吸热反应不一定需要加热才能进行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



