解题方法
1 . 铝热剂的主要成分为铝及氧化铁,先以火焰枪或镁带加热引发后,二者进行反应,产生熔融态的铁,可供焊接之用。下列相关化学反应的叙述,哪些正确?
| A.反应为放热反应 |
| B.反应有氧气参与 |
| C.反应属于氧化还原反应 |
| D.此反应中,铝比铁较易失去电子 |
| E.在反应中铝为氧化剂,氧化铁为还原剂 |
您最近一年使用:0次
2 . 如图是“即热饭盒”的结构示意图,撤去隔板,水与下层物质接触,一段时间后食物就变热了。以下物质中适合作下层物质的是
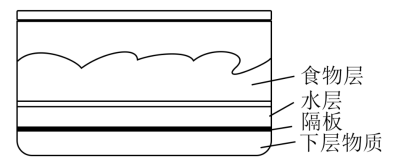

| A.食盐 | B.生石灰 | C.熟石灰 | D.浓硫酸 |
您最近一年使用:0次
2022-07-02更新
|
200次组卷
|
3卷引用:2021年河南省普通高中学生学业水平考试化学试题
3 . 化学反应与能量变化是化学研究的重要问题,根据相关材料分析回答:
(1)已知断开1mol下列物质中的化学键需要吸收的能量如下表:
根据以上数据判断:N2 + O2 = 2NO属于___________ 反应(填“放热”或“吸热”)。
(2)符合某些特征的化学反应理论上都可以设计成原电池。下列化学反应___________ (填字母)不能设计成原电池,原因是___________ 。
A.CH4+2O2=CO2+2H2O
B.Fe+CuSO4=FeSO4+Cu
C.2NaOH + H2SO4 = Na2SO4 + 2H2O
D.Pb+PbO2+2H2SO4=2PbSO4+2H2O
(3)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是___________ ;写出装置乙中正极的电极反应式:___________ 。
(4)锂离子电池已经成为新一代实用的蓄电池,它具有能量密度大、电压高的特性。某锂离子电池放电时电极反应如下:
负极Li-e-= Li+,
正极Li1-xMnO2+xLi++xe-=LiMnO2
该锂离子电池放电时电池的反应方程式为___________ 。
(1)已知断开1mol下列物质中的化学键需要吸收的能量如下表:
| 物质 | N2 | O2 | NO |
| 吸收的能量 | 946kJ | 498 kJ | 632kJ |
根据以上数据判断:N2 + O2 = 2NO属于
(2)符合某些特征的化学反应理论上都可以设计成原电池。下列化学反应
A.CH4+2O2=CO2+2H2O
B.Fe+CuSO4=FeSO4+Cu
C.2NaOH + H2SO4 = Na2SO4 + 2H2O
D.Pb+PbO2+2H2SO4=2PbSO4+2H2O
(3)把A、B、C、D四种金属按表中装置进行实验。
| 装置 | 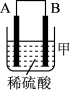 | 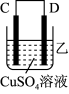 | 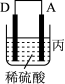 |
| 电子从A到B | C电极的质量增加 | 二价金属D不断溶解 |
根据表中信息判断四种金属活动性由大到小的顺序是
(4)锂离子电池已经成为新一代实用的蓄电池,它具有能量密度大、电压高的特性。某锂离子电池放电时电极反应如下:
负极Li-e-= Li+,
正极Li1-xMnO2+xLi++xe-=LiMnO2
该锂离子电池放电时电池的反应方程式为
您最近一年使用:0次
4 . 医用热敷袋使用时要轻揉,袋内的反应可看作是铁粉、空气和水相互作用,先产生氢氧化亚铁,后转化为氢氧化铁。下列说法错误的是
| A.这一变化过程的总反应可表示为:2Fe+O2+H2O=2Fe(OH)3 |
| B.热敷袋放出的热量是由化学反应产生的 |
| C.热敷袋含铁物质变化过程中,铁元素的化合价呈现了0价、+2价、+3价 |
| D.热敷袋中的铁粉与水在未使用时要分别密封保存 |
您最近一年使用:0次
2022-03-14更新
|
250次组卷
|
2卷引用:陕西省渭南市华州区咸林中学2021-2022学年高一上学期第三阶段质量检测化学试题
名校
解题方法
5 . 在Fe作催化剂的条件下,合成氨反应途径可简单地表示为:①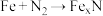
 ;②
;②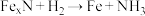
 。已知反应①和②的活化能分别为126
。已知反应①和②的活化能分别为126 和13
和13 ,则合成氨反应的
,则合成氨反应的 在有催化剂(a)和无催化剂(b)时反应过程能量变化图是
在有催化剂(a)和无催化剂(b)时反应过程能量变化图是
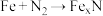
 ;②
;②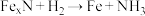
 。已知反应①和②的活化能分别为126
。已知反应①和②的活化能分别为126 和13
和13 ,则合成氨反应的
,则合成氨反应的 在有催化剂(a)和无催化剂(b)时反应过程能量变化图是
在有催化剂(a)和无催化剂(b)时反应过程能量变化图是A.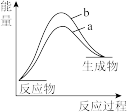 | B.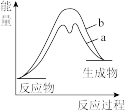 |
C.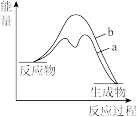 | D.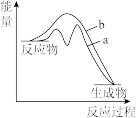 |
您最近一年使用:0次
2022-03-14更新
|
152次组卷
|
3卷引用:四川省内江市第六中学2021-2022学年上学期高二第二次月考化学试题
6 . 下列说法不正确 的是
| A.自嗨锅的发热包主要成分是生石灰,其与水反应放热从而使食材加热 |
| B.抗坏血酸(即维生素C)是水果罐头中常用的抗氧化剂,是因为其具有较强的氧化性 |
| C.在食品包装袋内放入铁系保鲜剂可以防止食品因氧化而变质 |
| D.臭氧是饮用水的理想消毒剂之一,因为它杀菌能力强且不影响水质 |
您最近一年使用:0次
2022-03-09更新
|
206次组卷
|
2卷引用:四川省南充高级中学2021-2022学年高二上学期入学考试化学试题
7 . 下列有关下图所示装置或图象的判断或说法错误的是
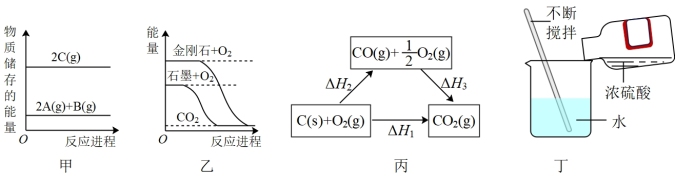

| A.图甲所示反应为2A(g)+B(g)=2C(g) ΔH>0 |
| B.根据图乙可判断:石墨转变为金刚石是吸热反应 |
| C.结合盖斯定律,由图丙可得:ΔH1=ΔH2+ΔH3 |
| D.图丁所示实验发生的为放热反应 |
您最近一年使用:0次
2022-02-20更新
|
532次组卷
|
6卷引用:浙江省吴兴高级中学2021-2022学年高二上学期12月月考化学试题
名校
8 . I.目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应过程中能量的变化。
CH3OH(g)+H2O(g),如图表示该反应过程中能量的变化。
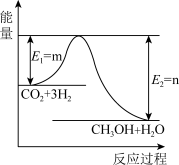
(1)该反应为____ 反应(“吸热”或“放热”)。
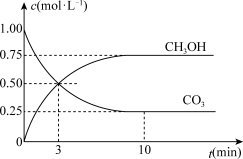
(2)在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)=____ 。反应达到平衡时CO2的转化率为____ 。平衡时CH3OH的体积分数为____ 。
II.在298K时,将0.1molN2O4气体充入1L抽空的密闭容器中,回答下列问题:
(3)当反应达到平衡时,对于反应N2O4(g) 2NO2(g),改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是
2NO2(g),改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是____ (填序号)。
①气体颜色加深②NO2的体积分数增加③单位时间内消耗N2O4和NO2的物质的量之比大于1∶2④恒温恒压充入He
(4)达到平衡后下列条件的改变可使NO2反应速率增大的是____ (填字母序号)。
a.扩大容器的容积 b.再充入一定量的N2O4 c.分离出一定量的NO2
(5)在固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的____ (填“深”或“浅”),其原因是____ 。

 CH3OH(g)+H2O(g),如图表示该反应过程中能量的变化。
CH3OH(g)+H2O(g),如图表示该反应过程中能量的变化。
(1)该反应为
(2)在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v(H2)=

II.在298K时,将0.1molN2O4气体充入1L抽空的密闭容器中,回答下列问题:
(3)当反应达到平衡时,对于反应N2O4(g)
 2NO2(g),改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是
2NO2(g),改变某一条件后,下列说法中,一定能说明化学平衡向正反应方向移动的是①气体颜色加深②NO2的体积分数增加③单位时间内消耗N2O4和NO2的物质的量之比大于1∶2④恒温恒压充入He
(4)达到平衡后下列条件的改变可使NO2反应速率增大的是
a.扩大容器的容积 b.再充入一定量的N2O4 c.分离出一定量的NO2
(5)在固定体积的密闭容器中,发生可逆反应:2NO2(g)
 N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用如图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
您最近一年使用:0次
解题方法
9 . 利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
已知:
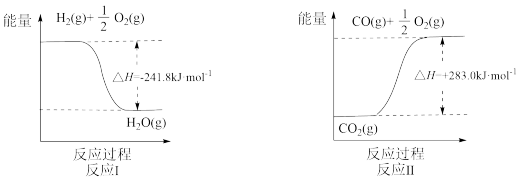
(1)反应Ⅱ是___________ 反应(填“吸热”或“放热”),其原因是___________ 。
(2)反应A的热化学方程式是___________ 。
反应A:

已知:

(1)反应Ⅱ是
(2)反应A的热化学方程式是
您最近一年使用:0次
2022-01-28更新
|
98次组卷
|
2卷引用:山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题
名校
解题方法
10 . 图象可更直观地表现化学变化中的物质变化和能量变化。下列判断错误的是
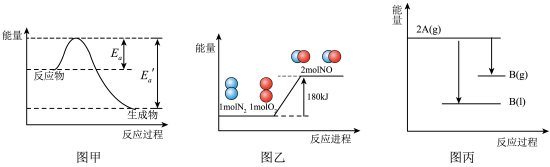
A.图甲所示反应为放热反应,且△H=Ea-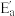 |
B.若已知石墨比金刚石稳定,则C(石墨,s)=C(金刚石,s)  |
C.图乙所示反应的热化学方程式为: 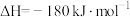 |
D.若  ,则物质能量高低如图丙 ,则物质能量高低如图丙 |
您最近一年使用:0次
2022-01-10更新
|
805次组卷
|
10卷引用:河南省义马市高级中学2021-2022学年高三上学期11月份联考化学试题
河南省义马市高级中学2021-2022学年高三上学期11月份联考化学试题宁夏石嘴山市第三中学2021-2022学年高三上学期第二次月考化学试题内蒙古通辽市开鲁县第一中学2021-2022学年高一下学期期中考试化学试题宁夏石嘴山市第三中学2022-2023学年高三上学期期中考试化学试题湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题湖南省长沙市长郡中学2022--2023学年高二上学期第二次线上月考化学试题(已下线)专题15 反应热计算的几种类型-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)福建省福州第三中学2022-2023学年高一下学期3月月考化学试题宁夏银川市上游学校2023-2024学年高二下学期开学考试化学试卷安徽省安庆市第一中学2023-2024学年高二下学期第一次段考(期中)化学试题



