解题方法
1 . 碳、氮的单质及其化合物在生产和生活中有广泛应用。
(1)已知在298K时,C(石墨)完全燃烧的热化学方程式:C(石墨)+O2(g)=CO2(g) ∆H=-393.5kJ·mol-1。该反应属于___________ (填“放热”或“吸热”)反应。
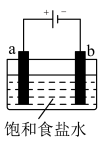
(2)—定条件下,在某密闭容器中进行反应:N2(g)+3H2(g)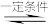 2NH3(g) ∆H<O。
2NH3(g) ∆H<O。
①若N2(g)的起始浓度为1mol-1•L-1,H2(g)的起始浓度为3mol•L-1,反应进行到2min时,测得H2(g)浓度为2mol•L-1,测2min内v(H2)=___________ mol•L-1•min•L-1。
②当反应达到平衡时,若只升高温度,则平衡向___________ (填“正反应”或“逆反应”)方向移动。
③当反应达到平衡时,若只增大压强,则化学平衡常数K___________ (填"增大”“减小”或“不变”)。
(3)常温下,往0.1mol•L-1NH4Cl溶液中滴入紫色石蕊试液后,溶液变红色,则该溶液pH___________ 7(填“〉”或“<”);c( )
)___________ c(Cl-)(填“〉”或“<”)。
(4)如图所示实验,用石墨电极电解饱和食盐水:2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
①a电极是电解池的___________ (填“阳极”或“阴极”)。
②溶液中H+向___________ (填“a”或“b”)电极移动。
③生成Cl2的电极反应式:___________ 。
(1)已知在298K时,C(石墨)完全燃烧的热化学方程式:C(石墨)+O2(g)=CO2(g) ∆H=-393.5kJ·mol-1。该反应属于
(2)—定条件下,在某密闭容器中进行反应:N2(g)+3H2(g)
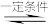 2NH3(g) ∆H<O。
2NH3(g) ∆H<O。①若N2(g)的起始浓度为1mol-1•L-1,H2(g)的起始浓度为3mol•L-1,反应进行到2min时,测得H2(g)浓度为2mol•L-1,测2min内v(H2)=
②当反应达到平衡时,若只升高温度,则平衡向
③当反应达到平衡时,若只增大压强,则化学平衡常数K
(3)常温下,往0.1mol•L-1NH4Cl溶液中滴入紫色石蕊试液后,溶液变红色,则该溶液pH
 )
)(4)如图所示实验,用石墨电极电解饱和食盐水:2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
①a电极是电解池的
②溶液中H+向
③生成Cl2的电极反应式:
您最近一年使用:0次
2 . 回答下列问题
(1)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。
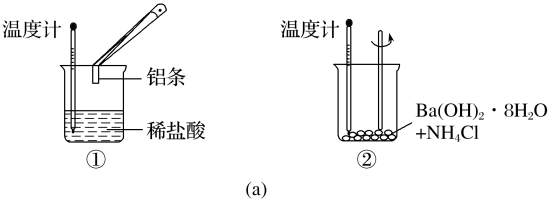
实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是___________ 热反应,Ba(OH)2·8H2O与NH4Cl的反应是___________ 热反应。
(2)我国发射宇宙飞船的 “神舟”系列火箭用偏二甲肼(C2H8N2)作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体,其反应的化学方程式为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O。则该反应是___________ (填“放热”或“吸热”)反应,反应物的总能量___________ (填“大于”、“小于”或“等于”)生成物的总能量,断开化学键吸收的总能量___________ (填“大于”、“小于”或“等于”)形成化学键放出的总能量。
(3)矿物能源是现代人类社会赖以生存的重要物质基础,目前,全球仍主要处于化石能源时期。下列不属于化石能源的是___________。
(4)沼气是有机废弃物(树叶、秸秆、草类及垃圾、粪便等)在隔绝空气的条件下发酵分解而成的气体,主要成分是甲烷。农村沼气池中发酵后的池底剩余物是很好的沤肥。下面有关叙述中,错误的是___________。
(1)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。

实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是
(2)我国发射宇宙飞船的 “神舟”系列火箭用偏二甲肼(C2H8N2)作燃料,液态四氧化二氮作氧化剂,生成氮气和二氧化碳气体,其反应的化学方程式为C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O。则该反应是
(3)矿物能源是现代人类社会赖以生存的重要物质基础,目前,全球仍主要处于化石能源时期。下列不属于化石能源的是___________。
| A.石油 | B.煤 | C.天然气 | D.生物质能 |
| A.沼气是一种清洁的能源 |
| B.使用沼气作能源可以保护森林 |
| C.使用沼气给农民的生活带来了不便 |
| D.使用沼气是对化学能的充分利用 |
您最近一年使用:0次
解题方法
3 . 反应 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。_______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,
_______ ,
_______ (填增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ (填“增大”、“减小”或“不变”)。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
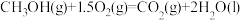
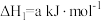
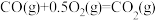
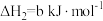
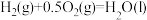
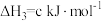
则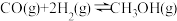

_______  (用a、b、c表示)。
(用a、b、c表示)。
(3)一定压强下,在容积为 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: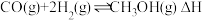 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则
_______  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
 过程中的能量变化如下图所示,回答下列问题。
过程中的能量变化如下图所示,回答下列问题。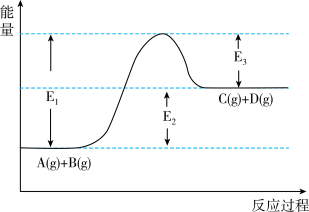
②在反应体系中加入催化剂,反应速率增大,


③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
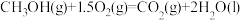
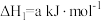
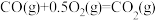
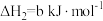
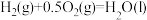
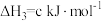
则
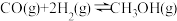

 (用a、b、c表示)。
(用a、b、c表示)。(3)一定压强下,在容积为
 的密闭容器中充入
的密闭容器中充入 与
与 ,在催化剂作用下发生反应:
,在催化剂作用下发生反应: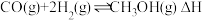 ,平衡转化率与温度、压强的关系如图所示。则
,平衡转化率与温度、压强的关系如图所示。则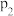
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);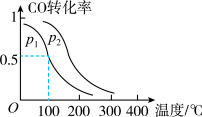
您最近一年使用:0次
名校
解题方法
4 . 以CO和 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。
已知:①
 kJ·mol
kJ·mol
②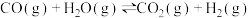
 kJ·mol
kJ·mol
③
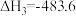 kJ·mol
kJ·mol
下列说法不正确 的是
 为原料合成甲醇是工业上的成熟方法,直接以
为原料合成甲醇是工业上的成熟方法,直接以 为原料生产甲醇是目前的研究热点。我国科学家用
为原料生产甲醇是目前的研究热点。我国科学家用 人工合成淀粉时,第一步就需要将
人工合成淀粉时,第一步就需要将 转化为甲醇。
转化为甲醇。已知:①

 kJ·mol
kJ·mol
②
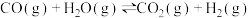
 kJ·mol
kJ·mol
③

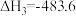 kJ·mol
kJ·mol
下列说法
A.若温度不变,反应①中生成1 mol  时,放出的热量大于90.5 kJ 时,放出的热量大于90.5 kJ |
B. 与 与 合成甲醇的热化学方程式为: 合成甲醇的热化学方程式为:  kJ·mol kJ·mol |
C.通过电解制 和选用高效催化剂,可降低 和选用高效催化剂,可降低 与 与 合成甲醇反应的焓变 合成甲醇反应的焓变 |
D.以 和 和 为原料合成甲醇,同时生成 为原料合成甲醇,同时生成 ,该反应需要吸收能量 ,该反应需要吸收能量 |
您最近一年使用:0次
2022-11-27更新
|
920次组卷
|
7卷引用:北京市海淀区2021-2022学年高三上学期期中考试化学试题
北京市海淀区2021-2022学年高三上学期期中考试化学试题天津市静海区第一中学2021-2022学年高三上学期12月调研考试化学试题北京市第二十二中学2021-2022学年高三上学期12月阶段性测试理科化学试题北京市东城区一六六中学2022-2023学年高三上学期期中考试化学试题(已下线)2023年北京卷高考真题变式题(选择题11-14)(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)化学反应的热效应
5 . 汽车尾气主要含有二氧化碳、一氧化碳、二氧化硫、一氧化氮等物质,是造成城市空气污染的主要因素之一。请回答下列问题。
(1)汽车尾气中的一氧化碳来自_____ ,一氧化氮来自_____ 。汽车尾气对环境的危害主要有_____ (至少填两种)。
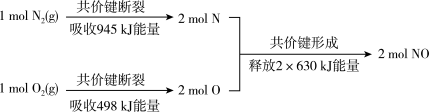
(2)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应_____ (填“释放”或“吸收”)____ kJ能量。
(1)汽车尾气中的一氧化碳来自
(2)氮气和氧气反应生成一氧化氮的能量变化如图所示,则由该反应生成2molNO时,应

您最近一年使用:0次
6 . 举例说明下列各能量形式之间的相互转化。
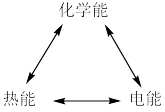
你还能说出其他形式的能量转化吗__________ ?

你还能说出其他形式的能量转化吗
您最近一年使用:0次
7 . 两位同学讨论放热反应和吸热反应。甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们的说法正确吗_______ ?为什么_________ ?
您最近一年使用:0次
8 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS____ 0,该反应自发进行的条件是____ (填“低温”“高温”或“任意温度”)。
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为____ kJ。
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH____ ΔH3(填“>”“<”“=”)。
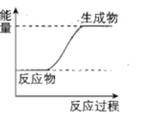
(4)根据盖斯定律计算反应②的ΔH2=____ kJ•mol-1,上述①②③反应中符合如图能量变化的是____ (填序号)。
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH
(4)根据盖斯定律计算反应②的ΔH2=

您最近一年使用:0次
9 . 如图是H2与Cl2发生反应生成HCl的途径和三个状态的能量,有关说法错误的是


| A.步骤2是放热过程 | B.三个状态的能量E2最大 |
| C.要实现步骤1的转化,必须加热 | D.该反应的ΔH<0 |
您最近一年使用:0次
2022-09-22更新
|
173次组卷
|
2卷引用:云南省文山州广南县第二中学校2021-2022学年高二上学期12月考试化学试题
10 . 下列反应形成新化学键释放的能量大于破坏旧化学键吸收的能量的是
| A.锌和盐酸反应生成氢气 | B.柠檬酸与碳酸氢钠溶液反应 |
| C.碳与二氧化碳共热生成一氧化碳 | D.碳酸钙受热分解 |
您最近一年使用:0次
2022-09-10更新
|
262次组卷
|
3卷引用:山东省菏泽市2020-2021学年高一下学期期末考试化学试题



