名校
解题方法
1 . 下列内容与结论对应的是
| 选项 | 内容 | 结论 |
| A |  (g)变成 (g)变成 (l) (l) | 该过程的△S>0 |
| B | 硝酸铵溶于水可自发进行 | 该过程的△S<0 |
| C | 一个反应的△H>0、△S>0 | 该反应一定不能自发进行 |
| D | 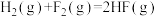 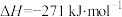 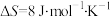 | 该反应在任何温度下均能自发进行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-14更新
|
231次组卷
|
2卷引用:山东省实验中学2022-2023学年高二上学期10月月考化学试题
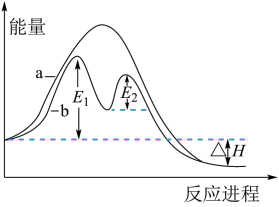
2 . 已知: 2SO2(g) + O2(g) 2SO3(g) ΔH,不同条件下反应过程能量变化如图所示。下列说法中正确的是
2SO3(g) ΔH,不同条件下反应过程能量变化如图所示。下列说法中正确的是
 2SO3(g) ΔH,不同条件下反应过程能量变化如图所示。下列说法中正确的是
2SO3(g) ΔH,不同条件下反应过程能量变化如图所示。下列说法中正确的是
| A.反应的ΔH>0 |
| B.过程b使用了催化剂,反应的ΔH= E1+ E2 |
| C.使用催化剂可以提高SO2的平衡转化率 |
| D.过程b发生两步反应,总反应速率大于过程a |
您最近一年使用:0次
2022-10-14更新
|
518次组卷
|
4卷引用:山东省枣庄市第三中学2022-2023学年高二上学期期中考试化学试题
3 . 煤和石油通常都含有硫的化合物,燃烧生成的二氧化硫为大气主要污染物之一、二氧化硫的治理已成为当前研究的课题。硫与硫的氧化物在转化过程中的能量变化如图所示。
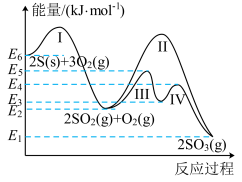
已知: 。回答下列问题:
。回答下列问题:
(1)图中的I、II、III、IV中属于放热反应的是_______ 。
(2)写出表示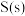 的燃烧热的热化学方程式:
的燃烧热的热化学方程式:_______ 。
(3)从图中可看出将SO2氧化成SO3有两条途径:
①SO2经过程III、过程IV转化成SO3;②SO2经过程II转化成SO3。已知过程IV的化学方程式为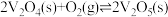 ,则过程III的热化学方程式为
,则过程III的热化学方程式为_______ 。
(4) 和
和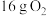 在一定条件下连续发生过程I和过程II的反应,充分反应后无固体剩余,测得放出的热量为
在一定条件下连续发生过程I和过程II的反应,充分反应后无固体剩余,测得放出的热量为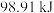 。则反应后的体系中各组分的物质的量分别为
。则反应后的体系中各组分的物质的量分别为_______ 。
(5)已知: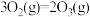
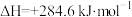 ,则相同条件下,
,则相同条件下,_______ (填“ ”或“
”或“ ”)更稳定,
”)更稳定,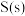 在
在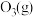 中能直接生成
中能直接生成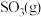 ,该反应的热化学方程式为
,该反应的热化学方程式为_______ 。

已知:
 。回答下列问题:
。回答下列问题:(1)图中的I、II、III、IV中属于放热反应的是
(2)写出表示
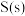 的燃烧热的热化学方程式:
的燃烧热的热化学方程式:(3)从图中可看出将SO2氧化成SO3有两条途径:
①SO2经过程III、过程IV转化成SO3;②SO2经过程II转化成SO3。已知过程IV的化学方程式为
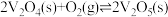 ,则过程III的热化学方程式为
,则过程III的热化学方程式为(4)
 和
和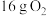 在一定条件下连续发生过程I和过程II的反应,充分反应后无固体剩余,测得放出的热量为
在一定条件下连续发生过程I和过程II的反应,充分反应后无固体剩余,测得放出的热量为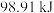 。则反应后的体系中各组分的物质的量分别为
。则反应后的体系中各组分的物质的量分别为(5)已知:
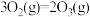
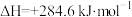 ,则相同条件下,
,则相同条件下, ”或“
”或“ ”)更稳定,
”)更稳定,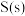 在
在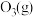 中能直接生成
中能直接生成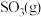 ,该反应的热化学方程式为
,该反应的热化学方程式为
您最近一年使用:0次
2022-10-11更新
|
176次组卷
|
2卷引用:山东省济南市2022-2023学年高二上学期10月份质量检测联合调考化学试题
名校
解题方法
4 . 若物质的量均为1 mol的A、B、C所具有的能量分别用Ea、Eb、Ec表示,则对于放热反应A=2B+C,下列关系错误的是
| A.2Eb+Ec>Ea | B.Ea>Ec | C.Ea>Eb+Ec | D.Ea>2Eb |
您最近一年使用:0次
2022-10-11更新
|
116次组卷
|
3卷引用:山东省济南市2022-2023学年高二上学期10月份质量检测联合调考化学试题
名校
5 . 下列反应既属于氧化还原反应,又属于放热反应的是
| A.灼热的木炭与水蒸气的反应 | B. 与水的反应 与水的反应 |
C. 受热分解 受热分解 | D. 与水的反应 与水的反应 |
您最近一年使用:0次
2022-10-11更新
|
158次组卷
|
2卷引用:山东省济南市2022-2023学年高二上学期10月份质量检测联合调考化学试题
6 . 科学家已获得了气态 分子,其空间结构为正四面体形(如图所示)。已知断裂1mol N—N键吸收193kJ能量,断裂1mol N≡N键吸收946kJ能量。下列说法正确的是
分子,其空间结构为正四面体形(如图所示)。已知断裂1mol N—N键吸收193kJ能量,断裂1mol N≡N键吸收946kJ能量。下列说法正确的是
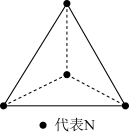
 分子,其空间结构为正四面体形(如图所示)。已知断裂1mol N—N键吸收193kJ能量,断裂1mol N≡N键吸收946kJ能量。下列说法正确的是
分子,其空间结构为正四面体形(如图所示)。已知断裂1mol N—N键吸收193kJ能量,断裂1mol N≡N键吸收946kJ能量。下列说法正确的是
A. 属于种新型化合物 属于种新型化合物 |
B.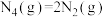 为吸热反应 为吸热反应 |
C. 的过程中吸收772kJ能量 的过程中吸收772kJ能量 |
D.以 为原料替代 为原料替代 合成等量 合成等量 时,可放出更多的热量 时,可放出更多的热量 |
您最近一年使用:0次
2022-10-11更新
|
660次组卷
|
2卷引用:山东省枣庄市第三中学2022-2023学年高二上学期10月阶段检测化学试题
7 . 受全球低碳节能环保理念、以及我国“双碳”政策的影响,“地沟油”华丽变身,用于生产生物柴油。下列说法不合理的是
| A.生物柴油不属于化石能源 |
| B.“地沟油”经过加工处理可用作生物柴油,实现了厨余垃圾的合理利用 |
| C.生物柴油的燃烧需要点燃,属于吸热反应 |
| D.生物柴油在燃烧过程中化学能主要转化为热能和光能 |
您最近一年使用:0次
2022-10-09更新
|
249次组卷
|
5卷引用:山东省济南市莱钢高级中学2022-2023学年高二上学期期中考试化学试题
名校
8 . 化学反应过程既是物质的转化过程,也是化学能与热能,电能等其他形式能量的转化过程。请根据要求回答下列与能量转化有关的问题:
I.利用如图所示装置测定中和热,取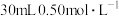 稀硫酸与
稀硫酸与 溶液进行实验,实验数据如表。
溶液进行实验,实验数据如表。
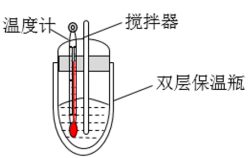
回答下列问题:
(1)若近似认为 稀硫酸与
稀硫酸与 溶液的密度均为
溶液的密度均为 (忽略溶液混合后体积变化),反应所得溶液的比热容
(忽略溶液混合后体积变化),反应所得溶液的比热容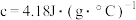 ,则实验测定中和热的数值为
,则实验测定中和热的数值为_______  (保留1位小数)。
(保留1位小数)。
(2)上述实验结果与中和热的标准数值 有偏差,产生偏差的原因不可能是因为_____。
有偏差,产生偏差的原因不可能是因为_____。
(3)如图三个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是_______ 。
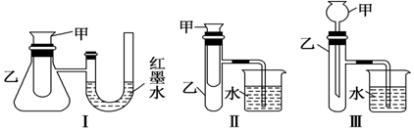
II.
(4)请用下图所示仪器装置设计一个包括:电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。
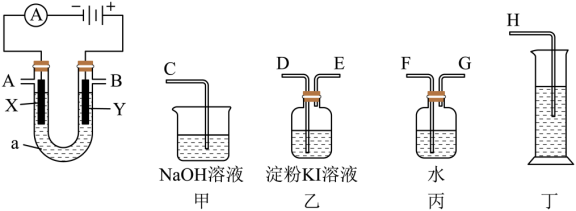
①所选仪器连接时,各接口的顺序是___________ (填各接口的字母代号):
A接______、_____接_____;B接_____、______接______;
②体现氯气的氧化性的实验现象为:_______ ,电解一段时间后,用丁测得气体体积为280mL(标准状况下);需加入_______ g(结果保留一位小数)的_______ 可使溶液复原。
| 温度 实验次数 | 起始温度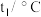 | 终止温度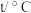 | ||
 |  | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.2 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 |
| 4 | 26.4 | 26.2 | 26.3 | 30.3 |
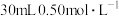 稀硫酸与
稀硫酸与 溶液进行实验,实验数据如表。
溶液进行实验,实验数据如表。
回答下列问题:
(1)若近似认为
 稀硫酸与
稀硫酸与 溶液的密度均为
溶液的密度均为 (忽略溶液混合后体积变化),反应所得溶液的比热容
(忽略溶液混合后体积变化),反应所得溶液的比热容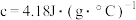 ,则实验测定中和热的数值为
,则实验测定中和热的数值为 (保留1位小数)。
(保留1位小数)。(2)上述实验结果与中和热的标准数值
 有偏差,产生偏差的原因不可能是因为_____。
有偏差,产生偏差的原因不可能是因为_____。| A.实验装置保温、隔热效果差 |
| B.用量筒量取NaOH溶液的体积时仰视读数 |
| C.分多次把NaOH溶液倒入内筒中 |
| D.测过稀硫酸的温度计未洗净直接用于测定NaOH溶液的温度 |

II.
(4)请用下图所示仪器装置设计一个包括:电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。

①所选仪器连接时,各接口的顺序是
A接______、_____接_____;B接_____、______接______;
②体现氯气的氧化性的实验现象为:
您最近一年使用:0次
9 . 下列示意图表示正确的是
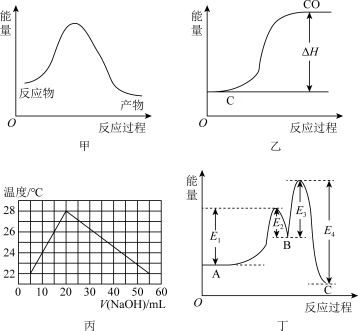

| A.甲图表示2Fe(s)+3CO2(g)=Fe2O3(s)+3CO(g) ΔH=-26.7kJ·mol-1反应的能量变化 |
| B.乙图表示碳的燃烧热 |
| C.丙图表示实验的环境温度为20℃,将物质的量浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,混合液的最高温度随V(NaOH)的变化(已知V1+V2=60mL) |
| D.已知稳定性顺序:B<A<C,某反应由两步反应A→B→C构成,反应过程中的能量变化曲线如丁图 |
您最近一年使用:0次
2022-10-08更新
|
257次组卷
|
2卷引用:山东省德州市第一中学2022-2023学年高二上学期10月月考化学试题
10 . 研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
(1)反应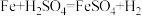 的能量变化如图1所示。
的能量变化如图1所示。
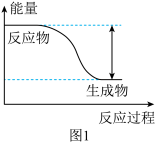
①该反应为_______ (填“吸热”或“放热”)反应。
②图2的3个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是_______ 。
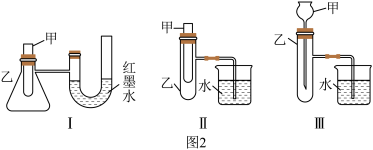
(2)现有纯铁片、纯铜片、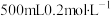 的硫酸溶液、导线和
的硫酸溶液、导线和 量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且 量筒中已充满了水。
量筒中已充满了水。
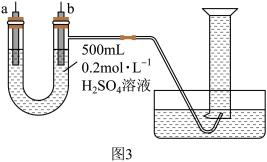
①若a、b极不用导线相连,则b极材料为_______ (填“纯铁片”或“纯铜片”)。
②将a、b极(a极为“纯铁片”,b极为“纯铜片”)用导线相连,则电子在导线上的流动方向为从_______ 到(填“a极”或“b极”,下同)_______ ;此时a极的电极反应式为_______ 。
③根据上述实验所得结论为_______ 。
(1)反应
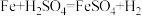 的能量变化如图1所示。
的能量变化如图1所示。
①该反应为
②图2的3个装置中,不能证明“铁与稀硫酸反应是吸热反应还是放热反应”的是

(2)现有纯铁片、纯铜片、
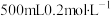 的硫酸溶液、导线和
的硫酸溶液、导线和 量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率。所用装置如图3所示,装置气密性良好,且 量筒中已充满了水。
量筒中已充满了水。
①若a、b极不用导线相连,则b极材料为
②将a、b极(a极为“纯铁片”,b极为“纯铜片”)用导线相连,则电子在导线上的流动方向为从
③根据上述实验所得结论为
您最近一年使用:0次



