名校
1 . 硫磺(主要成份:S)和黄铁矿(主要成份: )均是工业制取硫酸的主要原料。
)均是工业制取硫酸的主要原料。
Ⅰ.已知:①单质硫的燃烧热为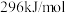
②

(1)写出由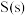 生成
生成 的热化学反应方程式
的热化学反应方程式_______
Ⅱ.黄铁矿因其浅黄铜色和明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。某兴趣小组设计如下实验方案,测定某高纯黄铁矿石中硫元素的含量。
称取 该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
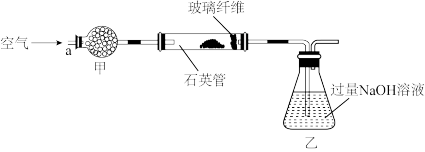
(2)写出石英管中发生反应的化学方程式:_______ 。
(3)上图中,干燥管甲内所盛试剂是_______ 。
(4)有同学提出该实验装置存在安全 隐患,请用简洁的文字说明:_______ 。
反应结束后,将乙瓶中的溶液进行如下处理:
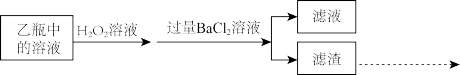
(5)为准确 测定该黄铁矿石中硫元素的质量分数,请将上述步骤补充完整_______ 。
(6)某同学设计如下实验,探究反应后乙瓶中溶液所含的阴离子种类 ,请完成下列表格
 )均是工业制取硫酸的主要原料。
)均是工业制取硫酸的主要原料。Ⅰ.已知:①单质硫的燃烧热为
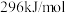
②


(1)写出由
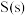 生成
生成 的热化学反应方程式
的热化学反应方程式Ⅱ.黄铁矿因其浅黄铜色和明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。某兴趣小组设计如下实验方案,测定某高纯黄铁矿石中硫元素的含量。
称取
 该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
(2)写出石英管中发生反应的化学方程式:
(3)上图中,干燥管甲内所盛试剂是
(4)有同学提出该实验装置存在
反应结束后,将乙瓶中的溶液进行如下处理:
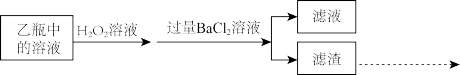
(5)为
(6)某同学设计如下实验,探究反应后乙瓶中溶液所含的
| 步骤 | 实验操作 | 现象及结论 |
| a | 取适量锥形瓶乙中反应后的溶液,滴加足量稀盐酸至不再有气泡产生,将所产生的气体通入到足量 | 红色褪去,说明有 |
| b | 取步骤a所得溶液,滴加 | 有白色沉淀产生,说明有 |
| c | 另取适量锥形瓶乙中反应后的溶液, | 溶液变红,说明有 |
您最近一年使用:0次
名校
解题方法
2 . 利用 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。
(1)20世纪初,工业上以 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
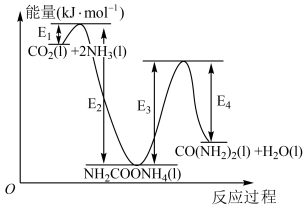
①反应物液氨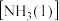 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在___________ (填作用力名称)。
②写出在该条件下由 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:___________ 。
(2)近年研究发现,电催化 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
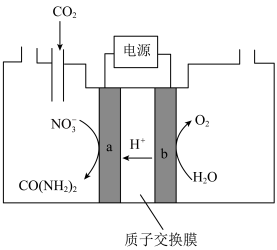
①电解过程中生成尿素的电极反应式为___________ 。
②目前以 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到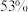 的法拉第效率
的法拉第效率 。已知:
。已知: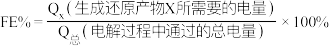 ,其中,
,其中,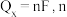 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下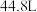 的
的 ,可获得尿素的质量为
,可获得尿素的质量为___________ 。(尿素的相对分子质量:60)
(3)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。

①消化液中的含氮粒子是___________ 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。
 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。(1)20世纪初,工业上以
 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
①反应物液氨
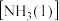 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在②写出在该条件下由
 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:(2)近年研究发现,电催化
 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
①电解过程中生成尿素的电极反应式为
②目前以
 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到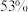 的法拉第效率
的法拉第效率 。已知:
。已知: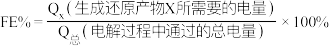 ,其中,
,其中,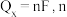 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下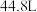 的
的 ,可获得尿素的质量为
,可获得尿素的质量为(3)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近一年使用:0次
3 . “碳达峰·碳中和”是我国社会发展重大战略之一,研究甲烷的燃烧技术可减少CO2的排放并实现资源利用。
Ⅰ.甲烷直接燃烧可达到2800℃左右的高温,主要发生反应ⅰ,可能发生副反应ⅱ。
ⅰ.
ⅱ.
ⅲ.……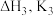
(1)利用 和
和 计算
计算 时,反应ⅲ是
时,反应ⅲ是_______ ;
_______ (用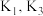 表示)。
表示)。
Ⅱ.化学链燃烧技术有利于 的捕获和综合利用。较高温度下,将恒定流速的
的捕获和综合利用。较高温度下,将恒定流速的 在
在 时刻通入反应器与载氧体
时刻通入反应器与载氧体 反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后,
反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后, 时刻向反应器中通入一段时间氩气,
时刻向反应器中通入一段时间氩气, 时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
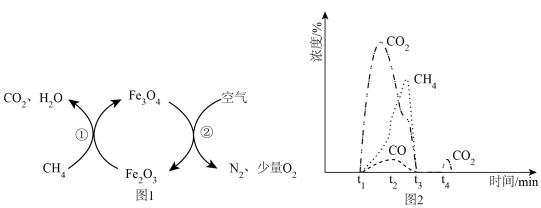
(2)①的化学反应方程式是_______ ,载氧体的主要作用是_______ (填“提供电子”或“接受电子”)。
(3)恒压条件下,反应①在某密闭容器中反应,平衡后通入 气,测得一段时间内
气,测得一段时间内 物质的量上升,其原因是
物质的量上升,其原因是_______ 。
(4)结合图2,依据 时刻产生
时刻产生 ,用化学方程式及简要文字解释
,用化学方程式及简要文字解释 时刻流出
时刻流出 速率突然增大的可能原因
速率突然增大的可能原因_______ 。
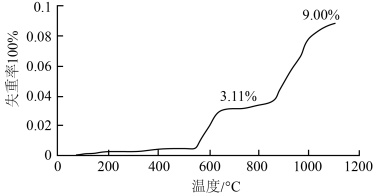
已知:失重率=
Ⅲ.某同学采用重量分析法探究载氧体的还原产物及循环效果,实验过程如下:在装置中放置一定量的 ,加热条件下通入足量
,加热条件下通入足量 ,充分均匀反应,分析固体失重率。
,充分均匀反应,分析固体失重率。
(5) 时载氧体的还原产物主要为
时载氧体的还原产物主要为 。
。结合简单计算 说明 时,载氧体的主要还原产物为
时,载氧体的主要还原产物为_______ ,依据是_______ 。
Ⅳ.有人设想利用“ ”间的转化实现
”间的转化实现 的化学链燃烧过程,按图1的呈现方式。
的化学链燃烧过程,按图1的呈现方式。
(6)将该转化关系在虚线框内画出_______ 。

Ⅰ.甲烷直接燃烧可达到2800℃左右的高温,主要发生反应ⅰ,可能发生副反应ⅱ。
ⅰ.

ⅱ.

ⅲ.……
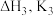
(1)利用
 和
和 计算
计算 时,反应ⅲ是
时,反应ⅲ是
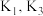 表示)。
表示)。Ⅱ.化学链燃烧技术有利于
 的捕获和综合利用。较高温度下,将恒定流速的
的捕获和综合利用。较高温度下,将恒定流速的 在
在 时刻通入反应器与载氧体
时刻通入反应器与载氧体 反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后,
反应,原理如图1所示,流出气体中各组分的浓度随反应时间变化如图2所示。待反应①完成后, 时刻向反应器中通入一段时间氩气,
时刻向反应器中通入一段时间氩气, 时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
时刻再通入一段时间空气,发生反应②,实现载氧体的循环再生。
(2)①的化学反应方程式是
(3)恒压条件下,反应①在某密闭容器中反应,平衡后通入
 气,测得一段时间内
气,测得一段时间内 物质的量上升,其原因是
物质的量上升,其原因是(4)结合图2,依据
 时刻产生
时刻产生 ,用化学方程式及简要文字解释
,用化学方程式及简要文字解释 时刻流出
时刻流出 速率突然增大的可能原因
速率突然增大的可能原因
已知:失重率=

Ⅲ.某同学采用重量分析法探究载氧体的还原产物及循环效果,实验过程如下:在装置中放置一定量的
 ,加热条件下通入足量
,加热条件下通入足量 ,充分均匀反应,分析固体失重率。
,充分均匀反应,分析固体失重率。(5)
 时载氧体的还原产物主要为
时载氧体的还原产物主要为 。
。 时,载氧体的主要还原产物为
时,载氧体的主要还原产物为Ⅳ.有人设想利用“
 ”间的转化实现
”间的转化实现 的化学链燃烧过程,按图1的呈现方式。
的化学链燃烧过程,按图1的呈现方式。(6)将该转化关系在虚线框内画出

您最近一年使用:0次
4 . 由某精矿石(MCO3·ZCO3)可以制备单质M,制备过程中排放出的二氧化碳可以作为原料制备甲醇,取该矿石样品1.84g,高温灼烧至恒重,得到0.96g仅含两种金属氧化物的固体,其中m(M)︰m(Z)=3:5,请回答:
(1)该矿石的化学式为_______ 。
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2︰1)。写出该反应的化学方程式_______ 。
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是_______ 。
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g) CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1
反应2:CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
反应3:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。

则△H3_______ △H2 (填“大于”、“小于”、“等于”),理由是_______ 。
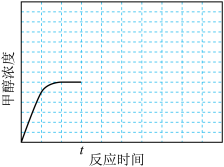
(4)在温度T1时,使体积比为3︰1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。_______
(1)该矿石的化学式为
(2)①以该矿石灼烧后的固体产物为原料,真空高温条件下用单质硅还原,仅得到单质M和一种含氧酸盐(只含Z、Si和O元素,且Z和Si的物质的量之比为2︰1)。写出该反应的化学方程式
②单质M还可以通过电解熔融MCl2得到,不能用电解MCl2溶液的方法制备M的理由是
(3)一定条件下,由CO2和H2制备甲醇的过程中含有下列反应:
反应1:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1反应2:CO(g)+2H2(g)
 CH3OH(g) △H2
CH3OH(g) △H2反应3:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3其对应的平衡常数分别为K1、K2、K3,它们随温度变化的曲线如图所示。

则△H3
(4)在温度T1时,使体积比为3︰1的H2和CO2在体积恒定的密闭容器内进行反应。T1温度下甲醇浓度随时间变化曲线如图所示;不改变其他条件,假定t时刻迅速降温到T2,一段时间后体系重新达到平衡。试在图中画出t时刻后甲醇浓度随时间变化至平衡的示意曲线。

您最近一年使用:0次
2014·江苏南通·三模
5 . 一氧化碳被广泛应用于冶金工业和电子工业。
(1)高炉炼铁是最为普遍的炼铁方法,相关反应的热化学方程式如下:
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H=akJ·mol-1
CO(g)+3Fe2O3(s)=CO2(g)+2Fe3O4(s) △H=bkJ·mol-1
反应3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)的△H=______ kJ·mol-1(用含a、b 的代数式表示)。
(2)电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g)⇌HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g)⇌CH3OH(g) +CO(g) △H>0
①第一步反应的机理可以用下图表示:

图中中间产物X的结构简式为______ 。
②在工业生产中,为提高CO的产率,可采取的合理措施有______ 。
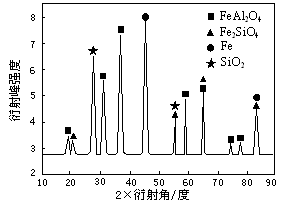
(3)为进行相关研究,用CO还原高铝铁矿石,反应后固体物质的X—射线衍射谱图如图所示(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。反应后混合物中的一种产物能与盐酸反应生产两种盐,该反应的离子方程式为______ 。
(4)某催化剂样品(含Ni2O340%,其余为SiO2)通过还原、提纯两步获得镍单质:首先用CO将33.2 g样品在加热条件下还原为粗镍;然后在常温下使粗镍中的Ni与CO结合成Ni(CO)4(沸点43 ℃),并在180 ℃时使Ni(CO)4重新分解产生镍单质。上述两步中消耗CO的物质的量之比为______ 。
(5)为安全起见,工业生产中需对空气中的CO进行监测。
①粉红色的PdCl2溶液可以检验空气中少量的CO。若空气中含CO,则溶液中会产生黑色的Pd沉淀。每生成5.3gPd沉淀,反应转移电子数为______ 。
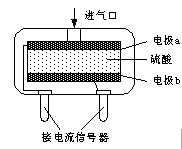
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其结构如图所示。这种传感器利用原电池原理,则该电池的负极反应式为______ 。
(1)高炉炼铁是最为普遍的炼铁方法,相关反应的热化学方程式如下:
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H=akJ·mol-1
CO(g)+3Fe2O3(s)=CO2(g)+2Fe3O4(s) △H=bkJ·mol-1
反应3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)的△H=
(2)电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g)⇌HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g)⇌CH3OH(g) +CO(g) △H>0
①第一步反应的机理可以用下图表示:

图中中间产物X的结构简式为
②在工业生产中,为提高CO的产率,可采取的合理措施有
(3)为进行相关研究,用CO还原高铝铁矿石,反应后固体物质的X—射线衍射谱图如图所示(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。反应后混合物中的一种产物能与盐酸反应生产两种盐,该反应的离子方程式为

(4)某催化剂样品(含Ni2O340%,其余为SiO2)通过还原、提纯两步获得镍单质:首先用CO将33.2 g样品在加热条件下还原为粗镍;然后在常温下使粗镍中的Ni与CO结合成Ni(CO)4(沸点43 ℃),并在180 ℃时使Ni(CO)4重新分解产生镍单质。上述两步中消耗CO的物质的量之比为
(5)为安全起见,工业生产中需对空气中的CO进行监测。
①粉红色的PdCl2溶液可以检验空气中少量的CO。若空气中含CO,则溶液中会产生黑色的Pd沉淀。每生成5.3gPd沉淀,反应转移电子数为
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其结构如图所示。这种传感器利用原电池原理,则该电池的负极反应式为

您最近一年使用:0次



