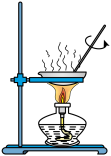
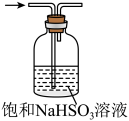
1 . 下列装置中能达到实验目的的是
A.灼烧 固体制得 固体制得 | B.定量测定化学反应速率 |
|
|
| C.保存液溴 | D.除去 中的HCl 中的HCl |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列实验操作不能达到实验目的的是


| A.用装置甲测定化学反应速率 | B.用装置乙探究温度对化学平衡的影响 |
| C.用装置丙测定中和反应的反应热 | D.用装置丁验证AgCl和AgI的Ksp大小 |
您最近一年使用:0次
名校
解题方法
3 . 某校化学小组的同学开展了一系列的化学实验活动。
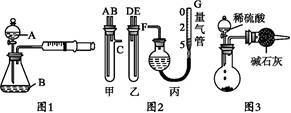
请你参与实验并完成下列问题:
(1)甲同学用图1所示装置,测量锌与硫酸反应速率:把2 g锌粒放入锥形瓶内,通过分液漏斗加入1 mol·L-1稀硫酸40 mL,收集10 mL气体,通过记录______ 得到反应速率为x mol·(L·min)-1.实验开始时检查该装置气密性的方法是______ 。
(2)乙同学用图2装置测定Na2CO3和NaCl的固体混合物中Na2CO3的质量分数:
①甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则固体混合物和稀硫酸应分别置于______ 、__ 仪器中(填仪器编号);
②G管可以用化学实验室里的一种常用仪器来替代,这种仪器是______ ;
③仪器甲、乙接口的连接方式如下:A连接__ ,B连接______ ,C连接______ (填写各接口的编号);
④为提高测量的准确性,收集完气体后,丙装置读数前应进行的操作是______ 。
(3)丙同学与甲同学实验目的相同:用图3装置测定生成的CO2的质量,但该装置存在明显缺陷,从而导致实验误差_____ ,请你分析其中使测定结果可能偏大的主要原因______ 。

请你参与实验并完成下列问题:
(1)甲同学用图1所示装置,测量锌与硫酸反应速率:把2 g锌粒放入锥形瓶内,通过分液漏斗加入1 mol·L-1稀硫酸40 mL,收集10 mL气体,通过记录
(2)乙同学用图2装置测定Na2CO3和NaCl的固体混合物中Na2CO3的质量分数:
①甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则固体混合物和稀硫酸应分别置于
②G管可以用化学实验室里的一种常用仪器来替代,这种仪器是
③仪器甲、乙接口的连接方式如下:A连接
④为提高测量的准确性,收集完气体后,丙装置读数前应进行的操作是
(3)丙同学与甲同学实验目的相同:用图3装置测定生成的CO2的质量,但该装置存在明显缺陷,从而导致实验误差
您最近一年使用:0次
4 . 2021年国务院政府工作报告时指出:优化产业结构和能源结构,扎实做好碳达峰、碳中和各项工作。
(1)利用工业废气中的CO2可制取甲醇,其反应为: CO2+3H2 CH3OH+H2O。
CH3OH+H2O。
①常温常压下,已知反应的能量变化如图1、图2所示,由二氧化碳和氢气制备甲醇的热化学方程式为_______ 。
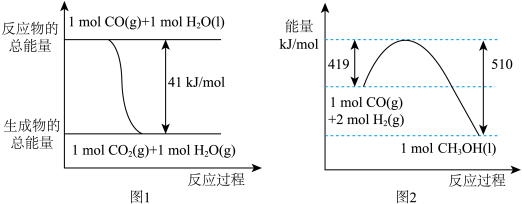
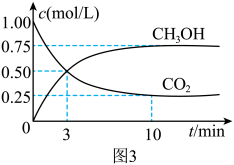
②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入1molCO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图3所示。从反应开始到平衡,v(H2)=_______ mol·L-1·min-1;能使平衡体系中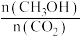 增大的措施有
增大的措施有_______ (任写一条)。
(2)已知CO2(g)+ H2(g) HCOOH(g) ΔH= -31.4 kJ·mol-1。
HCOOH(g) ΔH= -31.4 kJ·mol-1。
①温度为T1°C时,将等物质的量的CO2和H2充入体积为1 L的密闭容器中发生反应:CO2(g)+ H2(g) HCOOH(g) K=2,实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正 、k逆为速率常数。T1°C时,k正=
HCOOH(g) K=2,实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正 、k逆为速率常数。T1°C时,k正=_______ k逆。
②温度为T2°C时,k正=1.9k逆, 则T2°C时平衡压强_______ (填“> ”“<”或“=”)T1°C时平衡压强,理由是_______ 。
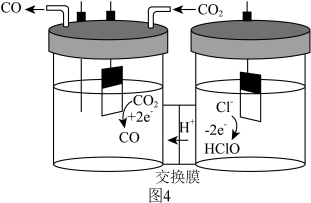
(3)我国科学家设计了一种将电解饱和食盐水与电催化还原CO2相耦合的电解装置(如图4)。阴极上的电极反应式为:_______ 。
(1)利用工业废气中的CO2可制取甲醇,其反应为: CO2+3H2
 CH3OH+H2O。
CH3OH+H2O。①常温常压下,已知反应的能量变化如图1、图2所示,由二氧化碳和氢气制备甲醇的热化学方程式为

②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入1molCO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如图3所示。从反应开始到平衡,v(H2)=
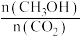 增大的措施有
增大的措施有
(2)已知CO2(g)+ H2(g)
 HCOOH(g) ΔH= -31.4 kJ·mol-1。
HCOOH(g) ΔH= -31.4 kJ·mol-1。①温度为T1°C时,将等物质的量的CO2和H2充入体积为1 L的密闭容器中发生反应:CO2(g)+ H2(g)
 HCOOH(g) K=2,实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正 、k逆为速率常数。T1°C时,k正=
HCOOH(g) K=2,实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正 、k逆为速率常数。T1°C时,k正=②温度为T2°C时,k正=1.9k逆, 则T2°C时平衡压强
(3)我国科学家设计了一种将电解饱和食盐水与电催化还原CO2相耦合的电解装置(如图4)。阴极上的电极反应式为:

您最近一年使用:0次
5 . 联氨(N2H4)又称肼,是一种应用广泛的化工原料;次磷酸钠( NaH2PO2 )是常用的次磷酸盐。二者都是重要的还原剂。
(1)已知:①2N2H4(l) +N2O4(l) =3N2(g) +4H2O(g) △H1= - 1038. 7kJ∙mol-1
②N2O4(l) =N2(g) +2O2(g) △H2= +204.3 kJ∙mol -1
③H2O(g) = H2O(l) △H3= -44 kJ∙mol -1
请写出表示N2H4(l)的燃烧热的热化学方程式_______ 。
(2)已知反应N2H4(g) + 2Cl2(g)⇌N2(g) +4HCl(g) ,T°C时,向V L恒容密闭容器中加入2 mol N2H4(g)和4 mol Cl2(g) ;测得Cl2和HCl的浓度随时间的关系如图所示。
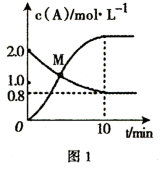
①0~ 10 min内,用HCl( g)表示的平均反应速率:v(HCl)=_______ 。
②M点时,Cl2的转化率为_______ % (精确到0.1)。
③T °C时,达到平衡后再向该容器中加入1.2 mol N2H4(g) 0.4 mol Cl2 (g)、0.8 mol N2(g)、1. 2 mol HCl(g), 此时平衡_______ (填“正向移动”“逆向移动’'或“不移动”)。
(3)①次磷酸(H3PO2)是一元弱酸,常温下,1.0 mol•L-1的NaH2PO2溶液pH为8,则次磷酸的Ka =_______ 。
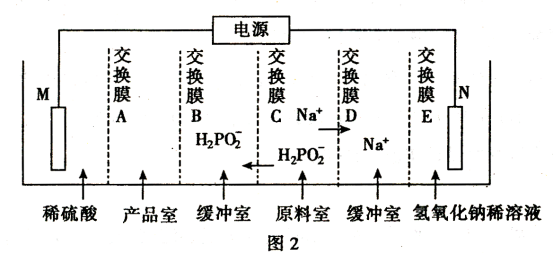
②用次磷酸钠通过电渗析法制备次磷酸,装置如图2所示。交换膜A属于_______ (填“阳离子”或“阴离子”)交换膜,电极N的电极反应式为_______ ,当电路中流过1.9264×105库仑电量时,制得次磷酸的物质的量为_______ (结果取整数) (已知一个电子的电量为1.6×10-19库仑,NA数值约为6.02×1023)。
(1)已知:①2N2H4(l) +N2O4(l) =3N2(g) +4H2O(g) △H1= - 1038. 7kJ∙mol-1
②N2O4(l) =N2(g) +2O2(g) △H2= +204.3 kJ∙mol -1
③H2O(g) = H2O(l) △H3= -44 kJ∙mol -1
请写出表示N2H4(l)的燃烧热的热化学方程式
(2)已知反应N2H4(g) + 2Cl2(g)⇌N2(g) +4HCl(g) ,T°C时,向V L恒容密闭容器中加入2 mol N2H4(g)和4 mol Cl2(g) ;测得Cl2和HCl的浓度随时间的关系如图所示。

①0~ 10 min内,用HCl( g)表示的平均反应速率:v(HCl)=
②M点时,Cl2的转化率为
③T °C时,达到平衡后再向该容器中加入1.2 mol N2H4(g) 0.4 mol Cl2 (g)、0.8 mol N2(g)、1. 2 mol HCl(g), 此时平衡
(3)①次磷酸(H3PO2)是一元弱酸,常温下,1.0 mol•L-1的NaH2PO2溶液pH为8,则次磷酸的Ka =
②用次磷酸钠通过电渗析法制备次磷酸,装置如图2所示。交换膜A属于

您最近一年使用:0次