名校
解题方法
1 . 某化学兴趣小组进行以下实验探究。
Ⅰ.设计实验探究反应速率的测定和比较实验步骤:
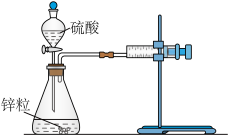
(1)用如图所示装置,加入 的稀硫酸溶液,测量收集
的稀硫酸溶液,测量收集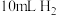 所需的时间。
所需的时间。
(2)另取一套相同的装置,加入40 mL 4 mol·L-1的稀硫酸溶液,测量收集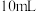 (相同条件下)
(相同条件下) 所需的时间。
所需的时间。
实验现象:锌跟稀硫酸反应产生气泡,收集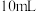 气体,(2)所用时间比(1)所用时间
气体,(2)所用时间比(1)所用时间__________ (填“长”或“短”)
实验结论: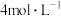 的稀硫酸与锌反应比
的稀硫酸与锌反应比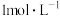 的稀硫酸与锌反应速率
的稀硫酸与锌反应速率___________ (填“大”或“小”):
注意事项:①锌粒的质量、颗粒(即表面积)大小___________ ;
②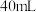 的硫酸要迅速加入;
的硫酸要迅速加入;
③装置____________ ,且计时要迅速准确;
④气体收集可以用排水量气装置代替。
实验讨论:除本实验测定反应速率的方法外,可行的方案还有_________________________ (任写一种)。
Ⅱ.利用 与大理石反应来研究影响反应速率的因素,所用
与大理石反应来研究影响反应速率的因素,所用 浓度为
浓度为 、
、 ,大理石有细颗粒与粗颗粒两种规格,实验温度为
,大理石有细颗粒与粗颗粒两种规格,实验温度为 、
、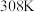 。
。
请完成以下实验设计表。
Ⅰ.设计实验探究反应速率的测定和比较实验步骤:

(1)用如图所示装置,加入
 的稀硫酸溶液,测量收集
的稀硫酸溶液,测量收集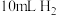 所需的时间。
所需的时间。(2)另取一套相同的装置,加入40 mL 4 mol·L-1的稀硫酸溶液,测量收集
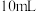 (相同条件下)
(相同条件下) 所需的时间。
所需的时间。实验现象:锌跟稀硫酸反应产生气泡,收集
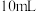 气体,(2)所用时间比(1)所用时间
气体,(2)所用时间比(1)所用时间实验结论:
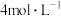 的稀硫酸与锌反应比
的稀硫酸与锌反应比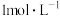 的稀硫酸与锌反应速率
的稀硫酸与锌反应速率注意事项:①锌粒的质量、颗粒(即表面积)大小
②
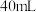 的硫酸要迅速加入;
的硫酸要迅速加入;③装置
④气体收集可以用排水量气装置代替。
实验讨论:除本实验测定反应速率的方法外,可行的方案还有
Ⅱ.利用
 与大理石反应来研究影响反应速率的因素,所用
与大理石反应来研究影响反应速率的因素,所用 浓度为
浓度为 、
、 ,大理石有细颗粒与粗颗粒两种规格,实验温度为
,大理石有细颗粒与粗颗粒两种规格,实验温度为 、
、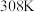 。
。请完成以下实验设计表。
| 实验编号 | T/K | 大理石规格 | 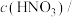  | 实验目的 |
| ① | 298 | 粗颗粒 |  | (1)实验①和②探究 浓度对该反应速率的影响; 浓度对该反应速率的影响;(2)实验①和 (3)实验①和 |
| ② | ||||
| ③ | 粗颗粒 | |||
| ④ |
您最近一年使用:0次
2020-10-11更新
|
145次组卷
|
3卷引用:江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷B卷化学试题
2 . 下列实验装置能达到实验目的的是


A.用装置甲定量测定 的分解速率 的分解速率 |
B.用装置乙蒸干 溶液制备无水 溶液制备无水 固体 固体 |
C.用装置丙制备 并能较长时间观察其颜色 并能较长时间观察其颜色 |
| D.用装置丁采集到的压强数据判断铁钉发生吸氧腐蚀还是析氢腐蚀 |
您最近一年使用:0次
2022-06-29更新
|
235次组卷
|
3卷引用:江苏省常州市教育学会2021-2022学年高二下学期期末学业水平监测化学试题
名校
3 . 用下列实验装置进行相应实验,能达到实验目的的是


| A.用甲装置测定一定时间内产生氢气的体积,可测定该反应的速率 |
| B.用乙所示方法探究固体表面积对反应速率的影响 |
| C.用丙装置制备Fe(OH)3胶体 |
| D.用丁装置蒸发结晶制AlCl3晶体 |
您最近一年使用:0次
名校
4 . 用下列实验装置和方法进行的相应实验,能达到实验目的的是


| A.用甲装置比较盐酸、碳酸和硅酸的酸性强弱 |
| B.用乙所示方法检验装置的气密性 |
| C.用丙装置制备和收集氨气 |
| D.用丁装置测定化学反应速率 |
您最近一年使用:0次
2017-06-24更新
|
515次组卷
|
3卷引用:江苏省启东中学2016-2017学年高一下学期期终化学试题
5 . 某学生为探究锌与稀盐酸反应的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00mol·L-1、2.00mol·L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g。实验温度为25℃、35℃。(已知Zn2+对该反应速率无影响)
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30~40s范围内盐酸的平均反应速率ν(HCl)=___________ (忽略溶液体积变化);
②反应速率最大的时间段(如0~10s)为___________ ,可能原因是___________ ;
③反应速率后段明显下降的主要影响因素是___________ 。
(3)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。___________ 现象,比较得出Fe3+和Cu2+对H2O2分解的催化效果结论;
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是___________ 。
(1)请在实验目的一栏中的空白项处填出对应的实验编号:
| 编号 | t/℃ | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | I.实验①和②探究盐酸浓度对该反应速率的影响; Ⅱ.实验 Ⅲ.实验 |
| ② | 25 | 粗颗粒 | 1.00 | |
| ③ | 35 | 粗颗粒 | 2.00 | |
| ④ | 25 | 细颗粒 | 2.00 |
(2)实验①记录如下(换算成标况):
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积/mL | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(如0~10s)为
③反应速率后段明显下降的主要影响因素是
(3)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如图所示的实验。
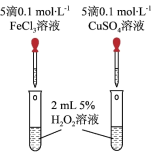
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
您最近一年使用:0次
名校
6 . 下列操作能达到实验目的的是
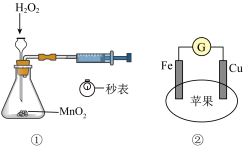
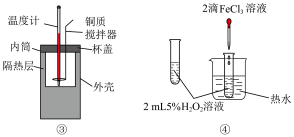


| A.用图①装置测定化学反应速率 |
| B.图②中苹果酸的结构简式为HOOCCH(OH)CH2COOH,铜片上可能发生的反应为:HOOCCH(OH)CH2COOH+2e-=-OOCCH(OH)CH2COO-+H2↑ |
| C.图③可用于中和反应热的测定 |
| D.图④验证FeCl3对H2O2分解反应有催化作用 |
您最近一年使用:0次
2023-06-17更新
|
176次组卷
|
2卷引用:江苏省苏州震泽中学2023~2024学年高二上学期10月月考化学试题
名校
7 . 下列实验操作能达到实验目的的是
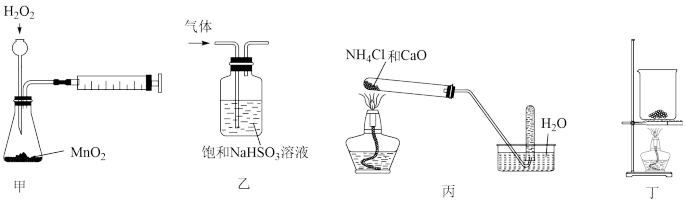

| A.用装置甲测定化学反应速率 | B.用装置乙除去SO2中的少量HCl |
| C.用装置丙制取并收集NH3 | D.用装置丁干燥NaHCO3 |
您最近一年使用:0次
解题方法
8 . 下列实验操作不能 达到实验目的的是
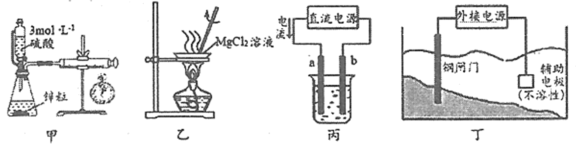

| A.用装置甲测定硫酸与锌反应的化学反应速率 |
| B.用装置乙制取无水氯化镁 |
| C.用装置丙电解精炼铜,a为粗铜,b为精铜 |
| D.用装置丁保护钢闸门,其中钢闸门与电源的负极相连 |
您最近一年使用:0次
9 . 某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下。
【实验目的】测量锌和稀硫酸反应的速率。
【实验用品】锥形瓶、双孔塞、分液漏斗、直角导管、50 mL注射器、铁架台、秒表、锌粒、1 mol·L-1的H2SO4溶液、4 mol·L-1的H2SO4溶液。

【实验步骤】
①甲同学取一套如图装置,加入40 mL 1 mol·L-1的H2SO4溶液,测量收集10 mL H2所需的时间。
②乙同学取另一套同样的装置,加入40 mL 4 mol·L-1的H2SO4溶液,测量收集10 mL H2所需的时间。
回答下列问题:
(1)Zn与稀H2SO4反应的离子方程式为____________________________ 。
(2)收集10 mL H2所需时间:甲________ 乙(填“大于”、“小于”或“等于”);反应速率:甲________ 乙(填“大于”、“小于”或“等于”)。
(3)下列说法正确的是________ (填序号)。
a.本实验中甲、乙两同学所用锌粒的表面积要相同
b.装置气密性要好
c.40 mL的H2SO4溶液要迅速加入
d.测量气体体积还可以用排水法
e.若用98%的浓H2SO4,则反应最快
【实验目的】测量锌和稀硫酸反应的速率。
【实验用品】锥形瓶、双孔塞、分液漏斗、直角导管、50 mL注射器、铁架台、秒表、锌粒、1 mol·L-1的H2SO4溶液、4 mol·L-1的H2SO4溶液。

【实验步骤】
①甲同学取一套如图装置,加入40 mL 1 mol·L-1的H2SO4溶液,测量收集10 mL H2所需的时间。
②乙同学取另一套同样的装置,加入40 mL 4 mol·L-1的H2SO4溶液,测量收集10 mL H2所需的时间。
回答下列问题:
(1)Zn与稀H2SO4反应的离子方程式为
(2)收集10 mL H2所需时间:甲
(3)下列说法正确的是
a.本实验中甲、乙两同学所用锌粒的表面积要相同
b.装置气密性要好
c.40 mL的H2SO4溶液要迅速加入
d.测量气体体积还可以用排水法
e.若用98%的浓H2SO4,则反应最快
您最近一年使用:0次
解题方法
10 . 下列图中的实验方案,不 能达到实验目的的是( )
A.依据2Fe3+(aq)+Cu(s)=Cu2+(aq)+2Fe2+(aq)设计如图甲装置的原电池 |
B.利用图乙装置验证氯化钠溶液(含酚酞)电解产物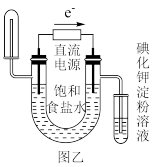 |
C.利用图丙装置测定中和热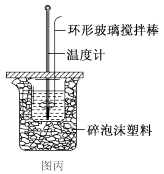 |
D.利用图丁装置探究浓度对化学反应速率的影响 |
您最近一年使用:0次



