19. 氮和氮的化合物在工农业生产、国防和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂,可由Cl
2和NO在一定条件下通过以下反应制得:2NO+Cl
2=2ClNO,已知几种化学键的键能数据如下表所示:
| 化学键 | Cl-Cl | Cl-N | N=O | N=O(NO) |
| 键能(kJ·mol-1) | 243 | a | 607 | 630 |
请根据表中数据计算:2NO(g)+Cl
2(g)=2ClNO(g)△
H=
___kJ•mol
-1。
(2)温度一定时,在一个体积为1L的密闭容器中通入2molNO和1molCl
2,10min时ClNO体积占气体总体积40%(气体的“体积分数”即“物质的量分数”),则反应开始到10min内NO的平均反应速率:v(NO)=
___mol·L
-1·min
-1(3)以NH
3为还原剂在脱硝装置中消除烟气中的氮氧化物,
主反应为4NH
3(g)+4NO(g)+O
2(g)=4N
2(g)+6H
2O(g) △
H1副反应:4NH
3(g)+3O
2(g)=2N
2(g)+6H
2O(g) △
H2=-1267.1kJ/mol
4NH
3(g)+5O
2(g)=4NO(g)+6H
2O(g) △
H3=-907.3kJ/mol
①△
H1=
___。
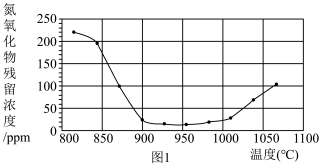
②将烟气按一定的流速通过脱硝装置,测得出口NO的浓度与温度的关系如图1,试分析脱硝的适宜温度是
___(填序号)
a.<850℃
b.900~1000℃
c.>1050 ℃
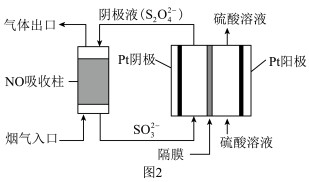
(4)以连二亚硫酸盐(S
2O
42-)为还原剂脱除烟气中的NO,并通过电解再生,装置如图2。阴极的电极反应式为
___。
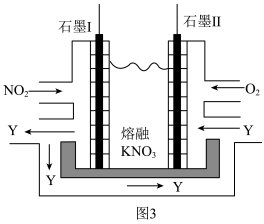
(5)利用电化学原理,将NO
2、O
2和熔融KNO
3制成燃料电池,装置如图3所示,电池工作时,NO
2转变成绿色硝化剂Y(N
2O
5),可循环使用,则石墨Ⅰ附近发生的电极反应式为:
___。