解题方法
1 . 一定条件下,向容积为4 L的密闭容器中通入4 mol SO2和a mol O2发生如下反应:2SO2+O2 2SO3,经过5 min反应达到平衡,SO3的浓度为0.9 mol·Lˉ1,容器内的压强变为原来的80%。请回答:
2SO3,经过5 min反应达到平衡,SO3的浓度为0.9 mol·Lˉ1,容器内的压强变为原来的80%。请回答:
(1)平衡时SO2的浓度____ mol·L-1。
(2)a=____ 。
 2SO3,经过5 min反应达到平衡,SO3的浓度为0.9 mol·Lˉ1,容器内的压强变为原来的80%。请回答:
2SO3,经过5 min反应达到平衡,SO3的浓度为0.9 mol·Lˉ1,容器内的压强变为原来的80%。请回答:(1)平衡时SO2的浓度
(2)a=
您最近一年使用:0次
9-10高一下·河北唐山·期中
名校
解题方法
2 . 在一体积固定的密闭容器中加入反应物A、B,发生如下反应:A+2B=3C。反应经2min后,A的浓度从开始时的1.0mol·L-1降到0.8mol·L-1。已知反应开始时B的浓度是1.2mol·L-1。
(1)2min末B、C的浓度____ 。
(2)用A表示该反应2min内的平均速率____ 。
(1)2min末B、C的浓度
(2)用A表示该反应2min内的平均速率
您最近一年使用:0次
2022-02-10更新
|
737次组卷
|
7卷引用:2009---2010学年唐山二中高一第二学期期中化学试卷
(已下线)2009---2010学年唐山二中高一第二学期期中化学试卷(已下线)2011-2012学年广东省梅州市曾宪梓中学高一5月月考化学试卷陕西省西安中学2019-2020学年高一下学期期中考试(平行班)化学试题(已下线)6.1.1 化学反应速率-2021-2022学年高一化学10分钟课前预习练(苏教版2019必修第二册)江苏省扬州市江都区邵伯高级中学2020-2021学年高一下学期期中考试化学试题苏教2020版化学必修第二册专题6第一单元 化学反应速率与反应限度课后习题福建省福州市福清市虞阳中学2022-2023学年下学期高一年第一次月考化学试卷
解题方法
3 . Bodensteins研究了反应:
 ,在716 K时,气体混合物中碘化氢的物质的量分数
,在716 K时,气体混合物中碘化氢的物质的量分数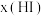 与反应时间t的关系如表所示:
与反应时间t的关系如表所示:
(1)根据上述实验结果,该反应的平衡常数K的计算式为_______ 。
(2)上述反应中,正反应速率 ,逆反应速率
,逆反应速率 ,其中
,其中 、
、 为正、逆反应速率常数,则
为正、逆反应速率常数,则 为
为_______ (用含K和 的代数式表示)。若起始时,
的代数式表示)。若起始时, ,
, ,则在
,则在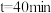 时,
时,
_______ 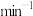 。
。

 ,在716 K时,气体混合物中碘化氢的物质的量分数
,在716 K时,气体混合物中碘化氢的物质的量分数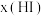 与反应时间t的关系如表所示:
与反应时间t的关系如表所示: | 0 | 20 | 40 | 60 | 80 | 120 |
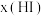 | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
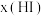 | 0 | 0.6 | 0.73 | 0.773 | 0.78 | 0.784 |
(2)上述反应中,正反应速率
 ,逆反应速率
,逆反应速率 ,其中
,其中 、
、 为正、逆反应速率常数,则
为正、逆反应速率常数,则 为
为 的代数式表示)。若起始时,
的代数式表示)。若起始时, ,
, ,则在
,则在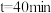 时,
时,
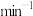 。
。
您最近一年使用:0次
2021-08-01更新
|
574次组卷
|
4卷引用:人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数及相关计算
人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时2 化学平衡常数及相关计算选择性必修1(SJ)专题2第二单元课时3 化学平衡常数平衡转化率(已下线)必考点03 化学平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)2.2.3化学平衡常数 课后
4 . 反应体系为气体、催化剂为固体的异相催化反应很普遍。设气体在均匀的固体催化剂表面发生单层吸附,各吸附活性中心能量相同,忽略吸附粒子间相互作用,吸附平衡常数不随压力变化。
(1)理想气体X在180 K和3.50 × 105Pa条件下,1 g固体的吸附量为1.242 cm3.在240 K达到相同的吸附量时,需要将压力增加到1.02MPa。估算X在该固体表面的摩尔吸附焓变________ (假设此温度范围内摩尔吸附焓变为定值)。
(2)已知反应A(g)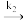 B(g)的反应机理为: A(g)+*
B(g)的反应机理为: A(g)+* 

 >B(g)+*,其中*表示固体催化剂表面的活性中心。每个活性中心只能吸附一个气态分 子A(g),形成吸附态分子
>B(g)+*,其中*表示固体催化剂表面的活性中心。每个活性中心只能吸附一个气态分 子A(g),形成吸附态分子 。
。 可直接转化生成气相产物B,该表面反应为决速步骤。吸附态
可直接转化生成气相产物B,该表面反应为决速步骤。吸附态 的浓度用表面覆盖度(
的浓度用表面覆盖度(  分子所占据的活性中心个数与表面活性中心总个数之比)表示。在298 K测量A(g)
分子所占据的活性中心个数与表面活性中心总个数之比)表示。在298 K测量A(g) 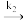 B(g)反应速率常数k2,高压下为5 kPa·s-1,低压下为0.1s-1.试计算气体A分压为50 kPa时,由A生成B的反应速率
B(g)反应速率常数k2,高压下为5 kPa·s-1,低压下为0.1s-1.试计算气体A分压为50 kPa时,由A生成B的反应速率________ 。
(3)假如产物B也发生表面吸附,反应机理变为:
A(g) + *



 B(g) + *
B(g) + *
其中由 生成
生成 的表面反应为决速步骤。假设ka,kd, k1都和问题(2)中的相同。当产物B的分压pB远大于pA时,A(g)
的表面反应为决速步骤。假设ka,kd, k1都和问题(2)中的相同。当产物B的分压pB远大于pA时,A(g) 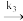 B(g)的反应对于A来说是一级反应,且速率常数k3可表达为pB的函数:K3=
B(g)的反应对于A来说是一级反应,且速率常数k3可表达为pB的函数:K3= kPa·s-1
kPa·s-1
求B(g)在催化剂上的吸附平衡常数KB = ka1/kg1________ 。
(1)理想气体X在180 K和3.50 × 105Pa条件下,1 g固体的吸附量为1.242 cm3.在240 K达到相同的吸附量时,需要将压力增加到1.02MPa。估算X在该固体表面的摩尔吸附焓变
(2)已知反应A(g)
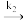 B(g)的反应机理为: A(g)+*
B(g)的反应机理为: A(g)+* 

 >B(g)+*,其中*表示固体催化剂表面的活性中心。每个活性中心只能吸附一个气态分 子A(g),形成吸附态分子
>B(g)+*,其中*表示固体催化剂表面的活性中心。每个活性中心只能吸附一个气态分 子A(g),形成吸附态分子 。
。 可直接转化生成气相产物B,该表面反应为决速步骤。吸附态
可直接转化生成气相产物B,该表面反应为决速步骤。吸附态 的浓度用表面覆盖度(
的浓度用表面覆盖度(  分子所占据的活性中心个数与表面活性中心总个数之比)表示。在298 K测量A(g)
分子所占据的活性中心个数与表面活性中心总个数之比)表示。在298 K测量A(g) 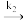 B(g)反应速率常数k2,高压下为5 kPa·s-1,低压下为0.1s-1.试计算气体A分压为50 kPa时,由A生成B的反应速率
B(g)反应速率常数k2,高压下为5 kPa·s-1,低压下为0.1s-1.试计算气体A分压为50 kPa时,由A生成B的反应速率(3)假如产物B也发生表面吸附,反应机理变为:
A(g) + *




 B(g) + *
B(g) + *其中由
 生成
生成 的表面反应为决速步骤。假设ka,kd, k1都和问题(2)中的相同。当产物B的分压pB远大于pA时,A(g)
的表面反应为决速步骤。假设ka,kd, k1都和问题(2)中的相同。当产物B的分压pB远大于pA时,A(g) 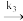 B(g)的反应对于A来说是一级反应,且速率常数k3可表达为pB的函数:K3=
B(g)的反应对于A来说是一级反应,且速率常数k3可表达为pB的函数:K3= kPa·s-1
kPa·s-1求B(g)在催化剂上的吸附平衡常数KB = ka1/kg1
您最近一年使用:0次
名校
解题方法
5 . 一定温度下,将3mol A气体和1mol B气体通入一密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)若容器体积固定为2L,反应2min时测得剩余0.6molB,C的浓度为0.4mol/L。请填写下列空白:
(1)2min内,A的平均反应速率为____ ;x=_____ ;
(2)若反应经4min达到平衡,平衡时C的浓度_____ 0.8mol/L(填“大于”、“等于”或“小于”);
(3)若达到平衡时C的体积分数为22%,则B的转化率为_____ 。(结果保留小数点后一位)
(1)2min内,A的平均反应速率为
(2)若反应经4min达到平衡,平衡时C的浓度
(3)若达到平衡时C的体积分数为22%,则B的转化率为
您最近一年使用:0次
名校
解题方法
6 . (1)反应3A(g)+B(g)=2C(g)在三种不同的条件下进行反应,一段时间后,测得的反应速率用不同的物质表示为:①vA=1mol/(L·min);②vC=0.5mol/(L·min);③vB=0.5mol/(L·min),则在三种不同条件下该反应速率由大到小的关系是___ (请用序号表示)。
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
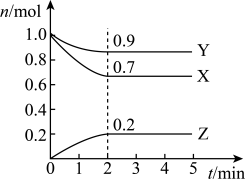
①该反应的化学方程式为___ 。
②反应开始至2min,以气体Z表示的平均反应速率为___ 。
③若2min后反应达平衡,与初始时刻相比,此时容器内混合气体的平均相对分子质量___ (填“增大”、“减小”或“不变”,下同),混合气体密度比起始时___ 。
④上述反应,在第2min时,X的转化率为___ 。
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
②反应开始至2min,以气体Z表示的平均反应速率为
③若2min后反应达平衡,与初始时刻相比,此时容器内混合气体的平均相对分子质量
④上述反应,在第2min时,X的转化率为
您最近一年使用:0次
2021-06-02更新
|
383次组卷
|
6卷引用:2015-2016学年河南省信阳市息三中高一下第二次月考化学试卷
7 . 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2 L的密闭容器中加入0.2 mol的N2和0.6 mol的H2在一定条件下发生反应:N2(g)+3H2(g) ⇌2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率v(N2)=_______ 。
(2)平衡后,若提高H2的转化率,可以采取的措施有_______ 。
A.加了催化剂 B.增大容器体积
C.降低反应体系的温度 D.加入一定量N2
(3)若在0.5 L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1_______ K2(填“<”“>”或“=”);
②400℃时,反应2NH3(g) ⇌N2(g)+3H2(g)的化学平衡常数为_______ 。当测得NH3、N2和H2物质的量分别为3 mol、2 mol和 1 mol时,则该反应的v(N2)正_______ v(N2)逆(填“<”“>”或“=”)。
(1)若在一容积为2 L的密闭容器中加入0.2 mol的N2和0.6 mol的H2在一定条件下发生反应:N2(g)+3H2(g) ⇌2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率v(N2)=
(2)平衡后,若提高H2的转化率,可以采取的措施有
A.加了催化剂 B.增大容器体积
C.降低反应体系的温度 D.加入一定量N2
(3)若在0.5 L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)⇌2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
| T/℃ | 200 | 300 | 400 |
| K | K1 | K3 | 0.5 |
请完成下列问题:
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g) ⇌N2(g)+3H2(g)的化学平衡常数为
您最近一年使用:0次
19-20高一下·浙江·阶段练习
解题方法
8 . 某温度时,在5 L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。

(1)由图中的数据分析,该反应的化学方程式为___________ 。
(2)反应开始至2min, Z的平均反应速率为___________ 。
(3)5min后达到平衡,则X的转化率是___________ 。

(1)由图中的数据分析,该反应的化学方程式为
(2)反应开始至2min, Z的平均反应速率为
(3)5min后达到平衡,则X的转化率是
您最近一年使用:0次
名校
9 . 在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)⇌3C(g)+nD(g),开始时A为4mol,B为6mol,5min末时测得C的物质的量为3mol,D的化学反应速率v(D)=0.2mol/(L·min)。请回答:
(1)5min末A的物质的量浓度为_______ ;
(2)前5min内用B表示的化学反应速率v(B)为_______ ;
(3)前5min内A的转化率为_______ ;(转化率是指某一反应物的转化百分率)
(4)化学方程式中n的值为_______ ;
(5)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol/(L·min) ②v(B)=6mol/(L·min)
③v(C)=4.5mol/(L·min) ④v(D)=8mol/(L·min)
其中反应速率最快的是_______ (填编号)。
(1)5min末A的物质的量浓度为
(2)前5min内用B表示的化学反应速率v(B)为
(3)前5min内A的转化率为
(4)化学方程式中n的值为
(5)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol/(L·min) ②v(B)=6mol/(L·min)
③v(C)=4.5mol/(L·min) ④v(D)=8mol/(L·min)
其中反应速率最快的是
您最近一年使用:0次
2021-04-17更新
|
869次组卷
|
5卷引用:湖南省长沙市明德中学2019-2020学年高一下学期第八次阶段性检测化学试题
湖南省长沙市明德中学2019-2020学年高一下学期第八次阶段性检测化学试题(已下线)【浙江新东方】双师208高一下吉林省白城市第一中学2020-2021学年高一下学期期中考试化学试题(已下线)第二章 第一节 化学反应速率(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)河北省唐山市第十一中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
10 . 某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应反应物是_____ ,生成物是_______ ,化学方程式为_______ 。
②反应开始至2min,以气体Z表示的平均反应速率为_______ 。

①该反应反应物是
②反应开始至2min,以气体Z表示的平均反应速率为
您最近一年使用:0次
2021-04-15更新
|
856次组卷
|
2卷引用:福建省莆田第十五中学2020-2021学年高一下学期期中考试化学试题



