1 . 对于可逆反应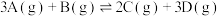 ,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是
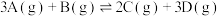 ,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最慢的是A. | B.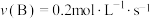 |
C. | D.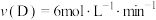 |
您最近一年使用:0次
名校
解题方法
2 . 某反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的化学反应速率为
| A.0.01mol/(L·s) | B.0.04mol/(L·s) | C.0.08mol/(L·s) | D.0.05mol/(L·s) |
您最近一年使用:0次
2024-04-05更新
|
457次组卷
|
2卷引用:甘肃省白银市会宁县第四中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
3 . 日常生活中常见的措施与化学反应速率也有密切的关系。下列措施中,其使用目的与速率无关的是
| A.夏天没有将牛奶放入冰箱中冷藏,易变质 | B.在月饼包装内放置抗氧化剂 |
| C.医疗上使用75%的酒精杀菌消毒 | D.用热水溶解食盐以加快溶解速率 |
您最近一年使用:0次
2024-02-19更新
|
200次组卷
|
2卷引用:湖北省武汉市新洲区第一中学2024届高二上学期期末联考化学试题
名校
4 . 下列说法不正确的是
| A.化学反应速率是用来表示一段时间内化学反应快慢的物理量 |
| B.化学反应速率通常用反应物或生成物物质的量浓度随时间的变化表示 |
| C.对于同一时间、同一个反应,化学反应速率用不同物质表示时数值不同 |
| D.用不同物质表示化学反应速率时,其数值之比等于方程式中计量数之比 |
您最近一年使用:0次
2023-12-29更新
|
491次组卷
|
2卷引用:上海市七宝中学2023-2024学年高二上学期12月测试化学试题
名校
解题方法
5 . 一定温度下,向2L恒容密闭容器中充入0.4molNH3和0.5molO2发生反应 。2min后,NO的浓度为0.06mol/L。下列说法正确的是
。2min后,NO的浓度为0.06mol/L。下列说法正确的是
 。2min后,NO的浓度为0.06mol/L。下列说法正确的是
。2min后,NO的浓度为0.06mol/L。下列说法正确的是A. 末,用 末,用 表示的反应速率为 表示的反应速率为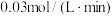 |
B. 末, 末, 的浓度为 的浓度为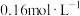 |
C. 内,生成的水的物质的量为 内,生成的水的物质的量为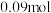 |
D. 内,反应物 内,反应物 的转化率为 的转化率为 |
您最近一年使用:0次
解题方法
6 . 一定条件下,将3 molA气体和1 mol B气体混合于固定容积为2L的密闭容器中,发生反应:3A(g)+B(g) 4C(g)+ 2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
4C(g)+ 2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
 4C(g)+ 2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是
4C(g)+ 2D(s)。2min末该反应达到平衡,生成D的物质的量随时间的变化情况如图所示。下列判断正确的是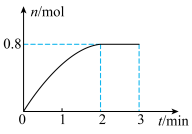
| A.若混合气体的平均摩尔质量不再改变时,该反应一定达到平衡状态 |
| B.平衡时的体系的压强与开始时体系的压强之比为3∶2 |
| C.反应过程中A和B的转化率之比为3∶1 |
| D.从开始到平衡,用D表示的化学反应速率为0.2 mol/(L·min) |
您最近一年使用:0次
2023-12-03更新
|
494次组卷
|
2卷引用:山东省菏泽市2023-2024学年高二上学期11月期中化学试题
7 . 治理汽车尾气中NO和CO污染的一种方法的反应原理为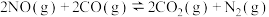 ,某一温度下,其化学平衡常数
,某一温度下,其化学平衡常数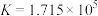 。下列说法正确的是
。下列说法正确的是
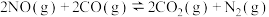 ,某一温度下,其化学平衡常数
,某一温度下,其化学平衡常数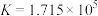 。下列说法正确的是
。下列说法正确的是| A.反应达到平衡时,CO、NO的转化率相等 |
B.化学平衡常数的表达式为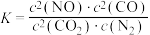 |
| C.此温度下,因K值较大,故化学反应速率较快 |
| D.加入催化剂,反应物的活化分子百分数增大,有效碰撞次数增多,反应速率增大 |
您最近一年使用:0次
8 . 短程硝化-厌氧氨氧化工艺的目的是将氨氮( )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:

资料:氧气浓度过高时, 会被氧化成
会被氧化成 。
。
(1)参与I中反应的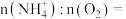
_____ 。
(2)Ⅱ中生成 的离子方程式为
的离子方程式为_____ 。
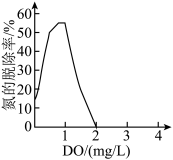
(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是_____ 。
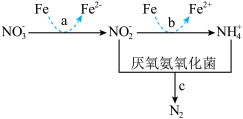
(4)经上述工艺处理后,排出的水中含有一定量的 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:_____ 。
 )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:
资料:氧气浓度过高时,
 会被氧化成
会被氧化成 。
。(1)参与I中反应的
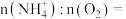
(2)Ⅱ中生成
 的离子方程式为
的离子方程式为(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是

(4)经上述工艺处理后,排出的水中含有一定量的
 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:
您最近一年使用:0次
名校
9 . 化学反应速率是指一定时间内任何一种反应物物质的量的减少或任何一种生成物物质的量的增加。(________)
您最近一年使用:0次
名校
解题方法
10 . 下列有关化学反应速率的说法中正确的是
| A.化学反应速率通常表示某一时刻的化学反应快慢 |
| B.化学反应速率是用来衡量化学反应进行快慢的尺度 |
| C.对任何化学反应来说,反应速率越大,反应现象就越明显 |
| D.温度和压强都是通过增大活化分子百分数来加快化学反应速率 |
您最近一年使用:0次
2023-10-12更新
|
178次组卷
|
2卷引用:甘肃省兰州第一中学2023-2024学年高二上学期10月月考化学试题



