名校
1 . 甲醇脱水可制备新型能源二甲醚 。某温度下,向密闭容器中加入甲醇发生反应,
。某温度下,向密闭容器中加入甲醇发生反应,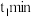 时测得各组分的浓度为
时测得各组分的浓度为 ,
,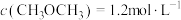 ,
,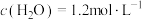 。已知该温度下的平衡常数
。已知该温度下的平衡常数 ,则
,则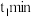 时
时
___________ 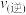 (填“>”、“<”或“=”),理由是:
(填“>”、“<”或“=”),理由是:___________ 。
 。某温度下,向密闭容器中加入甲醇发生反应,
。某温度下,向密闭容器中加入甲醇发生反应,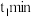 时测得各组分的浓度为
时测得各组分的浓度为 ,
,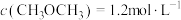 ,
,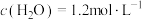 。已知该温度下的平衡常数
。已知该温度下的平衡常数 ,则
,则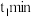 时
时
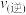 (填“>”、“<”或“=”),理由是:
(填“>”、“<”或“=”),理由是:
您最近一年使用:0次
名校
解题方法
2 . 某反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的化学反应速率为
| A.0.01mol/(L·s) | B.0.04mol/(L·s) | C.0.08mol/(L·s) | D.0.05mol/(L·s) |
您最近一年使用:0次
2024-04-05更新
|
495次组卷
|
2卷引用:甘肃省白银市会宁县第四中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
3 . 一定温度下,向2L恒容密闭容器中充入0.4molNH3和0.5molO2发生反应 。2min后,NO的浓度为0.06mol/L。下列说法正确的是
。2min后,NO的浓度为0.06mol/L。下列说法正确的是
 。2min后,NO的浓度为0.06mol/L。下列说法正确的是
。2min后,NO的浓度为0.06mol/L。下列说法正确的是A. 末,用 末,用 表示的反应速率为 表示的反应速率为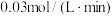 |
B. 末, 末, 的浓度为 的浓度为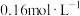 |
C. 内,生成的水的物质的量为 内,生成的水的物质的量为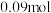 |
D. 内,反应物 内,反应物 的转化率为 的转化率为 |
您最近一年使用:0次
4 . 治理汽车尾气中NO和CO污染的一种方法的反应原理为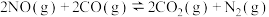 ,某一温度下,其化学平衡常数
,某一温度下,其化学平衡常数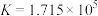 。下列说法正确的是
。下列说法正确的是
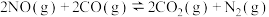 ,某一温度下,其化学平衡常数
,某一温度下,其化学平衡常数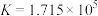 。下列说法正确的是
。下列说法正确的是| A.反应达到平衡时,CO、NO的转化率相等 |
B.化学平衡常数的表达式为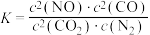 |
| C.此温度下,因K值较大,故化学反应速率较快 |
| D.加入催化剂,反应物的活化分子百分数增大,有效碰撞次数增多,反应速率增大 |
您最近一年使用:0次
5 . 短程硝化-厌氧氨氧化工艺的目的是将氨氮( )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:

资料:氧气浓度过高时, 会被氧化成
会被氧化成 。
。
(1)参与I中反应的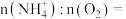
_____ 。
(2)Ⅱ中生成 的离子方程式为
的离子方程式为_____ 。
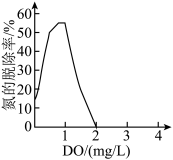
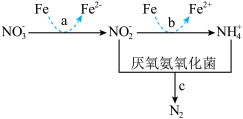
(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是_____ 。
(4)经上述工艺处理后,排出的水中含有一定量的 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:_____ 。
 )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:
资料:氧气浓度过高时,
 会被氧化成
会被氧化成 。
。(1)参与I中反应的
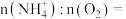
(2)Ⅱ中生成
 的离子方程式为
的离子方程式为(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是

(4)经上述工艺处理后,排出的水中含有一定量的
 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:
您最近一年使用:0次
名校
解题方法
6 . 下列有关化学反应速率的说法中正确的是
| A.化学反应速率通常表示某一时刻的化学反应快慢 |
| B.化学反应速率是用来衡量化学反应进行快慢的尺度 |
| C.对任何化学反应来说,反应速率越大,反应现象就越明显 |
| D.温度和压强都是通过增大活化分子百分数来加快化学反应速率 |
您最近一年使用:0次
2023-10-12更新
|
185次组卷
|
2卷引用:甘肃省兰州第一中学2023-2024学年高二上学期10月月考化学试题
7 . 下列有说法正确的是
| A.对反应A→B,1min内消耗4molA的反应速率一定比1min内消耗2molA的反应速率快 |
| B.糕点包装袋内放置抗氧化剂是为了减缓食物氧化速率 |
C.实验室用盐酸跟锌片反应制 ,用粗锌比纯锌速率快,主要目的是为了增大锌片和盐酸的接触面积从而加快反应速率 ,用粗锌比纯锌速率快,主要目的是为了增大锌片和盐酸的接触面积从而加快反应速率 |
| D.水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 |
您最近一年使用:0次
名校
解题方法
8 . 反应4NH3(气)+5O2(气)⇌4NO(气)+6H2O(气)在2L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.9mol,则此反应的平均速率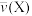 (反应物的消耗速率或产物的生成速率)可表示为
(反应物的消耗速率或产物的生成速率)可表示为
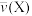 (反应物的消耗速率或产物的生成速率)可表示为
(反应物的消耗速率或产物的生成速率)可表示为A.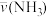 =0.10mol·L-1·s-1 =0.10mol·L-1·s-1 | B.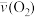 =0.010mol·L-1·s-1 =0.010mol·L-1·s-1 |
C.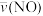 =0.010mol·L-1·s-1 =0.010mol·L-1·s-1 | D.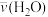 =0.45mol·L-1·s-1 =0.45mol·L-1·s-1 |
您最近一年使用:0次
2022-12-22更新
|
362次组卷
|
2卷引用:福建省泉州市第六中学2021-2022学年高二上学期期中模块测试化学试题
名校
9 . I.实验室利用下列方案探究影响化学反应速率的因素。请回答相关问题:
(1)实验时,分别量取 溶液(过量)和酸性
溶液(过量)和酸性 溶液,迅速混合并开始计时,可以通过测定
溶液,迅速混合并开始计时,可以通过测定_______ 来判断反应的快慢。
(2)实验①和实验②是探究_______ 对化学反应速生的影响,实验②和③是探究_______ 对化学反应速率的影响。
II.恒容密闭容器中,用 还原
还原 ,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示,请分析并回答如下问题:
,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示,请分析并回答如下问题:
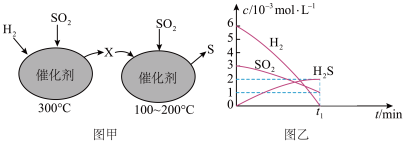
(3)写出300℃发生的化学反应方程式_______ 。其中一种产物X进入下一容器,在100~200℃与 反应,则X为(填化学式)
反应,则X为(填化学式)_______ 。
(4)0~ 时间段用
时间段用 表示的化学反应速率为
表示的化学反应速率为_______ 。
| 编号 | 温度/℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度 | 体积/mL | 浓度 | 体积/mL | ||
| ① | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| ② | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| ③ | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
 溶液(过量)和酸性
溶液(过量)和酸性 溶液,迅速混合并开始计时,可以通过测定
溶液,迅速混合并开始计时,可以通过测定(2)实验①和实验②是探究
II.恒容密闭容器中,用
 还原
还原 ,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示,请分析并回答如下问题:
,生成S的反应分两步完成(如图甲所示),在300℃反应时相关物质的物质的量浓度随时间的变化关系如图乙所示,请分析并回答如下问题:
(3)写出300℃发生的化学反应方程式
 反应,则X为(填化学式)
反应,则X为(填化学式)(4)0~
 时间段用
时间段用 表示的化学反应速率为
表示的化学反应速率为
您最近一年使用:0次
2022-12-11更新
|
264次组卷
|
2卷引用:福建省泉州第五中学2022-2023学年高二上学期期中考化学试题
名校
10 . 已知反应N2(g)+3H2(g) 2NH3(g)在四种不同情况下的反应速率分别如下:
2NH3(g)在四种不同情况下的反应速率分别如下:
①v(N2)=6.0mol•L-1•min-1
②v(H2)=0.45mol•L-1•s-1
③v(H2)=0.3mol•L-1•s-1
④v(NH3)=0.15mol•L-1•s-1
则该反应进行速率快慢顺序正确的是
 2NH3(g)在四种不同情况下的反应速率分别如下:
2NH3(g)在四种不同情况下的反应速率分别如下:①v(N2)=6.0mol•L-1•min-1
②v(H2)=0.45mol•L-1•s-1
③v(H2)=0.3mol•L-1•s-1
④v(NH3)=0.15mol•L-1•s-1
则该反应进行速率快慢顺序正确的是
| A.①>②>③>④ | B.②>①=③>④ | C.③>①>②>④ | D.④>③>①>② |
您最近一年使用:0次
2022-11-18更新
|
683次组卷
|
2卷引用:辽宁省六校协作体2022-2023学年高二上学期期中考试化学试题



