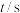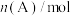解题方法
1 . 一定温度下,向2L恒容容器中充入1.0molA和1.0molB,发生反应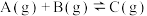 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
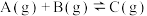 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是
| 0 | 5 | 15 | 25 | 35 |
| 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.前5s的平均反应速率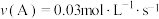 |
| B.反应进行到25s时,反应刚好达到平衡状态 |
C.温度不变,起始向容器中充入0.4molA、0.4molB和0.1molC,达平衡前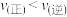 |
| D.保持温度不变,起始时向容器中充入2.0molC,达平衡时,C的转化率大于80% |
您最近一年使用:0次
2022-11-16更新
|
355次组卷
|
4卷引用:专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)河北省邢台市五校联考2022-2023学年高三上学期期中考试化学试题河北省邢台市五校2022-2023学年高三上学期第二次联考化学试题第二章 章末训练
10-11高一下·吉林·开学考试
名校
解题方法
2 . 在不同条件下,分别测得反应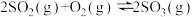 的化学反应速率,其中表示该反应进行得最快的是
的化学反应速率,其中表示该反应进行得最快的是
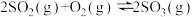 的化学反应速率,其中表示该反应进行得最快的是
的化学反应速率,其中表示该反应进行得最快的是A. | B.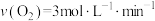 |
C.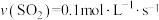 | D.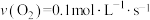 |
您最近一年使用:0次
2022-11-15更新
|
491次组卷
|
43卷引用:第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)
(已下线)第26练 化学反应速率-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2.3.1 化学反应速率的概念和测定-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修1)(已下线)2010—2011学年吉林省油田高中高一下学期期初考试化学试卷(已下线)2010—2011学年湖北省长阳一中高一下学期期中考试化学试卷(已下线)2011-2012年安徽芜湖一中高二下学期期中考试理科化学试卷(已下线)2012-2013学年安徽省宿松县复兴中学高二第二次月考化学试卷(已下线)2012-2013学年江西省白鹭洲中学高一下学期期中考试化学试卷(已下线)2012-2013学年云南省大理州宾川县第四高级中学高二4月月考化学卷2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷2015-2016学年四川省雅安市高二上学期期末考试化学试卷2016-2017学年吉林省汪清六中高二上第一次月考化学试卷2016-2017学年河南省新乡市延津县中学高二上第一次月考化学卷陕西省西安中学2016-2017学年高二(平行班)上学期期末考试化学试题2016-2017学年江苏省沭阳县高二下学期期中调研测试化学试卷山东省微山县第二中学2018-2019学年高二上学期第三学段教学质量监测化学试题陕西省白水中学2018-2019学年高二上学期第二次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二上学期期末考试化学试题云南省玉溪一中2018-2019学年高二上学期期末考试化学试题河北省唐山市第十一中学2018-2019学年高一下学期期中考试化学试题【校级联考】江苏省常州“教学研究合作联盟”2018-2019学年高二下学期期中考试化学试题青海省海东市第二中学2018-2019学年高二下学期第一次月考化学试题新疆乌鲁木齐市二十三中学2018-2019学年高二10月月考化学试题贵州省岑巩县第四中学2019-2020学年高二上学期期末考试化学试题内蒙古包钢第一中学2019-2020学年高二上学期10月月考化学试题陕西省宝鸡市金台区2019-2020学年高二上学期期中检测化学试题甘肃省靖远县第四中学2019-2020学年高一下学期期中考试化学(普通班)试题辽宁省铁岭市调兵山市第二高级中学2019—2020学年高一下学期线上教学测试化学试题新疆吐蕃市高昌区第二中学2020-2021学年高二10月月考化学试题西藏自治区拉萨市第二高级中学2019-2020学年高二上学期期末考试化学试题西藏自治区日喀则市第二高级中学2020-2021学年高二上学期期中考试化学试题西藏日喀则市上海实验学校2020-2021学年高二上学期期中考试化学试题云南省丽江市玉龙纳西族自治县田家炳民族中学2020-2021学年高二下学期第一次月考化学试题山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期第一次月考化学试题 陕西省咸阳市武功县2021--2022学年高二上学期质量调研化学试题上海市市北中学2022-2023学年高二上学期期中考试(等级)化学试题山西省太原市第五十六中学2022-2023学年高二上学期10月联考化学试题上海市致远高级中学2022-2023学年高二上学期期末教学评估化学等级考试题(已下线)专题03 化学反应速率与化学平衡(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)(已下线)期末模拟题(一)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)作业(四) 化学反应速率陕西省洛南中学2022-2023学年高二上学期10月月考化学试题第二章 化学反应速率与化学平衡 第一节 化学反应速率 第1课时 化学反应速率
2022高三·全国·专题练习
名校
解题方法
3 . 室温下,某溶液初始时仅溶有P和Q且浓度相等,同时发生以下两个反应:①P+Q=X+Z;②P+Q=Y+Z,反应①的速率可表示为v1=k1c2(P)(k1、k2为速率常数)。反应体系中组分Q、X的浓度随时间变化情况如图所示(溶液体积变化忽略不计,Y、Z均可溶于水)。下列说法不正确 的是
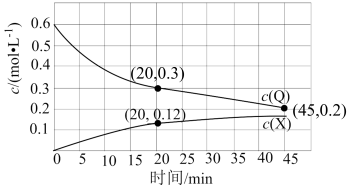

| A.反应①的活化能比反应②的活化能大 |
| B.0~20min内,Z的平均反应速率为6×10-3mol•L-1•min-1 |
| C.反应30min时,v1:v2=2:3 |
| D.45min时Y的浓度为0.24mol•L-1 |
您最近一年使用:0次
2022-11-09更新
|
609次组卷
|
7卷引用:解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)热点情景汇编-专题七 化学反应速率与平衡(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(11-16)山东省肥城市2022届高考适应性训练(二)化学试题广东省广州市第六中学2022届高三第三次模拟考试化学试题河北省邢台市五校联考2022-2023学年高三上学期期中考试化学试题河北省邢台市五校2022-2023学年高三上学期第二次联考化学试题
2022高三·全国·专题练习
解题方法
4 . 在一个体积固定的密闭容器中,进行的可逆反应A(s)+3B(g)  3C (g)。下列叙述中表明可逆反应一定达到平衡状态的是
3C (g)。下列叙述中表明可逆反应一定达到平衡状态的是
①C的生成速率与C的分解速率相等;②单位时间内生成a mol A,同时生成3a mol B;③B的浓度不再变化;④混合气体总的物质的量不再发生变化;⑤A、B、C的物质的量之比为1∶3∶3;⑥混合气体的密度不再变化。
 3C (g)。下列叙述中表明可逆反应一定达到平衡状态的是
3C (g)。下列叙述中表明可逆反应一定达到平衡状态的是①C的生成速率与C的分解速率相等;②单位时间内生成a mol A,同时生成3a mol B;③B的浓度不再变化;④混合气体总的物质的量不再发生变化;⑤A、B、C的物质的量之比为1∶3∶3;⑥混合气体的密度不再变化。
| A.①②③ | B.①③④⑥ | C.①③⑥ | D.①③④ |
您最近一年使用:0次
11-12高二·山西太原·阶段练习
名校
5 . 把3mol P和2.5mol Q置于2L密闭容器中,发生如下反应:3P(g)+Q(g) xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是
xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是
 xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是
xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是| A.Q的转化率为25% |
| B.5min内P的平均反应速率为0.15mol/(L·min) |
| C.Q的平衡浓度为1mol/L |
| D.x是2 |
您最近一年使用:0次
2022-10-26更新
|
104次组卷
|
26卷引用:夯基提能2020届高三化学选择题对题专练——选修四化学反应原理——化学反应速率及其影响因素专练
夯基提能2020届高三化学选择题对题专练——选修四化学反应原理——化学反应速率及其影响因素专练(已下线)2012-2013学年山西省太原五中高二8月月考化学试卷(已下线)2012-2013学年江西省南昌市第二中学高二第一次月考化学试卷(已下线)2014-2015学年河南省洛阳市第八中学高二10月月考化学试卷2015-2016学年河南省洛阳市伊川实验高中高二上第二次月考化学试卷2015-2016学年安徽省安庆市怀宁高河中学高二上第一次月考化学试卷2015-2016学年河北省保定三中高一下4月月考化学试卷2016-2017学年山西省大同一中高二上10月月考化学卷2016-2017学年江西省九江一中高二上期中化学试卷江西省南昌市第二中学2017-2018学年高二上学期第一次月考化学试题江西省赣州市崇义中学2017-2018学年高二上学期第一次月考化学试题四川省射洪县射洪中学2018-2019学年高二上学期开学考试化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高二上学期10月月考化学试题江苏省泰州市第二中学2017-2018学年高二上学期期中考试化学试题(已下线)【南昌新东方】江西省九江第一中学2016-2017学年高二上学期期中考试化学试题江西省赣州市赣县区第三中学2020-2021学年高二(实验重点班)9月月考化学试题安徽省滁州市定远县重点中学2020-2021学年高二10月月考化学试题甘肃省庆阳市第六中学2020-2021学年高二上学期期中考试化学(理)试题湖北随州市第一中学2020-2021学年高二上学期期中考试化学试题新疆乌鲁木齐市第七十中学2021-2022学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高一下学期期末考试化学试题重庆市铜梁区2021-2022学年高一下学期期末考试化学试题甘肃省庆阳市宁县第二中学2022-2023学年高二上学期第一次月考化学试题江西省丰城市第九中学2022-2023学年高二上学期入学质量检测化学试题湖南省株洲市炎陵县2023-2024学年高二上学期入学考试化学试题
2022高三·全国·专题练习
解题方法
6 . 减弱温室效应的方法之一是将CO2回收利用,科学家研究利用回收的CO2制取甲醛,反应的热化学方程式为CO2(g)+2H2(g HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
已知:v(B)=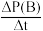 ,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为_____ kPa•min-1。
 HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
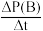 ,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
您最近一年使用:0次
2022高三·全国·专题练习
解题方法
7 . 工业上利用正丁烷的裂解反应制备乙烯、丙烯等化工基础原料,相关反应如下:
反应i:CH3CH2CH2CH3(g) CH4(g)+CH3CH=CH2(g) △H1=+80kJ•mol-1
CH4(g)+CH3CH=CH2(g) △H1=+80kJ•mol-1
反应ii:CH3CH2CH2CH3(g) CH3CH3 (g)+CH2=CH2(g) △H2=+92kJ•mol-1
CH3CH3 (g)+CH2=CH2(g) △H2=+92kJ•mol-1
请回答下列问题:
T℃下,在某催化剂作用下向2L恒容密闭容器中充入2mol正丁烷,发生上述反应i和反应ii,经10min反应达到平衡状态,此时的压强是起始时压强的1.8倍,计算反应在0~10min内的平均反应速率v(正丁烷)=______ mol•L-1•min-1。
反应i:CH3CH2CH2CH3(g)
 CH4(g)+CH3CH=CH2(g) △H1=+80kJ•mol-1
CH4(g)+CH3CH=CH2(g) △H1=+80kJ•mol-1反应ii:CH3CH2CH2CH3(g)
 CH3CH3 (g)+CH2=CH2(g) △H2=+92kJ•mol-1
CH3CH3 (g)+CH2=CH2(g) △H2=+92kJ•mol-1请回答下列问题:
T℃下,在某催化剂作用下向2L恒容密闭容器中充入2mol正丁烷,发生上述反应i和反应ii,经10min反应达到平衡状态,此时的压强是起始时压强的1.8倍,计算反应在0~10min内的平均反应速率v(正丁烷)=
您最近一年使用:0次
2020·浙江·模拟预测
8 . 一定温度下,在2 L的恒容密闭容器中发生反应:A(g)+2B(g) 3C(g)反应过程中的部分数据如下表所示:
3C(g)反应过程中的部分数据如下表所示:
下列说法正确的是
 3C(g)反应过程中的部分数据如下表所示:
3C(g)反应过程中的部分数据如下表所示:| 时间(t/min) | 物质的量(n/mol) | ||
| n(A) | n(B) | n(C) | |
| 0 | 2.0 | 2.4 | 0 |
| 5 | 0.9 | ||
| 10 | 1.6 | ||
| 15 | 1.6 | ||
| A.0~5 min用A表示的平均反应速率为0. 09 mol·L-1·min-1 |
| B.该反应在10 min后才达到平衡 |
| C.平衡状态时,c(C)=0.6 mol·L-1 |
| D.物质B的平衡转化率为20% |
您最近一年使用:0次
2022-09-13更新
|
2796次组卷
|
36卷引用:解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练
(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题12.化学反应速率与化学平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)热点情景汇编-专题七 化学反应速率与平衡(已下线)题型24 单反应体系中的化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)浙江省2020年1月选考(学考)化学试题2020年浙江省高考化学试卷(1月选考)浙江省丽水市松阳县第二中学2019-2020学年高二4月线上教学检测化学试题浙江省东阳中学2019-2020学年高一下学期期中考试化学试题四川省射洪中学校2019-2020学年高一下学期期中考试化学试题河南省洛阳市2019-2020学年高一下学期期末考试化学试题河南省豫南九校2020-2021学年高二上学期第二次联考化学试题山东省滨州渤海中学2020-2021学年高二上学期10月月考化学试题青海省海西蒙古族藏族自治州德令哈市海西州高级中学2020-2021学年高二上学期期中考试化学试题高中化学苏教2019版必修第二册-专题6 第一单元综合拔高练人教版2019必修第二册 第六章 第二节综合拔高练浙江省杭州市长征中学2020-2021学年高二下学期第二学期阶段性练习化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一5月月考化学试题选择性必修1(SJ)专题2第二单元课时3 化学平衡常数平衡转化率甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(B班)化学试题甘肃省张掖市第二中学2021-2022学年高二上学期10月月考(A班)化学试题浙江省宁波市六校2020-2021学年高二上学期期中联考化学试题浙江省吴兴高级中学高二 2021-2022学年上学期10月月考化学试题广东省大联考2021-2022学年高一下学期期中检测化学试题广东省汕头市2021-2022学年高一下学期期末教学质量检测化学试题浙江省湖州中学2021-2022学年高一下学期第一次质量检测化学试题山东省济宁市泗水县2021-2022学年高二上学期期中考试化学试题湖北省黄州中学2022--2023学年高二上学期10月月考化学试题广东省广州市天河区第八十九中学2022~2023学年高一下学期期中考试化学选考试题2.2.3化学平衡常数 课后广西河池市八校联考2022-2023学年高一下学期4月月考化学试题黑龙江省鹤岗市第一中学2022-2023学年高一下学期期末考试化学试题
2022高三·全国·专题练习
解题方法
9 . 通过计算机分析,我们可从势能图(峰值数据是峰谷和峰值物质能量的差值)认识 加氢制甲醇在不同催化条件下存在的两种反应路径,如图1所示。
加氢制甲醇在不同催化条件下存在的两种反应路径,如图1所示。

(1)①写出甲酸盐路径决速步的化学方程式___________ 。
②下列说法正确的有___________ 。
A.增大催化剂表面积可提高 在催化剂表面的吸附速率
在催化剂表面的吸附速率
B.不考虑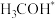 ,两种路径中产生的含碳中间体种类均有5种
,两种路径中产生的含碳中间体种类均有5种
C.中间体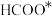 比
比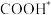 更稳定
更稳定
D.使用高活性催化剂可降低反应焓变,加快反应速率
(2)向恒压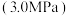 密闭装置中通入反应物混合气[混合比例
密闭装置中通入反应物混合气[混合比例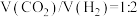 ],测定甲醇的平均生成速率随温度的变化曲线,如图2所示。
],测定甲醇的平均生成速率随温度的变化曲线,如图2所示。
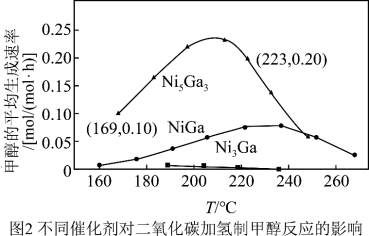
①甲醇的平均生成速率呈“抛物线”形状的原因___________ ,最佳催化剂及最佳反应温度是___________ 。
②二氧化碳加氢制甲醇的速率方程可表示为: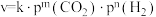 ,其中k为速率常数,各物质起始分压的指数为各物质的反应级数。实验结果表明,速率常数与反应级数均受反应温度的影响。使用
,其中k为速率常数,各物质起始分压的指数为各物质的反应级数。实验结果表明,速率常数与反应级数均受反应温度的影响。使用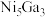 催化剂时,反应温度由
催化剂时,反应温度由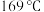 升高到
升高到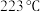 ,若
,若 反应级数
反应级数 ,
, 反应级数不变,则速率常数之比
反应级数不变,则速率常数之比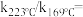
___________ 。
(3)在 催化加氢制甲醇过程中也存在竞争性的反应:
催化加氢制甲醇过程中也存在竞争性的反应:
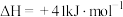 。在恒温密闭容器中,维持压强和投料不变,将
。在恒温密闭容器中,维持压强和投料不变,将 和
和 按一定流速通过反应器,二氧化碳转化率和甲醇选择性
按一定流速通过反应器,二氧化碳转化率和甲醇选择性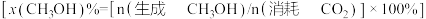 随温度变化关系如图3所示。
随温度变化关系如图3所示。
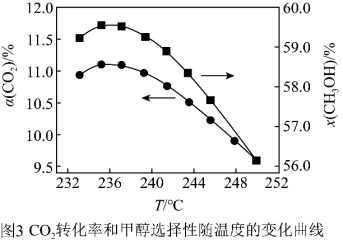
①若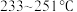 时催化剂活性受温度影响不大,则
时催化剂活性受温度影响不大,则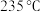 后图中曲线下降的原因
后图中曲线下降的原因___________ 。
②某温度时,向压强为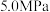 的恒压装置中加入
的恒压装置中加入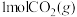 和
和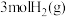 反应并达到平衡状态,
反应并达到平衡状态, 平衡转化率为
平衡转化率为 ,甲醇选择性为
,甲醇选择性为 ,则甲醇的平衡分压为
,则甲醇的平衡分压为___________ (结果保留2位有效数字) 。
 加氢制甲醇在不同催化条件下存在的两种反应路径,如图1所示。
加氢制甲醇在不同催化条件下存在的两种反应路径,如图1所示。
(1)①写出甲酸盐路径决速步的化学方程式
②下列说法正确的有
A.增大催化剂表面积可提高
 在催化剂表面的吸附速率
在催化剂表面的吸附速率B.不考虑
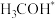 ,两种路径中产生的含碳中间体种类均有5种
,两种路径中产生的含碳中间体种类均有5种C.中间体
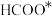 比
比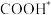 更稳定
更稳定D.使用高活性催化剂可降低反应焓变,加快反应速率
(2)向恒压
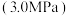 密闭装置中通入反应物混合气[混合比例
密闭装置中通入反应物混合气[混合比例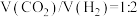 ],测定甲醇的平均生成速率随温度的变化曲线,如图2所示。
],测定甲醇的平均生成速率随温度的变化曲线,如图2所示。
①甲醇的平均生成速率呈“抛物线”形状的原因
②二氧化碳加氢制甲醇的速率方程可表示为:
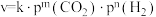 ,其中k为速率常数,各物质起始分压的指数为各物质的反应级数。实验结果表明,速率常数与反应级数均受反应温度的影响。使用
,其中k为速率常数,各物质起始分压的指数为各物质的反应级数。实验结果表明,速率常数与反应级数均受反应温度的影响。使用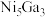 催化剂时,反应温度由
催化剂时,反应温度由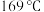 升高到
升高到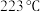 ,若
,若 反应级数
反应级数 ,
, 反应级数不变,则速率常数之比
反应级数不变,则速率常数之比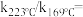
(3)在
 催化加氢制甲醇过程中也存在竞争性的反应:
催化加氢制甲醇过程中也存在竞争性的反应:
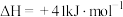 。在恒温密闭容器中,维持压强和投料不变,将
。在恒温密闭容器中,维持压强和投料不变,将 和
和 按一定流速通过反应器,二氧化碳转化率和甲醇选择性
按一定流速通过反应器,二氧化碳转化率和甲醇选择性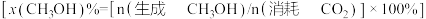 随温度变化关系如图3所示。
随温度变化关系如图3所示。
①若
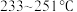 时催化剂活性受温度影响不大,则
时催化剂活性受温度影响不大,则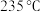 后图中曲线下降的原因
后图中曲线下降的原因②某温度时,向压强为
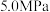 的恒压装置中加入
的恒压装置中加入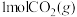 和
和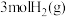 反应并达到平衡状态,
反应并达到平衡状态, 平衡转化率为
平衡转化率为 ,甲醇选择性为
,甲醇选择性为 ,则甲醇的平衡分压为
,则甲醇的平衡分压为
您最近一年使用:0次
名校
10 . A与B在容积为1L的密闭容器中发生反应:aA(g)+bB(g) cC(g)+dD(g),t1、t2时刻分别测得部分数据如下表;
cC(g)+dD(g),t1、t2时刻分别测得部分数据如下表;
下列说法正确的是
 cC(g)+dD(g),t1、t2时刻分别测得部分数据如下表;
cC(g)+dD(g),t1、t2时刻分别测得部分数据如下表;| n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min |
| 0.12 | 0.06 | 0.10 | t1 |
| 0.06 | 0.12 | 0.20 | t2 |
A.0~t1内,平均反应速率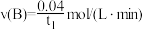 |
B.若起始时,n(D)=0,则t2时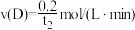 |
C.升高温度时,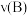 、 、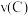 、 、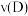 均增大 均增大 |
| D.b:d=5:3 |
您最近一年使用:0次