名校
1 . 下图是用钌 (Ru )基催化剂催化CO2(g)和H2(g)的反应的示意图,当反应生成46g液态HCOOH时放出31.2 kJ的热量。下列说法正确的是
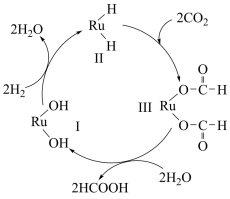
| A.图示中物质I、II、III均为该反应的催化剂 |
| B.使用催化剂可以降低反应的活化能,从而改变反应的焓变 |
| C.由题意知:HCOOH(l)=CO2(g)+H2(g) ΔH = +31.2kJ· mol-1 |
| D.因使用钌基催化剂使反应CO2(g) + H2(g)= HCOOH(l)分两步进行 |
您最近一年使用:0次
2022-09-06更新
|
491次组卷
|
7卷引用:宁夏吴忠中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
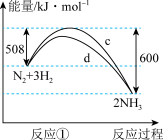
2 . I.氮及其化合物的转化过程如下图所示,其中下图为反应①过程中能量变化的曲线图。
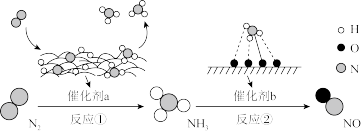
(1)下图中曲线_______ (填字母)是加入催化剂a时的能量变化曲线,该反应破坏生成物全部化学键所需要的总能量_______ (填“大于”或“小于”或“等于”)破坏反应物全部化学键所需要的总能量。
(2)标准状况下进行反应②,若有1.25mol电子发生转移,则参加反应的NH3的体积为_____ 。
(3)下列说法正确的是_______。
II.某同学为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(4)求2~4分钟时间段以盐酸的浓度变化来表示的该反应速率_______ 。(设溶液体积不变)
(5)有同学认为在盐酸溶液中滴入少量的CuSO4溶液可以加快反应的速率,请从电化学的角度给予分析:构成的原电池中负极反应式为_______ ;溶液中H+移向_______ 极(填“正“或“负")。
III.某温度下在4L恒容密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如图。
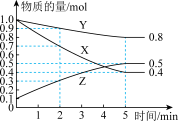
(6)写出该反应的化学方程式_______ 。
(7)在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是_______。
(8)该反应达平衡时,X的转化率为_______ 。

(1)下图中曲线

(2)标准状况下进行反应②,若有1.25mol电子发生转移,则参加反应的NH3的体积为
(3)下列说法正确的是_______。
| A.合成氨在工业生产中常将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.工业合成氨中,为加快化学反应速率,压强和温度越高越好 |
| C.合成氨工业要用合适的催化剂,目的是降低该反应的活化能 |
| D.工业合成氨中反应物不能百分之百转化为生成物 |
II.某同学为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 190 | 414 | 526 | 570 |
(5)有同学认为在盐酸溶液中滴入少量的CuSO4溶液可以加快反应的速率,请从电化学的角度给予分析:构成的原电池中负极反应式为
III.某温度下在4L恒容密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如图。

(6)写出该反应的化学方程式
(7)在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是_______。
| A.X、Y、Z的浓度相等 | B.容器内气体压强保持不变 |
| C.X、Y的反应速率比为3∶1 | D.生成1molY的同时生成2molZ |
您最近一年使用:0次
名校
解题方法
3 . 能够加快少量铁粉与200mL0.5mol/L 溶液反应速率且不改变生成氢气的量的组合是
溶液反应速率且不改变生成氢气的量的组合是
①用同质量的铁块代替铁粉;②加入硫酸钠固体;③加入硝酸钠固体;④加入醋酸钠固体;⑤加入少量锌粒;⑥通入HCl气体;⑦加热;⑧再加入100mL0.5mol/L 溶液
溶液
 溶液反应速率且不改变生成氢气的量的组合是
溶液反应速率且不改变生成氢气的量的组合是①用同质量的铁块代替铁粉;②加入硫酸钠固体;③加入硝酸钠固体;④加入醋酸钠固体;⑤加入少量锌粒;⑥通入HCl气体;⑦加热;⑧再加入100mL0.5mol/L
 溶液
溶液| A.①②⑤⑥⑦⑧ | B.②③⑤⑦ | C.⑤⑥⑦ | D.⑥⑦ |
您最近一年使用:0次
2022-08-25更新
|
543次组卷
|
2卷引用:宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
4 . 下列措施对增大反应速率明显有效的是
| A.Na与水反应时增大水的用量 |
| B.在K2SO4与BaCl2两溶液反应时,增大压强 |
| C.Fe与稀硫酸反应制取氢气时,改用浓硫酸 |
| D.将铝片改为铝粉,做铝与氧气反应的实验 |
您最近一年使用:0次
23-24高一上·全国·假期作业
名校
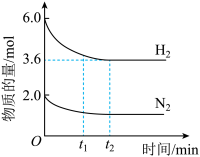
5 . 在2.0 L恒温恒容密闭容器中充入2.0 mol N2和6.0 mol H2,加入催化剂发生反应:N2(g)+3H2(g) 2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
 2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
| A.t1 min时,N2的生成速率等于N2的消耗速率 |
| B.使用催化剂可以缩短到达平衡时所需的时间 |
C.0~t2 min内,v(NH3)= mol·L−1·min−1 mol·L−1·min−1 |
| D.反应中通入足量的N2,可使H2完全转化为NH3 |
您最近一年使用:0次
2022-08-25更新
|
307次组卷
|
4卷引用:宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题
宁夏石嘴山第三中学2021-2022学年高一下学期期末考试化学试题江苏省盐城市田家炳中学2021-2022学年高一下学期期中考试化学试题(已下线)第10讲 化学反应限度(讲义)-【寒假自学课】2023年高一化学寒假精品课(人教版2019必修第二册)江西省萍乡市2022-2023学年高一下学期7月期末考试化学试题
2012·山西·一模
名校
解题方法
6 . 对可逆反应:A(g) + B(s) ⇌ 2C(s) + D(g) ΔH>0,如图所示为正、逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:①加入A;②加入催化剂;③加压;④升温;⑤减少C,符合图示条件的是
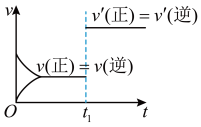

| A.②③ | B.①② | C.③④ | D.④⑤ |
您最近一年使用:0次
2022-08-19更新
|
366次组卷
|
13卷引用:宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题
宁夏石嘴山市平罗中学2021-2022学年高二下学期第一次月考化学试题2014-2015学年宁夏回族自治区银川一中高二上学期期中化学试卷甘肃省玉门市2021-2022学年高二上学期 “研课标读教材”期中学业质量监测化学试题甘肃省玉门市2021-2022学年高二下学期 “研课标读教材”期中学业质量监测试化学试题(一)黑龙江省牡丹江市第三高级中学2022-2023学年高二上学期第一次月考化学试题陕西省咸阳市武功县2022-2023学年高二上学期期中考试化学试题(已下线)2013届山西省高新二中高考一轮复习阶段考试化学试卷(已下线)2012-2013学年广西南宁九中高二上学期段考理科化学试卷内蒙古集宁市第一中学2016-2017学年高一下学期期末考试化学试题(已下线)考点11 化学反应速率——备战2019年浙江新高考化学考点新疆自治区生产建设兵团第一师高级中学2018-2019学年高二上学期第二次月考化学试题河北省尚义县第一中学2020-2021学年高二上学期期中考试化学试题四川省广安代市中学校2021-2022学年高二上学期第一次月考化学试题
12-13高一下·四川广安·期末
名校
解题方法
7 . 向四个体积相同的密闭容器中分别充入一定量的 和
和 ,开始反应时,按正反应速率由大到小的顺序排列,正确的是
,开始反应时,按正反应速率由大到小的顺序排列,正确的是
①500℃,10mol 和5mol
和5mol 反应
反应
②500℃,用 作催化剂,10mol
作催化剂,10mol 和5mol
和5mol 反应
反应
③450℃,8mol 和5mol
和5mol 反应
反应
④500℃,8mol 和5mol
和5mol 反应
反应
 和
和 ,开始反应时,按正反应速率由大到小的顺序排列,正确的是
,开始反应时,按正反应速率由大到小的顺序排列,正确的是 ①500℃,10mol
 和5mol
和5mol 反应
反应②500℃,用
 作催化剂,10mol
作催化剂,10mol 和5mol
和5mol 反应
反应③450℃,8mol
 和5mol
和5mol 反应
反应④500℃,8mol
 和5mol
和5mol 反应
反应| A.①②③④ | B.②①③④ | C.②①④③ | D.④③②① |
您最近一年使用:0次
2022-05-19更新
|
1497次组卷
|
77卷引用:宁夏回族自治区银川一中2021-2022学年高一下学期期中考试化学试题
宁夏回族自治区银川一中2021-2022学年高一下学期期中考试化学试题(已下线)6.1.2 化学反应速率(第2课时 影响化学反应速率的因素)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)第13讲 化学反应速率(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)课后-6.2.1 化学反应的速率-人教2019必修第二册湖北省襄阳市第三十六中学2021-2022学年高一下学期期中考试化学试题北京市清华大学附属中学2021-2022学年高一下学期期中考试化学试题山东省济宁市泗水县2021-2022学年高一下学期期中考试化学试题辽宁省鞍山市第一中学2021-2022学年高一下学期期中考试化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高一下学期期中考试化学试题山东师范大学附属中学2021-2022学年高一下学期期中考试(等级考)化学试题黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期开学考试化学试题 重庆市二0三中学2021-2022学年高一下学期第二次月考化学试题山东省聊城市颐中外国语学校2021-2022学年高一下学期期中考试化学试题新疆乌鲁木齐市第八十中学2022-2023学年高二上学期期中考试化学试题(已下线)2012-2013学年四川省广安市高一下学期期末考试化学试卷2014-2015学年吉林省长春外国语学校高一下期末化学试卷12014-2015学年吉林省长春外国语学校高一下期末化学试卷22015-2016学年山东省青岛市华侨中学高二上学期10月月考化学试卷2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷2015-2016学年新疆生产建设兵团二中高一下期中化学试卷2015-2016学年江西省丰城中学高一下学期第二次月考化学试卷2016-2017学年湖北省七校(荆州中学、襄阳五中、襄阳四中等)高一下学期期中联考化学试卷河北省秦皇岛市卢龙县2016-2017学年高一下学期期末考试化学试题黑龙江省哈尔滨市第六中学2016-2017学年高一下学期期末考试化学试题青海省西宁市第四高级中学2017-2018学年高二上学期第一次月考化学试题福建省南安第一中学2017-2018学年高二上学期期中考试化学试题2017-2018学年高一化学人教版必修2:第二章检测题《课时同步君》2017-2018学年高一化学人教必修2-2.3.1 化学反应的速率(已下线)《周末培优君》2017-2018学年高一下学期化学-第07周 化学反应的速率和限度【全国市级联考】江苏省宿迁市2017-2018学年高一下学期期中考试化学试题【全国市级联考】黑龙江省齐齐哈尔市2017-2018学年高一下学期期末考试化学试题河北省安平中学2017-2018学年高一下学期期末考试化学试题1山西省长治市沁县中学2018-2019学年高一下学期期中考试化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高一下学期第二次月考化学试题吉林省吉林市第五十五中学2018-2019学年高一下学期期中考试化学试题陕西省咸阳百灵中学2019-2020学年高二上学期期中考试化学(理)试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 影响化学反应速率的因素(强化练习)2020年人教版高中化学必修2第二章《化学反应与能量》测试卷26.2.1 化学反应的速率——2020年春高一新人教版第二册化学一课一练(已下线)【南昌新东方】2019 南昌二中 高一下 第二次月考山东省烟台市第二中学2019-2020学年高一下学期4月月考化学试题四川省成都外国语学校2019-2020学年高一下学期开学考试化学试题湖南省双峰县第一中学2019-2020学年高一下学期入学考试化学试题2020年春高一化学新人教版第二册课后同步:6.2.1 化学反应的速率福建省莆田第二十四中学2019-2020学年高一化学下学期期中测试卷黑龙江省牡丹江市第一高级中学2019-2020学年高一下学期5月线上月考化学试题江西省南昌市第二中学2019-2020学年高一下学期第一次月考化学试题甘肃省张掖市高台县第一中学2019-2020学年高一下学期期中考试化学试题山东省烟台市第三中学2019-2020学年高一下学期4月月考化学试题辽宁省朝阳市凌源市凌源中学2019-2020高一下学期5月考试化学试题辽宁省葫芦岛市2019-2020学年高一下学期期末考试化学试题江西省南昌市第十中学2019-2020学年高二上学期第一次月考化学试题陕西省渭南市临渭区铁路自立中学2019-2020学年高一下学期5月月考化学试题山东省临沂第一中学2019-2020学年高一下学期期中考试化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第3节 化学反应的速率甘肃省平凉市庄浪县第一中学2019-2020学年高一下学期期中考试化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第三节 化学反应的快慢和限度 方法帮辽宁省葫芦岛市第八高级中学2020-2021学年高二上学期实验班第一次月考化学试题(人教版2019)必修第二册 第六章 化学反应与能量 第二节 化学反应的速率与限度人教版2019必修第二册 第六章 第二节 第1课时 化学反应的速率湖北省襄阳市第五中学2019-2020学年高一下学期6月月考化学试题江西省赣州市会昌县第五中学2020-2021学年高二上学期第一次月考化学试题兰州市第二十七中学2020-2021学年高一下学期期中考试化学试题四川省乐山市十校2020-2021学年高一下学期期中联考化学试题黑龙江省嫩江市第一中学校等五校2020-2021学年高一下学期期中联考化学试题四川省夹江中学校2020-2021学年高二下学期期中考试化学试题安徽省合肥市六校2020-2021学年高一下学期期末教学质量检测化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)江苏省淮安市车桥中学2021-2022学年高二上学期入学调研(A)化学试题(已下线)选择性必修1 期中检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)吉林省永吉县第四中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.1.2 影响化学反应速率的因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)第09讲 化学反应速率(讲义)-【寒假自学课】2023年高一化学寒假精品课(人教版2019必修第二册)浙江省温州市平阳县万全综合高级中学2021-2022学年高二上学期期中考试化学试题内蒙古自治区包头市2020-2021高一下学期期末教学质量检测试卷化学试题云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(B卷)(已下线)专题03 化学反应速率与化学平衡(知识串讲+专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(沪科版2020必修第二册)
名校
8 . 某小组对一定条件下的反应2SO2(g)+O2(g) 2SO3(g) ΔH=-197.7 kJ/mol进行研究。
2SO3(g) ΔH=-197.7 kJ/mol进行研究。
(1)相同条件下,在某恒容密闭容器中充入2molSO2和1molO2,发生上述反应。下列情况能说明反应达到化学平衡状态的是_______ (填标号)。
A.v(SO2)=2v(O2)
B.容器内气体的压强保持不变
C.SO2与O2的浓度比保持不变
D.混合气体的平均相对分子质量保持不变
E.O2的分压保持不变
F.气体的密度保持不变
(2)在一个容积为2L的恒温恒容密闭容器中,以不同投料方式研究上述反应,得到的数据如下表:
①表中a=_______ ,b=_______ ,甲组实验在该条件下的平衡常数K=_______ 。
②在相同条件下,若将甲组实验按1molSO2、0.5molO2、2molSO3进行投料,则反应开始时v正_______ v逆(填“>”“=”或“<”),平衡时SO3的百分含量与原甲组实验相比_______ (填“变大”“变小”或“不变”)。
③为加快乙组实验的反应速率,下列措施可行的是_______ (填标号)。
A.升高温度 B.降低温度 C.充入适量N2 D.移走SO2
若将乙组实验的容器改为恒温恒压容器,则b值_______ (填“变大”“变小”或“不变”)。
 2SO3(g) ΔH=-197.7 kJ/mol进行研究。
2SO3(g) ΔH=-197.7 kJ/mol进行研究。(1)相同条件下,在某恒容密闭容器中充入2molSO2和1molO2,发生上述反应。下列情况能说明反应达到化学平衡状态的是
A.v(SO2)=2v(O2)
B.容器内气体的压强保持不变
C.SO2与O2的浓度比保持不变
D.混合气体的平均相对分子质量保持不变
E.O2的分压保持不变
F.气体的密度保持不变
(2)在一个容积为2L的恒温恒容密闭容器中,以不同投料方式研究上述反应,得到的数据如下表:
| 实验分组 | 甲组 | 乙组 |
| 反应物 | 2molSO2、1molO2 | 2molSO3 |
| 反应热量 | 放热158.16kJ | 吸热bkJ |
| 反应物的平衡转化率 | a |
②在相同条件下,若将甲组实验按1molSO2、0.5molO2、2molSO3进行投料,则反应开始时v正
③为加快乙组实验的反应速率,下列措施可行的是
A.升高温度 B.降低温度 C.充入适量N2 D.移走SO2
若将乙组实验的容器改为恒温恒压容器,则b值
您最近一年使用:0次
名校
解题方法
9 . 我国科学家使用双功能催化剂催化水煤气变换反应:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH<0,在低温下获得高转化率与高反应速率,反应过程示意图如下,下列说法正确的是


| A.过程Ⅰ、过程Ⅱ均为放热过程 |
| B.图中显示:起始时的2个H2O都参与了反应过程 |
| C.过程Ⅲ只生成了极性共价键 |
| D.使用催化剂降低了水煤气变换反应的ΔH |
您最近一年使用:0次
2022-05-16更新
|
371次组卷
|
15卷引用:宁夏银川市第二中学2021-2022学年高二下学期期中考试化学试题
宁夏银川市第二中学2021-2022学年高二下学期期中考试化学试题天津市第二南开学校2022-2023学年度高二上学期期中质量调查化学试题上海财经大学附属中学2022-2023学年高二上学期期中考试化学试题【市级联考】四川省攀枝花市2019届高三下学期第三次统考理科综合化学试题(已下线)专题07 化学反应中的能量变化——2019年高考真题和模拟题化学分项汇编2019年湖南省郴州市高三第一次教学质量监测化学试题2020届高三《新题速递·化学》1月第02期(考点01-06)北京市通州区2020届高三上学期期末摸底考试化学试题北京市2020届高三下学期周末测试化学试题广东省佛山市第一中学2019-2020学年高一下学期第一次段考化学试题河南省顶级名校2021届高三年级上学期期中考试化学试题山西省潞城第一中学2020-2021学年高二下学期3月月考化学试卷题福建省莆田第一中学2020-2021学年高二下学期期中考试化学试题第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题甘肃省嘉峪关市第一中学2021届高三下学期六模考试理综化学试题
名校
10 . 少量铁片与100mL 0.01mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变 的产量,可以使用如下方法中的
的产量,可以使用如下方法中的
①加 ②加
②加 溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改为足量的浓盐酸
溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改为足量的浓盐酸
 的产量,可以使用如下方法中的
的产量,可以使用如下方法中的 ①加
 ②加
②加 溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改为足量的浓盐酸
溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改为足量的浓盐酸| A.①⑥⑦ | B.③⑤⑧ | C.③⑦⑧ | D.③④⑥⑦⑧ |
您最近一年使用:0次



