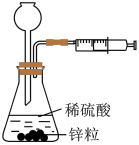
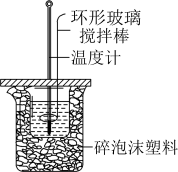
解题方法
1 . 回答下列问题:
(1)将除去氧化膜的镁条插入到稀盐酸溶液中,发现生成氢气的速度变化情况如下图所示: 速度变化的主要原因
速度变化的主要原因______________ 。
② 速度变化的主要原因是
速度变化的主要原因是_____________ 。
(2)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,其原因是____________ ;配制完毕后要加入少量铁屑,其目的是______________ 。
(1)将除去氧化膜的镁条插入到稀盐酸溶液中,发现生成氢气的速度变化情况如下图所示:
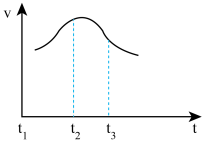
 速度变化的主要原因
速度变化的主要原因②
 速度变化的主要原因是
速度变化的主要原因是(2)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,其原因是
您最近半年使用:0次
名校
2 . 一定条件下可合成乙烯:6H2(g)+2CO2(g) ⇌CH2=CH2 (g)+4H2O(g) 已知温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是
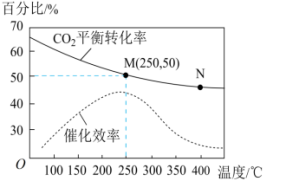
| A.温度不变,若增大压强,ν正增加、ν逆减小 |
| B.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低 |
| C.温度不变,若恒压下向平衡体系中充入惰性气体,平衡不移动 |
| D.若投料比n(H2):n(CO2)=3:1,则图中 M点乙烯的体积分数为7.7% |
您最近半年使用:0次
名校
解题方法
3 . 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定反应过程中产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别,有关说法错误的是
| 实验组别 |  | 温度/ ℃ | 形状(Fe) |
| Ⅰ | 2.0 | 30 | 块状 |
| Ⅱ | 2.5 | 30 | 块状 |
| Ⅲ | 2.5 | 50 | 粉末状 |
| Ⅳ | 2.5 | 50 | 块状 |
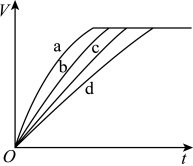
| A.曲线a对应的实验组别为Ⅲ |
| B.对比实验Ⅰ、Ⅱ说明浓度对化学反应速率的影响 |
| C.对比实验Ⅱ、Ⅳ说明温度对化学反应速率的影响 |
| D.曲线a、b、c、d对应的实验组别分别为Ⅳ、Ⅲ、Ⅱ、Ⅰ |
您最近半年使用:0次
2024-04-30更新
|
92次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
4 . 回答下列问题。
(1)一定条件下,在 密闭容器中充入
密闭容器中充入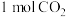 和
和 ,发生反应:
,发生反应: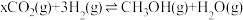 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
___________ ; 内
内 的平均反应速率
的平均反应速率
___________ 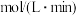 ,平衡时
,平衡时 的转化率为
的转化率为___________ 。
(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
(3)工业上常以水煤气( 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: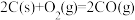
 ;
;
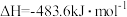 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为___________ 。
(1)一定条件下,在
 密闭容器中充入
密闭容器中充入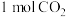 和
和 ,发生反应:
,发生反应: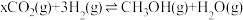 。测得
。测得 和
和 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。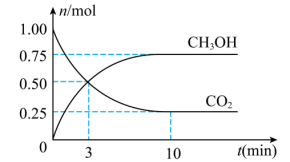

 内
内 的平均反应速率
的平均反应速率
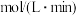 ,平衡时
,平衡时 的转化率为
的转化率为(2)下列措施能提高正反应速率的是___________(填正确答案的字母)。
| A.降低温度 | B.增加 的量 的量 | C.使用催化剂 | D.及时分离出甲醇 |
 和
和 )为原料合成甲醇。已知:
)为原料合成甲醇。已知: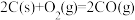
 ;
;
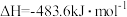 ,则
,则 与
与 制备水煤气的热化学方程式为
制备水煤气的热化学方程式为
您最近半年使用:0次
名校
解题方法
5 . 下列实验方案或装置能达到目的的是
| 选项 | 目的 | 实验方案或装置 |
| A | 定量测量化学反应速率 |
|
| B | 测定酸碱中和热 |
|
| C | 探究浓度影响化学平衡移动的因素 | 水煤气的反应C(s)+H2O(g) CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 CO(g)+ H2(g),增加碳的量,平衡向正反应方向移动。 |
| D | 探究浓度对反应速率的影响 | 分别向两支盛有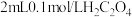 溶液的试管中分别加入 溶液的试管中分别加入 和 和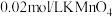 溶液,比较溶液褪色快慢 溶液,比较溶液褪色快慢 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 钢渣是钢铁行业的固体废弃物,含有2CaO·SiO2、Fe2O3、FeO、Al2O3和V2O3等物质。一种以钢渣粉为原料固定CO2并制备V2O3的工艺流程如图所示。
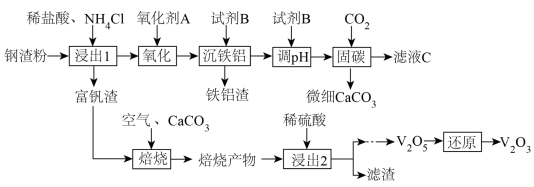
已知钢渣中Ca元素质量分数为30%。V2O3在稀盐酸和NH4Cl混合溶液中不易被浸出。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH如下表所示:
回答下列问题:
(1)浸出1过程生成的SiO2“包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措施有_______ (除粉碎外,举1例)。该浸出过程不使用稀硫酸代替稀盐酸的原因是_______ 。
(2)为避免引入杂质离子,氧化剂A应为_______ (举1例)。
(3)滤液C的溶质可循环利用,试剂B应为_______ 。
(4)若钢渣粉中含有钒酸钙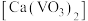 ,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡:
,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡: 。已知
。已知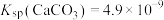 ,
,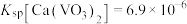 ,则该平衡常数
,则该平衡常数
_______ (结果保留2位有效数字)。
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随pH变化如图所示。已知浸出2的pH约为2.5,则应控制焙烧条件使该钒钙盐为_______ 。该培烧反应的化学方程式是_______ 。

(6)若Ca的浸出率为90%,理论上1吨钢渣在“固碳”中可固定_______ kgCO2。

已知钢渣中Ca元素质量分数为30%。V2O3在稀盐酸和NH4Cl混合溶液中不易被浸出。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ca2+ |
| 开始沉淀的pH | 1.9 | 7.2 | 3.5 | 12.4 |
| 沉淀完全的pH | 2.9 | 8.2 | 5.1 | 13.8 |
(1)浸出1过程生成的SiO2“包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措施有
(2)为避免引入杂质离子,氧化剂A应为
(3)滤液C的溶质可循环利用,试剂B应为
(4)若钢渣粉中含有钒酸钙
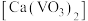 ,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡:
,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡: 。已知
。已知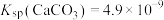 ,
,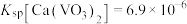 ,则该平衡常数
,则该平衡常数
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随pH变化如图所示。已知浸出2的pH约为2.5,则应控制焙烧条件使该钒钙盐为

(6)若Ca的浸出率为90%,理论上1吨钢渣在“固碳”中可固定
您最近半年使用:0次
7 .  是
是 还原工业废水中六价Cr的催化剂,反应机理如图所示。
还原工业废水中六价Cr的催化剂,反应机理如图所示。
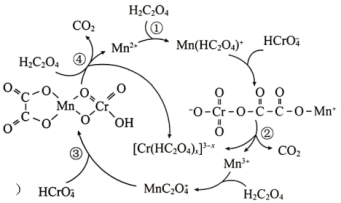
下列叙述错误 的是
 是
是 还原工业废水中六价Cr的催化剂,反应机理如图所示。
还原工业废水中六价Cr的催化剂,反应机理如图所示。
下列叙述
| A.反应①、③均不属于氧化还原反应 |
B.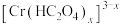 中Cr元素的化合价为+3价 中Cr元素的化合价为+3价 |
| C.加入Mn能够降低活化能,提高六价铬的转化率 |
D.总反应 |
您最近半年使用:0次
名校
解题方法
8 . 工业上利用黄铁矿(FeS2)制取硫酸,其反应流程如下:

| A.反应①矿石粉碎的目的是提高反应速率 |
| B.反应②中即使通入过量的氧气,也不能将SO2全部转化成SO3 |
| C.接触室选择500℃左右的温度是因为比常温更有利于合成SO3 |
| D.过量的氨水吸收SO2的化学方程式:2NH3·H2O+SO2=(NH4)2SO3+H2O |
您最近半年使用:0次
2024-03-20更新
|
63次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
9 . 对于可逆反应 ,当其他条件不变时,C的体积分数
,当其他条件不变时,C的体积分数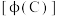 在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是

 ,当其他条件不变时,C的体积分数
,当其他条件不变时,C的体积分数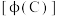 在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的体积分数将增大 |
B.该反应的 |
C.化学方程式中,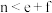 |
| D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动 |
您最近半年使用:0次
名校
10 . 在水溶液中进行的反应: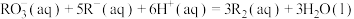 ,已知该反应速率方程为
,已知该反应速率方程为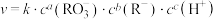 (k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
(k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
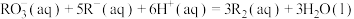 ,已知该反应速率方程为
,已知该反应速率方程为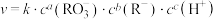 (k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
(k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是实验编号 相关数据 | ① | ② | ③ | ④ | ⑤ |
 | 0.008 | 0.008 | 0.004 | 0.008 | 0.008 |
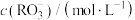 | 0.001 | 0.001 | 0.001 | 0.002 | 0.001 |
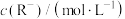 | 0.10 | 0.20 | 0.20 | 0.10 | 0.40 |
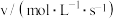 | 2.4×10-8 | 4.8×10-8 | 1.2×10-8 | 4.8×10-8 | v1 |
| A.反应体系的三种物质中,R-(aq)的浓度对反应速率影响最大 |
B.速率常数 的数值为3.75 的数值为3.75 |
| C.a、b、c的值分别为2、1、2 |
| D.实验⑤中,v1=4.8×10-8 |
您最近半年使用:0次
2024-02-13更新
|
65次组卷
|
2卷引用:宁夏银川市育才中学2023-2024学年高三上学期1月期末理科综合化学试题