1 . 我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生 的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
 的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是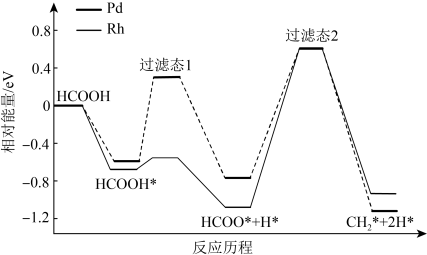
| A.参与反应的反应物总键能小于生成物总键能 |
B.Pd和Rh分别作催化剂时HCOOH分解产生 的 的 不同 不同 |
| C.HCOOH吸附在催化剂表面是一个放热过程 |
D. 是该历程的决速步骤 是该历程的决速步骤 |
您最近一年使用:0次
2024-05-17更新
|
140次组卷
|
2卷引用:2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学
名校
2 . 一定条件下可合成乙烯:6H2(g)+2CO2(g) ⇌CH2=CH2 (g)+4H2O(g) 已知温度对CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法正确的是
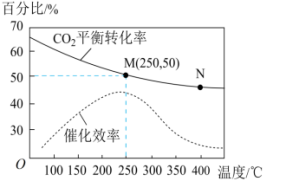
| A.温度不变,若增大压强,ν正增加、ν逆减小 |
| B.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低 |
| C.温度不变,若恒压下向平衡体系中充入惰性气体,平衡不移动 |
| D.若投料比n(H2):n(CO2)=3:1,则图中 M点乙烯的体积分数为7.7% |
您最近一年使用:0次
3 . 对于可逆反应 ,当其他条件不变时,C的体积分数
,当其他条件不变时,C的体积分数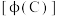 在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是

 ,当其他条件不变时,C的体积分数
,当其他条件不变时,C的体积分数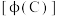 在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是
| A.达到平衡后,若使用催化剂,C的体积分数将增大 |
B.该反应的 |
C.化学方程式中,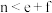 |
| D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动 |
您最近一年使用:0次
名校
4 . 在水溶液中进行的反应: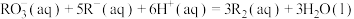 ,已知该反应速率方程为
,已知该反应速率方程为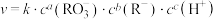 (k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
(k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
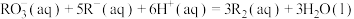 ,已知该反应速率方程为
,已知该反应速率方程为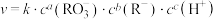 (k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是
(k为常数),为探究反应速率(v)与反应物浓度的关系,在20℃进行实验,所得的数据如下表:下列结论正确的是实验编号 相关数据 | ① | ② | ③ | ④ | ⑤ |
 | 0.008 | 0.008 | 0.004 | 0.008 | 0.008 |
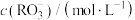 | 0.001 | 0.001 | 0.001 | 0.002 | 0.001 |
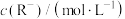 | 0.10 | 0.20 | 0.20 | 0.10 | 0.40 |
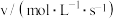 | 2.4×10-8 | 4.8×10-8 | 1.2×10-8 | 4.8×10-8 | v1 |
| A.反应体系的三种物质中,R-(aq)的浓度对反应速率影响最大 |
B.速率常数 的数值为3.75 的数值为3.75 |
| C.a、b、c的值分别为2、1、2 |
| D.实验⑤中,v1=4.8×10-8 |
您最近一年使用:0次
2024-02-13更新
|
65次组卷
|
2卷引用:宁夏银川市育才中学2023-2024学年高三上学期1月期末理科综合化学试题
5 . 下列相关事实不能用勒夏特列原理解释的是
| A.增大压强能提高合成氨的产率 | B.升高温度,水的离子积常数增大 |
C.加入 能加快 能加快 分解放出 分解放出 | D.大部分盐类水解符合“越稀越水解”的规律 |
您最近一年使用:0次
6 . 人们可通过改变条件来调控化学反应的速率与限度,使其向着对人类更有益的方向发展。下列条件的改变不是从化学反应速率与限度的角度考虑的是
| A.橡胶轮胎中加入防老剂 | B.燃煤中加入CaO |
| C.汽车排气管中使用三元催化器 | D.工业合成氨不断移去液氨 |
您最近一年使用:0次
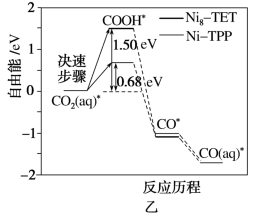
7 . 如图甲装置可将催化剂同时作用在阳极和阴极,从而进行甲醇和CO2的混合电解。图乙为CO2→CO在不同催化剂条件下的反应历程。下列说法正确的是
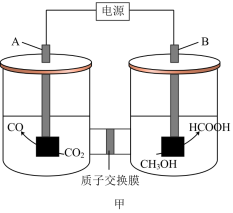


| A.电极B与电源负极相连,甲醇被氧化 |
| B.电极A发生的反应是CO2+2e-+H2O=CO+2OH- |
| C.选择Ni8-TET催化剂催化,会比Ni-TPP消耗更多电能 |
| D.若有2molH+穿过质子交换膜,则理论上有44gCO2反应 |
您最近一年使用:0次
2024-01-24更新
|
351次组卷
|
2卷引用:宁夏银川一中2023-2024学年高二上学期期末考试化学试题
名校
8 . 重要的化工原料丁烯(C4H8)可由丁烷(C4H10)催化脱氢制备,反应如下:
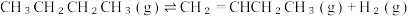 △H
△H
已知:i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.CH2=CHCH2CH3(g)+6O2 (g)=4CO2 (g)+4H2O(l) △H1
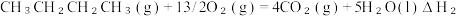
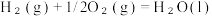 △H3
△H3
(1)用△H1、△H2、△H3表示丁烷催化脱氢反应的反应热△H=_______ 。
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一、
①催化剂使用 段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是_______ 。
②其他条件相同时,以SiO₂为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
下列说法正确的是_______ (填序号)。[收率=(生成某产物的原料量/投入的原料量)×100%]
a.脱氢反应中SiO2不起催化作用 b. CrOx的含量越高,反应的催化效果越好
c. CrOx的含量对丁烷脱氢反应的焓变有影响 d. 正丁烯收率越高,则原料的利用率越高
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。
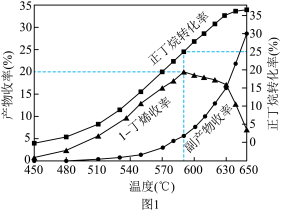
① 实际生产温度选择590℃, 由图1说明其理由是_______ 。
②590℃时,向体积为 1L 的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为_______ mol/(L·min)。
(4)利用电解装置可以将尾气中的 NO 转化为尿素[CO(NH2) 2,其中碳的化合价为+4 价,属于非电解质],工作原理如图2所示。
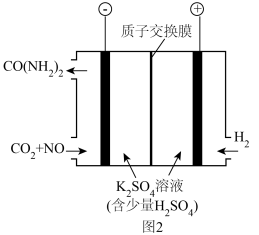
①阴极的电极反应式为_______ 。
②反应 段时间后,阳极区的pH基本不变,结合化学用语解释原因为_______ 。
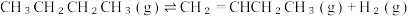 △H
△H已知:i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.CH2=CHCH2CH3(g)+6O2 (g)=4CO2 (g)+4H2O(l) △H1
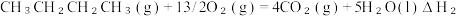
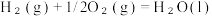 △H3
△H3(1)用△H1、△H2、△H3表示丁烷催化脱氢反应的反应热△H=
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一、
①催化剂使用 段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是
②其他条件相同时,以SiO₂为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
| 实验组 | 催化剂组成 | 正丁烷转化率 /% | 正丁烯收率 /% |
| 1 | 无催化剂 | 5 | 0.35 |
| 2 | SiO2 | 5 | 0.35 |
| 3 | SiO2+9%CrOx | 25.5 | 18.3 |
| 4 | SiO2+15% CrOx | 27.5 | 20.65 |
| 5 | SiO2+21%CrOx | 24 | 17.87 |
a.脱氢反应中SiO2不起催化作用 b. CrOx的含量越高,反应的催化效果越好
c. CrOx的含量对丁烷脱氢反应的焓变有影响 d. 正丁烯收率越高,则原料的利用率越高
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。

① 实际生产温度选择590℃, 由图1说明其理由是
②590℃时,向体积为 1L 的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为
(4)利用电解装置可以将尾气中的 NO 转化为尿素[CO(NH2) 2,其中碳的化合价为+4 价,属于非电解质],工作原理如图2所示。

①阴极的电极反应式为
②反应 段时间后,阳极区的pH基本不变,结合化学用语解释原因为
您最近一年使用:0次
名校
解题方法
9 . 废弃电池是一种有害垃圾,合理处理则能变废为宝。下图是废弃锌锰电池的处理流程图:
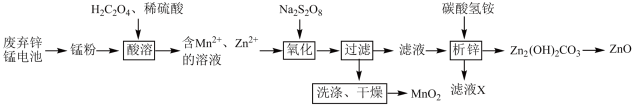
已知:锰粉的主要成分是Mn元素的+2、+3、+4价氧化物和ZnO。
回答下列问题:
(1)“废弃锌锰电池→锰粉”的操作是拆分、煅烧,煅烧类似于实验室中的焙烧,实验室焙烧使用的仪器名称是___________ 。
(2)“酸溶”采用锰粉比锰块的浸取速率快,为提高“酸溶”的浸取速率,还可以采取的措施有___________ (任写两条),
(3)“酸溶” 过程中H2C2O4与Mn元素+4价氧化物反应的离子方程式___________ ,“氧化”操作的氧化产物是___________ (填化学式)。
(4)“洗涤、干燥”时,检验MnO2洗涤干净的实验方法及现象是___________ 。
(5)滤液X可以用于制取化肥,其中除Na+外,主要含___________ 、 (填离子符号)。
(填离子符号)。
(6)由Zn2(OH)2CO3制备ZnO的条件是加热,写出该反应的化学方程式:___________ 。

已知:锰粉的主要成分是Mn元素的+2、+3、+4价氧化物和ZnO。
回答下列问题:
(1)“废弃锌锰电池→锰粉”的操作是拆分、煅烧,煅烧类似于实验室中的焙烧,实验室焙烧使用的仪器名称是
(2)“酸溶”采用锰粉比锰块的浸取速率快,为提高“酸溶”的浸取速率,还可以采取的措施有
(3)“酸溶” 过程中H2C2O4与Mn元素+4价氧化物反应的离子方程式
(4)“洗涤、干燥”时,检验MnO2洗涤干净的实验方法及现象是
(5)滤液X可以用于制取化肥,其中除Na+外,主要含
 (填离子符号)。
(填离子符号)。(6)由Zn2(OH)2CO3制备ZnO的条件是加热,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
10 . 反应Fe+H2SO4=FeSO4+H2↑的能量变化如图所示:
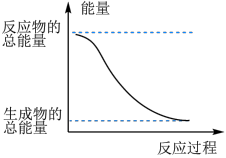
(1)该反应为___________ 反应(填“吸热”或“放热”)。
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为___________ (填“正”或“负”)极;其电极反应式为:___________ ,外电路中电流由___________ 流出。(填电极材料名称)。
(3)若要使该反应的反应速率加快,下列措施可行的是 。

(1)该反应为
(2)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为
(3)若要使该反应的反应速率加快,下列措施可行的是 。
| A.增加铁的量 | B.改稀硫酸为98%的硫酸 |
| C.增大压强 | D.滴加几滴CuSO4溶液 |
您最近一年使用:0次



