1 .  是
是 还原工业废水中六价Cr的催化剂,反应机理如图所示。
还原工业废水中六价Cr的催化剂,反应机理如图所示。
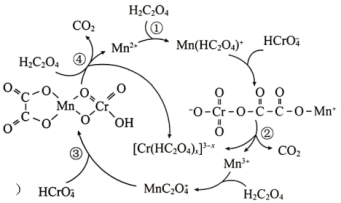
下列叙述错误 的是
 是
是 还原工业废水中六价Cr的催化剂,反应机理如图所示。
还原工业废水中六价Cr的催化剂,反应机理如图所示。
下列叙述
| A.反应①、③均不属于氧化还原反应 |
B.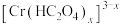 中Cr元素的化合价为+3价 中Cr元素的化合价为+3价 |
| C.加入Mn能够降低活化能,提高六价铬的转化率 |
D.总反应 |
您最近一年使用:0次
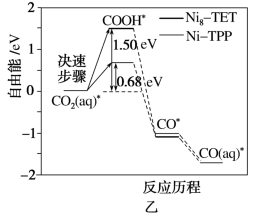
2 . 如图甲装置可将催化剂同时作用在阳极和阴极,从而进行甲醇和CO2的混合电解。图乙为CO2→CO在不同催化剂条件下的反应历程。下列说法正确的是
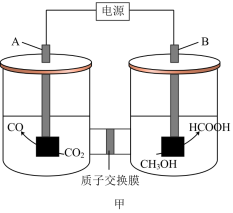


| A.电极B与电源负极相连,甲醇被氧化 |
| B.电极A发生的反应是CO2+2e-+H2O=CO+2OH- |
| C.选择Ni8-TET催化剂催化,会比Ni-TPP消耗更多电能 |
| D.若有2molH+穿过质子交换膜,则理论上有44gCO2反应 |
您最近一年使用:0次
2024-01-24更新
|
351次组卷
|
2卷引用:宁夏银川一中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
3 . 依据下列实验现象可以推出结论的是
| 选项 | 实验 | 现象 | 结论 |
| A |  | ①中产生大量气体 ②中无明显现象 |  是 是 分解的催化剂 分解的催化剂 |
| B |  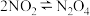 | 压缩体积,气体颜色加深 | 气体颜色加深是平衡正向移动的结果 |
| C | 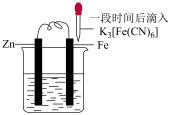 | 铁表面产生蓝色沉淀 | Zn不能对Fe起到保护作用 |
| D | 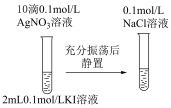 | 先产生黄色沉淀 滴加2mL NaCl后,上层清液无明显变化 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-11更新
|
226次组卷
|
3卷引用:宁夏银川一中2023-2024学年高二上学期期末考试化学试题
名校
4 . 关于下列说法正确的是
| A.催化剂都不参加化学反应 |
| B.使用催化剂能够降低化学反应的反应热(ΔH) |
| C.可逆反应中减小产物的浓度可增大正反应的速率 |
| D.增大反应体系的压强,反应速率不一定增大 |
您最近一年使用:0次
名校
5 . 一定条件下,0.3mol 和0.9mol
和0.9mol 在体积为1L的密闭容器中发生反应:
在体积为1L的密闭容器中发生反应:
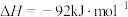 ,反应进行2min,
,反应进行2min, 的物质的量增加了0.4mol。
的物质的量增加了0.4mol。
下列说法正确的是
 和0.9mol
和0.9mol 在体积为1L的密闭容器中发生反应:
在体积为1L的密闭容器中发生反应:
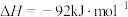 ,反应进行2min,
,反应进行2min, 的物质的量增加了0.4mol。
的物质的量增加了0.4mol。下列说法正确的是
A.平衡后再充入 ,既能加快反应速率又能提高 ,既能加快反应速率又能提高 的平衡转化率 的平衡转化率 |
| B.将容器的体积压缩,可增大单位体积活化分子数,增大活化分子的百分数,加快反应速率 |
| C.反应进行2min,放出的热量值小于18.4kJ |
D. 的体积分数保持不变,能说明反应达到平衡 的体积分数保持不变,能说明反应达到平衡 |
您最近一年使用:0次
2023-08-05更新
|
372次组卷
|
3卷引用:宁夏银川市上游学校2023-2024学年高二下学期开学考试化学试卷
6 . 下列实验设计能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 探究浓度对化学反应速率的影响 | 常温常压下,向一试管中加入10%的 溶液,另一试管中加入 溶液,另一试管中加入 固体和5%的 固体和5%的 溶液,观察现象 溶液,观察现象 |
| B | 制备并得到纯净的溴苯 | 向含溴的苯溶液中加入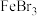 溶液,充分反应后,过滤洗涤 溶液,充分反应后,过滤洗涤 |
| C | 证明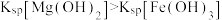 | 向  NaOH溶液中滴加2滴同浓度的 NaOH溶液中滴加2滴同浓度的 溶液后,再滴加2滴同浓度的 溶液后,再滴加2滴同浓度的 溶液,观察现象 溶液,观察现象 |
| D | 验证某溶液中一定含有钾元素 | 用洁净的铁丝蘸取该溶液在酒精灯外焰上灼烧,透过蓝色钴玻璃观察,火焰呈紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-16更新
|
133次组卷
|
2卷引用:宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题
名校
解题方法
7 . 电解锰渣含有 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含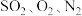 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
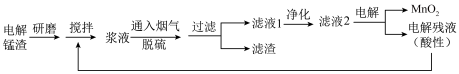
(1)上述流程中为增大反应速率采取的措施有_______ 。
(2)电解锰渣中的 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为_______ 。
(3)电解锰渣与电解残液混合后,浆液中部分离子浓度 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。
①用方程式表示脱硫过程溶液 降低的原因
降低的原因_______ 。
②分析浆液中 浓度增大的原因:
浓度增大的原因:
i. 被
被 还原;
还原;
ii. 被
被 还原,离子方程式为
还原,离子方程式为_______ ;
iii._______ (用离子方程式表示)。
(4)电解获得 ,装置如下图所示。
,装置如下图所示。
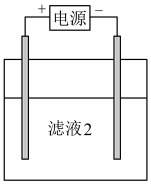
①滤液2在电解池_______ (填“阳”或“阴”)极放电产生 。
。
②净化过程须除去 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:_______ 。
 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含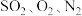 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
(1)上述流程中为增大反应速率采取的措施有
(2)电解锰渣中的
 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为(3)电解锰渣与电解残液混合后,浆液中部分离子浓度
 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。 |  |  |  |  | |
 | 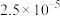 |  | 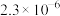 |  | 7.5 |
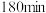 |  | 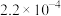 |  | 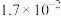 | 1.7 |
 降低的原因
降低的原因②分析浆液中
 浓度增大的原因:
浓度增大的原因:i.
 被
被 还原;
还原;ii.
 被
被 还原,离子方程式为
还原,离子方程式为iii.
(4)电解获得
 ,装置如下图所示。
,装置如下图所示。
①滤液2在电解池
 。
。②净化过程须除去
 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:
您最近一年使用:0次
2023-05-07更新
|
550次组卷
|
3卷引用:宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题
宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题北京市朝阳区2022-2023年高三下学期第二次模拟考试化学试题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
名校
解题方法
8 . 中医药根植于中华传统文化。下列说法不正确 的是
| A.屠呦呦团队用乙醚从青蒿中提取了青蒿素,采用了萃取的方法 |
| B.中药甘草、金银花、石膏、明矾等的主要化学成分都是有机物 |
| C.汤药存放于冰箱中,可以减小其腐败变质的速率 |
| D.煎制草药不宜使用铁质容器,可能因为草药的有些成分能与铁发生反应影响药效 |
您最近一年使用:0次
2023-03-31更新
|
924次组卷
|
6卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题
宁夏平罗中学2022-2023学年高二下学期期中考试化学试题北京市西城区2023届一模考试化学试题(已下线)专题01 化学与STSE(已下线)专题05 元素及其化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题广西柳州高级中学2023-2024学年高三上学期8月开学考试化学试题
名校
解题方法
9 . 为保护环境,充分利用钴资源,一种以废旧钴酸锂电池材料(正极材料主要含有LiCoO2、铝箔及金属钢壳)回收钴酸锂的工艺流程如下:
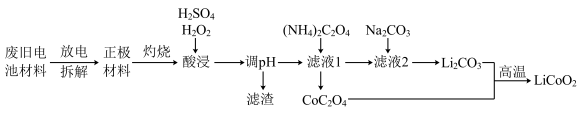
已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
请回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在_________ (填标号)中进行放电。粉碎的目的是_________ 。
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是_________ (填标号)。
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为_________ 。
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为_________ 。

(3)“调pH”时,溶液应控制的pH范围为_________ ,选用的最佳试剂是_________ (填标号)。
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为_________ 。

已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
| 离子 | Co3+ | Fe3+ | Co2+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 0.3 | 2.7 | 7.2 | 7.6 | 3.6 |
| 完全沉淀的pH | 1.1 | 3.2 | 9.2 | 9.6 | 5.2 |
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为

(3)“调pH”时,溶液应控制的pH范围为
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为
您最近一年使用:0次
2023-03-29更新
|
334次组卷
|
2卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题(重点班)
名校
10 . 近年来光催化处理船舶尾气技术被称为是一种“绿色友好”技术,以 半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成
半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成 自由基,光生电子则与
自由基,光生电子则与 等反应在催化剂表面生成
等反应在催化剂表面生成 、
、 等氧化物,这些氧化物作用于尾气中的
等氧化物,这些氧化物作用于尾气中的 、
、 等污染物并将其氧化降解,原理见图。下列说法错误的是
等污染物并将其氧化降解,原理见图。下列说法错误的是
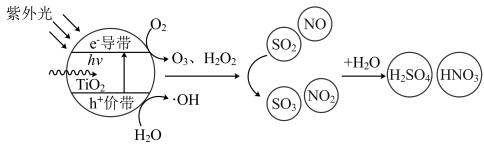
 半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成
半导体为基底的纳米催化剂,表面经光激发后产生空穴和光生电子,光生空穴被表面吸附水或氢氧根离子捕获生成 自由基,光生电子则与
自由基,光生电子则与 等反应在催化剂表面生成
等反应在催化剂表面生成 、
、 等氧化物,这些氧化物作用于尾气中的
等氧化物,这些氧化物作用于尾气中的 、
、 等污染物并将其氧化降解,原理见图。下列说法错误的是
等污染物并将其氧化降解,原理见图。下列说法错误的是
A.含有氮氧化物、硫氧化物的尾气排放到大气中易形成酸雨, 小于7的雨水为酸雨 小于7的雨水为酸雨 |
B.除 、NO的总反应分别为 、NO的总反应分别为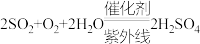 、 、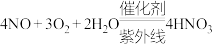 |
| C.催化剂可以改变氮氧化物、硫氧化物被氧化的速率 |
| D.尾气中含有大量有害物质,但经过科学的处理可以转化为多种有实用价值的物质 |
您最近一年使用:0次
2023-03-25更新
|
410次组卷
|
4卷引用:宁夏回族自治区银川一中2022-2023学年高一下学期期中考试化学试题



