电解锰渣含有 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含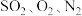 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
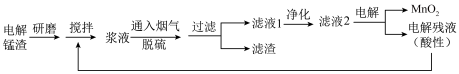
(1)上述流程中为增大反应速率采取的措施有_______ 。
(2)电解锰渣中的 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为_______ 。
(3)电解锰渣与电解残液混合后,浆液中部分离子浓度 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。
①用方程式表示脱硫过程溶液 降低的原因
降低的原因_______ 。
②分析浆液中 浓度增大的原因:
浓度增大的原因:
i. 被
被 还原;
还原;
ii. 被
被 还原,离子方程式为
还原,离子方程式为_______ ;
iii._______ (用离子方程式表示)。
(4)电解获得 ,装置如下图所示。
,装置如下图所示。
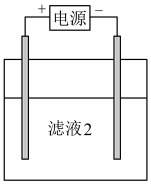
①滤液2在电解池_______ (填“阳”或“阴”)极放电产生 。
。
②净化过程须除去 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:_______ 。
 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含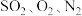 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
(1)上述流程中为增大反应速率采取的措施有
(2)电解锰渣中的
 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为(3)电解锰渣与电解残液混合后,浆液中部分离子浓度
 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。 |  |  |  |  | |
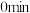 | 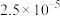 |  | 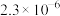 |  | 7.5 |
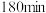 |  | 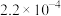 |  | 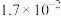 | 1.7 |
 降低的原因
降低的原因②分析浆液中
 浓度增大的原因:
浓度增大的原因:i.
 被
被 还原;
还原;ii.
 被
被 还原,离子方程式为
还原,离子方程式为iii.
(4)电解获得
 ,装置如下图所示。
,装置如下图所示。
①滤液2在电解池
 。
。②净化过程须除去
 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:
2023·北京朝阳·二模 查看更多[3]
北京市朝阳区2022-2023年高三下学期第二次模拟考试化学试题宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
更新时间:2023-05-07 21:20:43
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
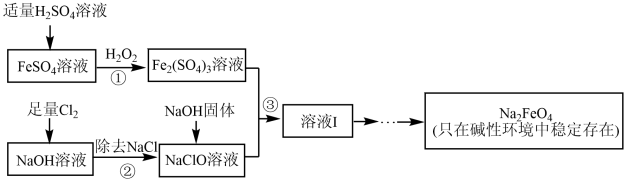
(1)高铁酸钠中铁元素的化合价为_______ ,次氯酸钠的电子式是_______ 。
(2)铁元素位于元素周期表的第四周期第VIII族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是_______ 。
(3)步骤①反应的离子方程式是_______ 。
(4)工业废水中常含有一定量的 易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理
转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理_______ 。
(5)已知Ksp[Cr(OH)3]=1×10-30。室温下,除去被SO2还原所得溶液中的Cr3+[使c(Cr3+)≤1×10-6mol·L-1],需调节溶液的pH至少为_______ 。
(6)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。写出Cr(OH)3与NaOH反应的方程式_______ 。

(1)高铁酸钠中铁元素的化合价为
(2)铁元素位于元素周期表的第四周期第VIII族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是
(3)步骤①反应的离子方程式是
(4)工业废水中常含有一定量的
 易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将
易被人体吸收积累而导致肝癌。处理工业含铬废水的方法通常是将 转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理
转化为Cr3+,再将Cr3+转化为沉淀。利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理(5)已知Ksp[Cr(OH)3]=1×10-30。室温下,除去被SO2还原所得溶液中的Cr3+[使c(Cr3+)≤1×10-6mol·L-1],需调节溶液的pH至少为
(6)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。写出Cr(OH)3与NaOH反应的方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上制备硫酸的某一步反应为 ,该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为
,该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为_______ L。
(2)兴趣小组欲探究SO2与FeCl3、I2的反应,设计了如下实验:分别将SO2气体通入氯化铁溶液和含有淀粉的I2溶液中至反应结束为止,观察现象。
①FeCl3溶液由黄色变为浅绿色,写出此步反应的离子方程式:_______ 。
②含有淀粉的I2溶液蓝色逐渐消失,说明氧化性:I2_______ (填">"或“<”) 。若要证明SO2与FeCl2、I-的还原性强弱关系,还需要补充的实验是(不增加其他试剂)
。若要证明SO2与FeCl2、I-的还原性强弱关系,还需要补充的实验是(不增加其他试剂)_______ 。
(3)工业上将SO2催化氧化为SO3的反应制得的气体中含有大量的SO3和未反应完的SO2等。现欲验证此混合气体中该两种气体的存在,设计如下步骤:
①将混合气体通入酸性高锰酸钾溶液,溶液颜色逐渐变浅,说明气体中含有SO2。请写出使溶液颜色变浅的反应的离子方程式:_______ 。
②另将混合气体通入BaCl2溶液,产生白色沉淀。请写出白色沉淀的化学式:_______ 。
(1)工业上制备硫酸的某一步反应为
 ,该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为
,该反应转移2.75mol电子时,生成的二氧化硫在标准状况下的体积为(2)兴趣小组欲探究SO2与FeCl3、I2的反应,设计了如下实验:分别将SO2气体通入氯化铁溶液和含有淀粉的I2溶液中至反应结束为止,观察现象。
①FeCl3溶液由黄色变为浅绿色,写出此步反应的离子方程式:
②含有淀粉的I2溶液蓝色逐渐消失,说明氧化性:I2
 。若要证明SO2与FeCl2、I-的还原性强弱关系,还需要补充的实验是(不增加其他试剂)
。若要证明SO2与FeCl2、I-的还原性强弱关系,还需要补充的实验是(不增加其他试剂)(3)工业上将SO2催化氧化为SO3的反应制得的气体中含有大量的SO3和未反应完的SO2等。现欲验证此混合气体中该两种气体的存在,设计如下步骤:
①将混合气体通入酸性高锰酸钾溶液,溶液颜色逐渐变浅,说明气体中含有SO2。请写出使溶液颜色变浅的反应的离子方程式:
②另将混合气体通入BaCl2溶液,产生白色沉淀。请写出白色沉淀的化学式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。试回答下列问题:
(1)“浸出”时用到的“试剂X”为______________ (填名称)。
(2)写出“氧化”过程的离子方程式_______________________________________ 。
(3)“调pH”过程可以选用_______________ (填序号)。
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是______________________________ (填化学式,下同)。
(4)“试剂Y”是__________________ 。
(5)“操作1”的方法是__________ ;在“操作1”时,必须采取的实验措施是_____________ 。
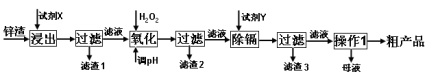
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。试回答下列问题:
(1)“浸出”时用到的“试剂X”为
(2)写出“氧化”过程的离子方程式
(3)“调pH”过程可以选用
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是
(4)“试剂Y”是
(5)“操作1”的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】影响化学反应速率的因素很多,某化学小组用实验的方法进行探究。
Ⅰ.探究一:备选药品:镁片、铝片、0.500 mol·L-1H2SO4、18.4 mol·L-1H2SO4。
甲同学研究的实验报告:
(1)甲同学用砂纸打磨镁片和铝片的原因是______________________________ ;选择H2SO4浓度为________________ 。
(2) 实验报告中现象为_______________________________________________ 。
Ⅱ.探究二:实验室经常用Na2S2O3与H2SO4的反应探究化学反应速率的影响因素,利用图1所示装置(夹持装置略去)进行实验,观察到锥形瓶底部有淡黄色浑浊。
(3)请用化学方程式表示出实验原理_________________________________ ,乙同学在实验过程中对产生的气体进行收集,并在2min内6个时间点对注射器内气体进行读数,记录数据并绘制出图像(如图2)。
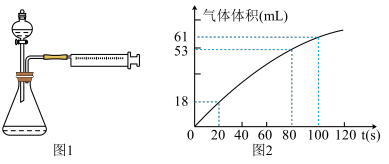
0~20s内反应速率υ1=__________ mL·s-1,80~100s内反应速率υ2=__________ mL·s-1。不考虑实验测量误差,分析速率差异的主要原因是_____________ 。
Ⅰ.探究一:备选药品:镁片、铝片、0.500 mol·L-1H2SO4、18.4 mol·L-1H2SO4。
甲同学研究的实验报告:
| 实验步骤 | 现象 | 结论 |
| ①用砂纸打磨镁片和铝片; ②分别取等体积等浓度的硫酸于两支试管中; ③将镁片和铝片同时投入到试管中。 | 金属的性质越活泼, 反应速率越快 |
(2) 实验报告中现象为
Ⅱ.探究二:实验室经常用Na2S2O3与H2SO4的反应探究化学反应速率的影响因素,利用图1所示装置(夹持装置略去)进行实验,观察到锥形瓶底部有淡黄色浑浊。
(3)请用化学方程式表示出实验原理

0~20s内反应速率υ1=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】三盐基硫酸铅简称“三盐”,是一种重要的工业原料,其化学式为 (相对分子质量为990)。以
(相对分子质量为990)。以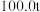 铅泥(主要成分为
铅泥(主要成分为 、
、 及
及 等,
等, 、
、 不与
不与 溶液反应)为原料制备三盐的工艺流程如图所示。
溶液反应)为原料制备三盐的工艺流程如图所示。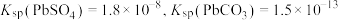 。
。
回答下列问题:
(1)“转化”时 发生反应的离子方程式为
发生反应的离子方程式为_______ ,反应达到平衡时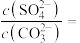
_______ 。
(2)“酸溶”时若有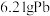 发生反应,则生成
发生反应,则生成 的体积(标准状况)为
的体积(标准状况)为_______  ,为提高“酸溶”速率,可采取的措施是
,为提高“酸溶”速率,可采取的措施是_______ (任意写出一条)。
(3)“滤液2”中溶质的主要成分的化学式为_______ 。
(4)“合成”时主要反应的化学方程式为_______ 。
(5)若得到纯净干燥的三盐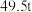 ,假设铅泥中的铅元素有
,假设铅泥中的铅元素有 转化为三盐,则铅泥中央铅元素的质量分数为
转化为三盐,则铅泥中央铅元素的质量分数为_______  。
。
 (相对分子质量为990)。以
(相对分子质量为990)。以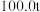 铅泥(主要成分为
铅泥(主要成分为 、
、 及
及 等,
等, 、
、 不与
不与 溶液反应)为原料制备三盐的工艺流程如图所示。
溶液反应)为原料制备三盐的工艺流程如图所示。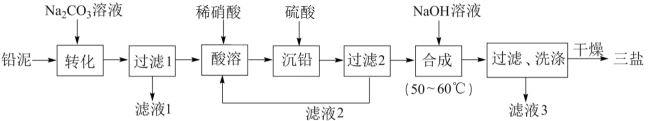
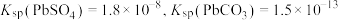 。
。回答下列问题:
(1)“转化”时
 发生反应的离子方程式为
发生反应的离子方程式为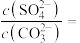
(2)“酸溶”时若有
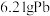 发生反应,则生成
发生反应,则生成 的体积(标准状况)为
的体积(标准状况)为 ,为提高“酸溶”速率,可采取的措施是
,为提高“酸溶”速率,可采取的措施是(3)“滤液2”中溶质的主要成分的化学式为
(4)“合成”时主要反应的化学方程式为
(5)若得到纯净干燥的三盐
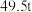 ,假设铅泥中的铅元素有
,假设铅泥中的铅元素有 转化为三盐,则铅泥中央铅元素的质量分数为
转化为三盐,则铅泥中央铅元素的质量分数为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】I.已知锌与稀硫酸反应为放热反应,某探究小组为了探究其反应过程中的速率变化,用排水集气法收集反应放出的氢气,实验记录如下:
(1)反应速率最大的(即0~1min、1~2min、2~3min、3~4min、4~5min)时间段为_______ ,原因是_______ 。
(2)反应速率最小的时间段为_______ ,原因是_______ 。
II.该探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol/L HNO3、2.00 mol/L HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴。
(3)他们能完成哪些因素对速率影响的探究_______ ?。
(4)请根据能进行的探究内容,补充完成下列实验设计表的空白部分,完成探究实验:
(5)整个实验中应控制的不变量是硝酸溶液体积和_______ 。
| 经过时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 30 | 120 | 280 | 350 | 370 |
(2)反应速率最小的时间段为
II.该探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol/L HNO3、2.00 mol/L HNO3,细颗粒大理石、粗颗粒大理石,35℃水浴。
(3)他们能完成哪些因素对速率影响的探究
(4)请根据能进行的探究内容,补充完成下列实验设计表的空白部分,完成探究实验:
| 实验编号 | T/℃ | 大理石规格 | 硝酸浓度(mol/L) |
| ① | 常温 | 细颗粒 | 2.00 |
| ② | 细颗粒 | 1.00 | |
| ③ | 35 | 2.00 | |
| ④ | 35 | 2.00 |
您最近一年使用:0次
【推荐1】碳、氮、氯是重要的非金属元素,它们的单质及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)煤的气化过程中,存在如下反应:
①C(s)+O2(g) ⇌CO2(g) ∆H1=-394.1 kJ/mol
②2CO(g)+O2(g)⇌2CO2(g) ∆H2=-566.0 kJ/mol
③2H2(g)+O2(g)⇌2H2O(g) ∆H3=-483.6 kJ/mol
写出利用水煤浆生产水煤气的热化学方程式_______ 。
(2)已知常温下部分弱电解质的电离平衡常数如表:
①常温下,物质的量溶度相同的三种溶液①NaF溶液 ②NaClO溶液 ③Na2CO3溶液,其pH由大到小的顺序是_______ (填序号)。
②25°C时,pH=4的NH4Cl溶液中各离子浓度的大小关系为_______ 。
(3)实验所用NaOH工业上的制备,以电解精制饱和食盐水的方法制取氯气、氢气、烧碱。图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

①写出电解饱和食盐水的离子方程式_______ 。
②精制饱和食盐水从图中_______ 位置补充(选填“a”、“b”、“c”或“d”)。
(4)含有NaCN的污水危害很大,0.01 mol/L的NaCN溶液pH=9,请判断该溶液中:c(CN-)_______ c(OH-)(填“>”、“<”或“=”),处理含NaCN污水时,可用制取的次氯酸钠溶液将CN-在酸性条件下氧化生成N2与CO2,该反应的离子方程为_______ 。
(1)煤的气化过程中,存在如下反应:
①C(s)+O2(g) ⇌CO2(g) ∆H1=-394.1 kJ/mol
②2CO(g)+O2(g)⇌2CO2(g) ∆H2=-566.0 kJ/mol
③2H2(g)+O2(g)⇌2H2O(g) ∆H3=-483.6 kJ/mol
写出利用水煤浆生产水煤气的热化学方程式
(2)已知常温下部分弱电解质的电离平衡常数如表:
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10-4 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 | Kb=1.7×10-5 |
①常温下,物质的量溶度相同的三种溶液①NaF溶液 ②NaClO溶液 ③Na2CO3溶液,其pH由大到小的顺序是
②25°C时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)实验所用NaOH工业上的制备,以电解精制饱和食盐水的方法制取氯气、氢气、烧碱。图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

①写出电解饱和食盐水的离子方程式
②精制饱和食盐水从图中
(4)含有NaCN的污水危害很大,0.01 mol/L的NaCN溶液pH=9,请判断该溶液中:c(CN-)
您最近一年使用:0次
【推荐2】处理电镀污水时会产生大量的电镀污泥,下面是处理某种电镀污泥回收铜、镍元素的一种工业流程:
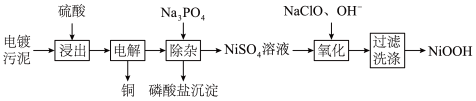
已知:硫酸浸出后得到的浸出液中含有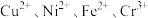 ;
;
回答下列问题:
(1)“浸出”工序中,为提高浸出率可以采取的措施__________ (写出两条)。
(2)在“电解”时,若维持电流强度为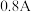 ,电流效率为90%,电解
,电流效率为90%,电解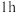 ,理论上可获得铜的质量
,理论上可获得铜的质量____ g(结果保留小数点后两位)。(已知:电流效率是指电解时电极上实际沉积与理论沉积物质的量之比,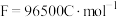 )
)
(3)为提高“除杂”工序的效果,“电解”工序中需控制电解电压稍大一些,其目的是___________ ;磷酸盐沉淀是FePO4、______ (填化学式)。
(4)硫酸镍溶液在强碱性环境下用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。“氧化”工序中反应的离子方程式__________ 。
(5)“过滤、洗涤”工序中,检验沉淀洗涤干净的操作方法________ 。

已知:硫酸浸出后得到的浸出液中含有
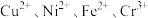 ;
;回答下列问题:
(1)“浸出”工序中,为提高浸出率可以采取的措施
(2)在“电解”时,若维持电流强度为
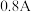 ,电流效率为90%,电解
,电流效率为90%,电解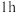 ,理论上可获得铜的质量
,理论上可获得铜的质量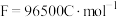 )
)(3)为提高“除杂”工序的效果,“电解”工序中需控制电解电压稍大一些,其目的是
(4)硫酸镍溶液在强碱性环境下用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。“氧化”工序中反应的离子方程式
(5)“过滤、洗涤”工序中,检验沉淀洗涤干净的操作方法
您最近一年使用:0次
【推荐3】A、B、C、D是四种常见的单质,A、B均为金属;C、D常温下均是气体。甲、乙、丙、丁、戊、己为六种常见的化合物。它们之间有如图所示的转化关系:
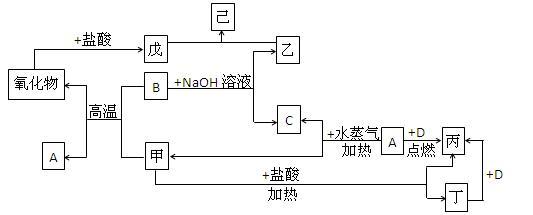
请回答下列问题:
(1)B与甲反应的化学方程式是_________________________ 。
(2)用等质量的B单质以及盐酸、氢氧化钠溶液为原料,制取等质量的己化合物,请你选择出最佳的制取方案,写出该方案有关的离子方程式_____________________ 。你确定该方案最佳的理由是_______________________ 。
(3)电浮选凝聚法是工业上采用的一种污水处理方法,图中是该方法处理污水的实验装置示意图,使用金属A、B为电极,实验过程中,污水的PH始终保持在5.0~6.0之间。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用。
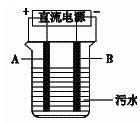
阳极的电极反应式分别是____________________ 、2H2O-4e-=4H++O2↑
阳极区生成沉淀的离子方程式是__________________________ 。

请回答下列问题:
(1)B与甲反应的化学方程式是
(2)用等质量的B单质以及盐酸、氢氧化钠溶液为原料,制取等质量的己化合物,请你选择出最佳的制取方案,写出该方案有关的离子方程式
(3)电浮选凝聚法是工业上采用的一种污水处理方法,图中是该方法处理污水的实验装置示意图,使用金属A、B为电极,实验过程中,污水的PH始终保持在5.0~6.0之间。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用。

阳极的电极反应式分别是
阳极区生成沉淀的离子方程式是
您最近一年使用:0次



