名校
1 . 在一定条件下,可逆反应X(g)+3Y(g) 2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是
2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是
 2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是
2Z(g)达到平衡时,测得X和Y转化的转化率均为25%,下列叙述正确的是| A.升高温度,正反应速率增大,逆反应速率减小 |
| B.开始充入容器中的X、Y物质的量之比为1∶3 |
| C.若Y的反应速率为0.2 mol·L-1·s-1,则Z的反应速率为0.3 mol·L-1·s-1 |
| D.若容器体积不变,向容器中充入氦气,压强增大,反应速率增大 |
您最近一年使用:0次
2023-05-11更新
|
479次组卷
|
3卷引用:宁夏吴忠中学2022-2023学年高一下学期学业水平模拟考试(三)化学(B)试题
名校
解题方法
2 . 下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究反应物浓度对化学反应速率的影响 | 其他条件不变,取两支试管,一支加入10 mL 0.1 mol/L  溶液,另一支加入5 mL 0.1 mol/L 溶液,另一支加入5 mL 0.1 mol/L  溶液、5 mL蒸馏水,同时向两支试管加入10 mL 0.1mol/L 溶液、5 mL蒸馏水,同时向两支试管加入10 mL 0.1mol/L  溶液 溶液 | 前者出现浑浊的时间更短,说明增大 浓度,可以加快反应速率 浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 其他条件不变,在容积固定的密闭容器中发生反应: 向其中通入氩气,反应速率不变 向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 证明溶液是否含 | 向溶液中加入稀氢氧化钠溶液,用湿润的红色石蕊试纸靠近瓶口 | 若试纸未变蓝,则说明不含 |
| D | 探究KI与 反应的限度 反应的限度 | 取1 mL 0.1 mol/L KI溶液于试管中,加入5 mL 0.1 mol/L 溶液,充分反应后滴入5滴15% KSCN溶液 溶液,充分反应后滴入5滴15% KSCN溶液 | 若溶液变血红色,则KI与 的反应有一定限度 的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-11更新
|
609次组卷
|
3卷引用:宁夏石嘴山市第三中学2022-2023学年高二下学期期末理科化学试题
名校
解题方法
3 . 电解锰渣含有 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含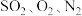 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
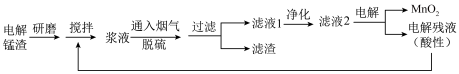
(1)上述流程中为增大反应速率采取的措施有_______ 。
(2)电解锰渣中的 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为_______ 。
(3)电解锰渣与电解残液混合后,浆液中部分离子浓度 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。
①用方程式表示脱硫过程溶液 降低的原因
降低的原因_______ 。
②分析浆液中 浓度增大的原因:
浓度增大的原因:
i. 被
被 还原;
还原;
ii. 被
被 还原,离子方程式为
还原,离子方程式为_______ ;
iii._______ (用离子方程式表示)。
(4)电解获得 ,装置如下图所示。
,装置如下图所示。
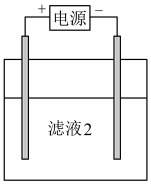
①滤液2在电解池_______ (填“阳”或“阴”)极放电产生 。
。
②净化过程须除去 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:_______ 。
 等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含
等。将电解锰渣与电解残液混合制成浆液,能在脱除烟气(含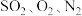 等)中
等)中 的同时,实现电解锰渣的资源化利用。
的同时,实现电解锰渣的资源化利用。
(1)上述流程中为增大反应速率采取的措施有
(2)电解锰渣中的
 能吸收烟气中的
能吸收烟气中的 ,反应的方程式为
,反应的方程式为(3)电解锰渣与电解残液混合后,浆液中部分离子浓度
 及
及 在脱硫过程中的变化如下。
在脱硫过程中的变化如下。 |  |  |  |  | |
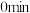 | 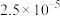 |  | 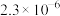 |  | 7.5 |
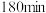 |  | 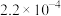 |  | 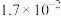 | 1.7 |
 降低的原因
降低的原因②分析浆液中
 浓度增大的原因:
浓度增大的原因:i.
 被
被 还原;
还原;ii.
 被
被 还原,离子方程式为
还原,离子方程式为iii.
(4)电解获得
 ,装置如下图所示。
,装置如下图所示。
①滤液2在电解池
 。
。②净化过程须除去
 。研究发现,滤液2中即使含有少量
。研究发现,滤液2中即使含有少量 ,也会导致
,也会导致 产率大幅降低,分析原因:
产率大幅降低,分析原因:
您最近一年使用:0次
2023-05-07更新
|
550次组卷
|
3卷引用:宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题
宁夏回族自治区石嘴山市平罗中学2023届高三下学期第六次模拟考试理科综合化学试题北京市朝阳区2022-2023年高三下学期第二次模拟考试化学试题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
名校
4 . 一定条件下,容积2L的密闭容器中,将1mol L气体和0.5mol M气体混合,发生如下反应: ,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为
,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为 。计算:
。计算:
(1)化学方程式中a的值为___________ 。
(2)前5s内用M表示的化学反应速率为___________ ,L的转化率为___________ 。
(3)一定能使该反应的速率增大的措施有___________(填字母)。
(4)可认定上述可逆反应在一定条件下已达到化学平衡状态的是___________ (填字母)。
A.体系压强不再变化
B.体系的密度不再变化
C.
D.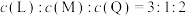
E.Q(g)的物质的量浓度不再发生变化
 ,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为
,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为 。计算:
。计算:(1)化学方程式中a的值为
(2)前5s内用M表示的化学反应速率为
(3)一定能使该反应的速率增大的措施有___________(填字母)。
| A.其他条件不变,充入一定量气体L | B.降低温度 |
| C.保持温度不变,将容器的体积压缩 | D.保持体积不变,充入无关惰性气体 |
A.体系压强不再变化
B.体系的密度不再变化
C.

D.
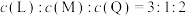
E.Q(g)的物质的量浓度不再发生变化
您最近一年使用:0次
2023-04-26更新
|
328次组卷
|
2卷引用:宁夏吴忠中学2022-2023学年高一下学期学业水平模拟考试(三)化学(B)试题
名校
5 . 定条件下,发生反应A(g)+B(g) C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:
A.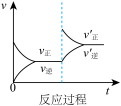 B.
B.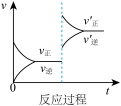 C.
C. D.
D.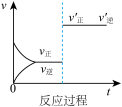 E.
E.
(1)表示升高温度,达到新平衡的是图______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是图______ ,A的转化率______ 。
(3)表示减少C的浓度,达到新平衡的是图______ ,表示使用催化剂,达新平衡的是图。
(4)增加A的浓度,达到新平衡的是图______ ,达到平衡后A的转化率______ 。
 C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是图
(2)表示降低压强,达到新平衡的是图
(3)表示减少C的浓度,达到新平衡的是图
(4)增加A的浓度,达到新平衡的是图
您最近一年使用:0次
2023-04-24更新
|
263次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
解题方法
6 . 碳达峰、碳中和是现在需要继续完成的环保任务,CO2的综合利用成为热点研究对象,CO2作为碳源加氢是再生能源的有效方法,CO2加氢可以合成甲醇,0lah 提出“甲醇经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过CO2加氢生产甲醇是有希望的可再生路线之一,该过程主要发生如下反应:
反应Ⅰ: CO2 (g)+ H2(g) CO(g) +H2O(g) ΔH1
CO(g) +H2O(g) ΔH1
反应Ⅱ: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2=-41.1KJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-41.1KJ·mol-1
(1)①相关键能如下表,则ΔH1=_______ ,该反应的活化能Ea(正)_______ Ea(逆)(填“大于”“小于”或“等于”)。
②若K1、K2分别表示反应Ⅰ、反应Ⅱ的平衡常数。则CO(g) +2H2(g)  CH3OH(g) 的平衡常数K=
CH3OH(g) 的平衡常数K=_______ (用含K1、K2的代数式表示)。
(2)据文献报道,Cu基纳米材料作为高性能催化剂可将CO2电还原为高能量密度的CH3OH,不同催化剂对生成CH3OH的法拉第效率与电极电势的变化如图1所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是________ 。
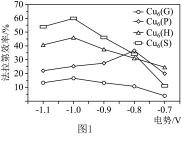
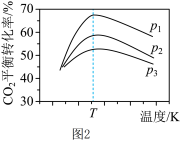
(3)在催化剂作用下,发生上述反应Ⅰ、Ⅱ, 达平衡时CO2的转化率随温度和压强的变化如图2,判断P1、P2、P3的大小关系:_______ ,解释压强一定时,CO2的平衡转化率呈现如图变化的原因:______ 。
(4)某温度下,初始压强为10MPa,向容积为2L的恒容密闭容器中充入2 mol CO2、3 mol H2发生反应Ⅰ、Ⅱ,平衡时CO2的转化率是50%,体系内剩余1 mol H2,反应Ⅱ的Kp=_______ 。
反应Ⅰ: CO2 (g)+ H2(g)
 CO(g) +H2O(g) ΔH1
CO(g) +H2O(g) ΔH1反应Ⅱ: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-41.1KJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-41.1KJ·mol-1(1)①相关键能如下表,则ΔH1=
| 化学键 | H-H | C≡ O | O-H | C=O |
| 键能/ (kJ·mol-1) | 436 | 1071 | 464 | 803 |
 CH3OH(g) 的平衡常数K=
CH3OH(g) 的平衡常数K=(2)据文献报道,Cu基纳米材料作为高性能催化剂可将CO2电还原为高能量密度的CH3OH,不同催化剂对生成CH3OH的法拉第效率与电极电势的变化如图1所示(已知法拉第效率是指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是

(3)在催化剂作用下,发生上述反应Ⅰ、Ⅱ, 达平衡时CO2的转化率随温度和压强的变化如图2,判断P1、P2、P3的大小关系:

(4)某温度下,初始压强为10MPa,向容积为2L的恒容密闭容器中充入2 mol CO2、3 mol H2发生反应Ⅰ、Ⅱ,平衡时CO2的转化率是50%,体系内剩余1 mol H2,反应Ⅱ的Kp=
您最近一年使用:0次
名校
解题方法
7 . 把在空气中久置的铝片5.0g投入盛有50mL0.1mol/L盐酸的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系可用如图所示的坐标曲线来表示,下列推论不正确的是
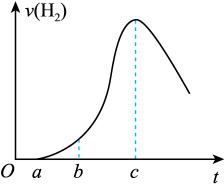

| A.O→a不产生氢气是因为表面的氧化物隔离了铝和稀盐酸 |
| B.b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
| C.t=c时,反应处于平衡状态 |
| D.t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降 |
您最近一年使用:0次
2023-04-22更新
|
390次组卷
|
7卷引用:宁夏银川市育才中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
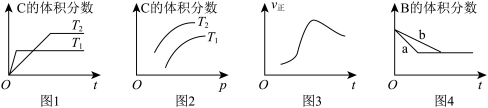
8 . 某化学研究小组探究外界条件对化学反应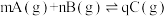 的速率和平衡的影响,如图所示,下列判断错误的是
的速率和平衡的影响,如图所示,下列判断错误的是
 的速率和平衡的影响,如图所示,下列判断错误的是
的速率和平衡的影响,如图所示,下列判断错误的是
A.由图1可知, ,该反应的正反应为放热反应 ,该反应的正反应为放热反应 |
B.由图2可知,该反应的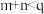 |
| C.图3是绝热条件下正反应速率和时间的图像(从反应物开始投料),由此说明该反应放热 |
| D.图4中,曲线a可能使用了催化剂 |
您最近一年使用:0次
2023-04-01更新
|
455次组卷
|
3卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
9 . 中医药根植于中华传统文化。下列说法不正确 的是
| A.屠呦呦团队用乙醚从青蒿中提取了青蒿素,采用了萃取的方法 |
| B.中药甘草、金银花、石膏、明矾等的主要化学成分都是有机物 |
| C.汤药存放于冰箱中,可以减小其腐败变质的速率 |
| D.煎制草药不宜使用铁质容器,可能因为草药的有些成分能与铁发生反应影响药效 |
您最近一年使用:0次
2023-03-31更新
|
924次组卷
|
6卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题
宁夏平罗中学2022-2023学年高二下学期期中考试化学试题北京市西城区2023届一模考试化学试题(已下线)专题01 化学与STSE(已下线)专题05 元素及其化合物北京师范大学附属实验中学2023-2024学年暑期高三第一次督导化学试题广西柳州高级中学2023-2024学年高三上学期8月开学考试化学试题
名校
解题方法
10 . 为保护环境,充分利用钴资源,一种以废旧钴酸锂电池材料(正极材料主要含有LiCoO2、铝箔及金属钢壳)回收钴酸锂的工艺流程如下:
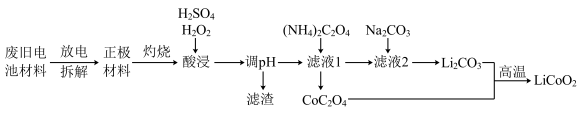
已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
请回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在_________ (填标号)中进行放电。粉碎的目的是_________ 。
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是_________ (填标号)。
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为_________ 。
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为_________ 。

(3)“调pH”时,溶液应控制的pH范围为_________ ,选用的最佳试剂是_________ (填标号)。
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为_________ 。

已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
| 离子 | Co3+ | Fe3+ | Co2+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 0.3 | 2.7 | 7.2 | 7.6 | 3.6 |
| 完全沉淀的pH | 1.1 | 3.2 | 9.2 | 9.6 | 5.2 |
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理。放电方式为电化学放电,可以将废旧电池浸泡在
A. Na2SO4溶液
B.98%的H2SO4溶液
C.酒精
(2)“酸浸”过程中,除加入H2SO4,还要加入H2O2。
①H2O2的作用是
A.做氧化剂
B.做还原剂
C.既做氧化剂又做还原剂
②H2O2促进了LiCoO2在H2SO4中转化为CoSO4,该反应的离子方程式为
③相同条件下,“酸浸”时钴的浸出率随温度变化如右图所示,此时温度控制在80°C左右的原因为

(3)“调pH”时,溶液应控制的pH范围为
A. H2SO4 B. CoCO3 C.石灰乳 D. NaOH
(4)高温时,CoC2O4和Li2CO3生成LiCoO2的同时放出CO2。此反应的化学方程式为
您最近一年使用:0次
2023-03-29更新
|
334次组卷
|
2卷引用:宁夏平罗中学2022-2023学年高二下学期期中考试化学试题(重点班)



