名校
1 .  与
与 在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法错误 的是

 与
与 在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
在镍基催化剂催化作用下能发生如图所示的可逆反应,下列说法
| A.催化剂能降低反应的活化能,增大单位体积内的活化分子百分数 |
B.更换更高效的催化剂,能提高 的平衡转化率 的平衡转化率 |
C.图示反应过程中有 键的断裂与形成 键的断裂与形成 |
D.该过程的总反应为 |
您最近一年使用:0次
名校
2 . 某反应的反应机理可以分成如下两步,下列说法错误的是
| 反应机理 | 第一步反应 | 第二步反应 |
 (慢反应) (慢反应) | 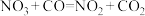 (快反应) (快反应) |
| A.在条件相同时,该反应的速率由第一步反应速率决定 |
| B.该反应的总反应方程式为NO2+CO=NO+CO2 |
| C.升高温度只会影响第一步反应速率,对第二步反应速率无影响 |
| D.加入合适的催化剂可降低反应的活化能,加快反应速率 |
您最近一年使用:0次
2024-01-01更新
|
144次组卷
|
12卷引用:四川省兴文第二中学校2023-2024学年高二上学期11月期中考试化学试题
四川省兴文第二中学校2023-2024学年高二上学期11月期中考试化学试题陕西省渭南市杜桥中学2023-2024学年高二上学期期中考试化学试卷 湖北省武汉市新洲区第一中学2024届高二上学期11月阶段测试化学试题安徽省A10联盟2022届高三上学期摸底考试化学试题吉林省洮南市第一中学2021-2022学年高二上学期第一次月考化学试题陕西省宝鸡市金台区2021-2022学年高二上学期期中考试化学(理)试题(已下线)必考点02 化学反应速率-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)2021年广东省高考化学试卷变式题11-21吉林省长春市第二十中学2021-2022学年高二上学期第一次质量检测化学试题湖北省武汉市部分学校2021-2022学年高二上学期12月联考化学试题(已下线)专题02 化学反应速率-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
名校
解题方法
3 .  可催化
可催化 分解,机理,Ⅰ:
分解,机理,Ⅰ: ;Ⅱ:
;Ⅱ: 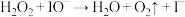 。反应过程中能量变化如图所示,下列判断正确的是
。反应过程中能量变化如图所示,下列判断正确的是
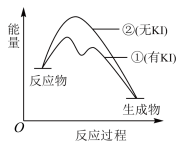
 可催化
可催化 分解,机理,Ⅰ:
分解,机理,Ⅰ: ;Ⅱ:
;Ⅱ: 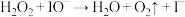 。反应过程中能量变化如图所示,下列判断正确的是
。反应过程中能量变化如图所示,下列判断正确的是
A. 是放热反应 是放热反应 | B. 分解反应的速率由机理Ⅰ决定 分解反应的速率由机理Ⅰ决定 |
C.KI能改变总反应的 | D. 不改变 不改变 分解反应的途径 分解反应的途径 |
您最近一年使用:0次
2023-12-19更新
|
96次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高二上学期期中考试化学试题
名校
4 . 下列有关速率和平衡说法正确的是
| A.已知反应:CaCO3(s)⇌CaO(s)+CO2(g),在密闭的反应炉内达到平衡后,若其他条件均不改变,将反应炉体积缩小一半,则达到新平衡时CO2(g)的浓度将升高 |
| B.H2、I2、HI平衡混合气体加压后颜色变深,能用勒夏特列原理解释 |
C.重铬酸钾溶液中存在: (橙色) (橙色) (黄色) (黄色) ,若滴加少量NaOH溶液,平衡正移,溶液由橙色变黄色 ,若滴加少量NaOH溶液,平衡正移,溶液由橙色变黄色 |
| D.使用正催化剂,改变了反应历程和∆H,降低了反应的活化能,增大了活化分子百分数,化学反应速率增大 |
您最近一年使用:0次
2023-11-21更新
|
121次组卷
|
2卷引用:四川省成都列五中学2023-2024学年高二上学期10月月考化学试题
5 . 已知2H2O(l)=2H2(g)+O2(g) ∆H=+571.0 kJ·mol-1,两步热循环制H2的过程如图。下列说法正确的是
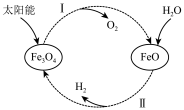
过程I:2Fe3O4(s)=6FeO(s)+O2(g) ∆HⅠ =+604.8 kJ·mol-1
过程II:H2O(l)+3FeO(s)=Fe3O4(s)+H2(g) ∆H II

过程I:2Fe3O4(s)=6FeO(s)+O2(g) ∆HⅠ =+604.8 kJ·mol-1
过程II:H2O(l)+3FeO(s)=Fe3O4(s)+H2(g) ∆H II
| A.该制氢过程中FeO为催化剂 |
| B.整个过程中能量转化形式只存在太阳能转化为化学能 |
| C.过程II在任何温度下均为自发反应 |
| D.根据盖斯定律∆H I+∆H II=0 |
您最近一年使用:0次
2023-11-12更新
|
369次组卷
|
2卷引用:四川省成都市第七中学2023-2024学年高二上学期期中考试化学试题
名校
6 . 下列关于有效碰撞理论的说法一定正确的是
| A.活化分子之间发生的碰撞一定是有效碰撞 |
| B.增大压强,反应的有效碰撞次数增多,反应速率加快 |
| C.升高温度,反应的活化能降低,反应速率加快 |
| D.使用催化剂,单位体积内活化分子数增多,反应速率加快 |
您最近一年使用:0次
2023-11-10更新
|
59次组卷
|
2卷引用:四川省南充市嘉陵第一中学2023-2024学年高二上学第三次月考化学试题
7 . 目前,常用三元催化将汽车尾气中NO和CO转化为CO2和N2。在密闭容器中模拟进行如下反应:2NO(g)+2CO(g) 2CO2(g)+N2(g) △H<0。达到平衡后,其他条件不变,分别改变下列条件。用“正反应方向”“逆反应方向”或“不”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断其他物理量变化情况。
2CO2(g)+N2(g) △H<0。达到平衡后,其他条件不变,分别改变下列条件。用“正反应方向”“逆反应方向”或“不”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断其他物理量变化情况。
(1)增加CO的浓度,平衡向_______ 移动,该反应的平衡常数K_______ 。
(2)保持反应容器压强和温度不变,通入He,平衡向_______ 移动,该化学反应速率_______ ,该反应的△H_______ 。
(3)在一定温度下,缩小反应容器体积,平衡向_______ 移动,NO(g)的转化率_______ 。
(4)使用相同质量的同种催化剂,增大催化剂的比表面积,平衡_______ 移动,该化学反应速率将_______ 。
 2CO2(g)+N2(g) △H<0。达到平衡后,其他条件不变,分别改变下列条件。用“正反应方向”“逆反应方向”或“不”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断其他物理量变化情况。
2CO2(g)+N2(g) △H<0。达到平衡后,其他条件不变,分别改变下列条件。用“正反应方向”“逆反应方向”或“不”分析判断平衡移动情况,用“增大”“减小”或“不变”分析判断其他物理量变化情况。(1)增加CO的浓度,平衡向
(2)保持反应容器压强和温度不变,通入He,平衡向
(3)在一定温度下,缩小反应容器体积,平衡向
(4)使用相同质量的同种催化剂,增大催化剂的比表面积,平衡
您最近一年使用:0次
2023-11-05更新
|
262次组卷
|
2卷引用:四川省成都市彭州市2023-2024学年高二上学期期中考试化学试题
名校
8 . 甲酸常被用于橡胶、医药等工业。在一定条件下可分解生成CO和H2O无、有催化剂条件下的能量与反应历程的关系分别如图1、图2所示。下列说法错误的是
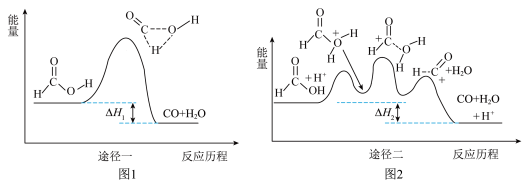

| A.途径一和途径二中甲酸的平衡转化率相等 |
| B.ΔH1<ΔH2<0 |
| C.途径二使用了H+作为催化剂 |
D.途径二反应的快慢由生成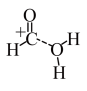 的速率决定 的速率决定 |
您最近一年使用:0次
2023-11-01更新
|
403次组卷
|
5卷引用:四川省德阳市第五中学2023-2024学年高三上学期期中考试化学试题
名校
9 . 下列说法正确的是
| A.Fe和Mg与0.1mol•L-1的盐酸反应,反应速率相同 |
| B.催化剂能降低分子活化时所需能量,使活化分子百分数大大增加 |
| C.1L0.1mol•L-1的盐酸与1L0.05mol•L-1H2SO4分别与大小、形状相同的大理石反应,反应速率相同 |
| D.100mL2mol•L-1的盐酸与锌片反应,加入适量的NaCl溶液,反应速率不变 |
您最近一年使用:0次
名校
解题方法
10 . 下列措施与化学反应速率无关的是
| A.炉膛内用煤粉代替煤块 |
| B.食物冷藏在冰箱 |
| C.糖果制作过程中添加着色剂 |
| D.过氧化氢制氧气时,加入氯化铁溶液 |
您最近一年使用:0次
2023-10-27更新
|
37次组卷
|
2卷引用:四川省泸县第一中学2023-2024学年高二上学期12月月考化学试题



